-
镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素,镓的原子序数为31,属ⅢA元素,镓的熔点29.78℃,沸点高达2403℃,镓有过冷现象(即冷至熔点以下不凝固),它可过冷到-120℃。下列有关镓的性质及用途的叙述不正确的是
A.镓是制造高温温度计的上佳材料
B.镓能溶于强酸或强碱溶液中
C.镓与锌、锡等金属制成合金,可提高其硬度
D.镓可用于制造半导体材料,这是因为镓的导电性介于导体和绝缘体之间
高三化学选择题中等难度题查看答案及解析
-
镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素,镓的原子序数为31,属ⅢA元素,镓的熔点为29.78℃,沸点高达2403℃,镓有过冷现象(即冷至熔点以下不凝固),它可过冷到-120℃。下列有关镓的性质及其用途的叙述不正确的是 ( )
A.镓是制造高温温度计的上佳材料
B.镓能溶于强酸或强碱溶液中
C.镓与锌、锡等金属制成合金,可提高其硬度
D.镓可用于制造半导体材料,这是因为镓的导电性介于导体和绝缘体之间
高三化学单选题中等难度题查看答案及解析
-
镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素,镓的原子序数为31,属ⅢA元素,镓的熔点为29.78℃,沸点高达2403℃,镓有过冷现象(即冷至熔点以下不凝固),它可过冷到-120℃。下列有关镓的性质及其用途的叙述不正确的是( )
A.镓是制造高温温度计的上佳材料
B.镓能溶于强酸或强碱溶液中
C.镓与锌、锡等金属制成合金,可提高其硬度
D.镓可用于制造半导体材料,这是因为镓的导电性介于导体和绝缘体之间
高三化学选择题中等难度题查看答案及解析
-
镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素,镓的原子序数为31,属ⅢA元素,镓的熔点为29.78℃,沸点高达2403℃,镓有过冷现象(即冷至熔点以下不凝固),它可过冷到-120℃。下列有关镓的性质及其用途的叙述不正确的是
A、镓是制造高温温度计的上佳材料
B、镓能熔于强酸强碱溶液中
C、镓与锌、锡等金属支撑合金,可提高其硬度
D、镓可用于制造半导体材料,这是因为镓的导电性介于导体和绝缘体之间
高三化学选择题简单题查看答案及解析
-
镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素,镓的原子序数为31,属ⅢA元素,镓的熔点为29.78℃,沸点高达2403℃,镓有过冷现象(即冷至熔点以下不凝固),它可过冷到-120℃.下列有关镓的性质及其用途的叙述不正确的是( )
A.镓是制造高温温度计的上佳材料
B.镓能溶于强酸或强碱溶液中
C.镓与锌、锡等金属制成合金,可提高其硬度
D.镓可用于制造半导体材料,这是因为镓的导电性介于导体和绝缘体之间高三化学选择题中等难度题查看答案及解析
-
镓是1871年俄国化学家门捷列夫在编制元素周期表时曾预言的“类铝”元素,镓的原子序数为31,属ⅢA元素,镓的熔点为29.78℃,沸点高达2403℃,镓有过冷现象(即冷至熔点以下不凝固),它可过冷到-120℃。下列有关镓的性质及其用途的叙述不正确的是
A.镓是制造高温温度计的上佳材料
B.镓能溶于强酸或强碱溶液中
C.镓与锌、锡等金属制成合金,可提高其硬度
D.镓可用于制造半导体材料,这是因为镓的导电性介于导体和绝缘体之间
高三化学选择题中等难度题查看答案及解析
-
下列有关化学史知识不正确的是( )
A.原子分子学说的建立是近代化学发展的里程碑
B.俄国科学家门捷列夫发现了元素周期律,编制了周期表
C.扫描隧道显微镜的研制成功能够清楚地观察到原子的图象和动态化学变化
D.英国科学家道尔顿首先发现了电子
高三化学选择题简单题查看答案及解析
-
为纪念编制元素周期表的俄国化学家,人们把第101号元素(人工合成元素)命名为钔(元素符号为Md),这位科学家是( )
A.拉瓦锡
B.波尔
C.门捷列夫
D.道尔顿高三化学选择题中等难度题查看答案及解析
-
元素周期律和元素周期表是学习化学的重要工具,下列说法正确的是
A.门捷列夫根据原子量排列的周期表成功预言了类铝(镓)、类硅(锗)等元素的存在
B.铀(U)属于过渡元素,能跟氟形成UF6,据此可推测U原子最外层有6个电子
C.HF、HCl、HBr、HI的还原性依次增强,热稳定性依次减弱,沸点依次升高
D.Na、Mg、Al原子的最外层电子数依次增加,故失去电子的能力越来越强
高三化学选择题简单题查看答案及解析
-
Ⅰ.1871 年门捷列夫最早预言了类硅元素锗,1886 年德国化学家温克勒发现和分离了锗元素,并以其祖国的名字命名为“Ge”。锗是重要的半导体材料,其有机化合物在治疗癌症方面有着独特的功效。下图为工业上利用锗锌矿(主要成分GeO2和ZnS)来制备高纯度锗的流程。
已知:
1.丹宁是一种有机沉淀剂,可与四价锗络合形成沉淀;
2.GeCl4易水解,在浓盐酸中溶解度低。
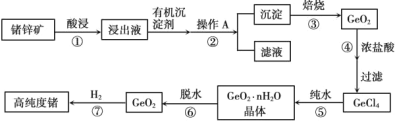
(1)锗元素在周期表中的位置:_____。
(2)步骤②操作A方法是_____。
(3)步骤③中的物质在_____(填仪器名称)中加热。
(4)步骤④不能用稀盐酸,原因可能是_____。
(5)写出步骤⑦的化学方程式_____。
Ⅱ.将过量的氨水加到硫酸铜溶液中,溶液最终变成深蓝色,继续加入乙醇,析出晶体Cu(NH3)4SO4·H2O。
(1)Cu2+基态核外电子排布式为 _________;1mol [Cu(NH3)4]2+中
键的数目为_______。
(2)SO42-的S原子轨道杂化类型_______________。
(3)NH3极易溶于H2O中,原因为______________________。
高三化学工业流程困难题查看答案及解析