-
(1)已知下列两个热化学方程式:
C3H8(g)+5O2(g) 3CO2(g)+4H2O(l) ΔH=-2220.0 kJ·mol-1
H2O(l) H2O(g) ΔH=+44.0 kJ·mol-1
则0.5 mol丙烷燃烧生成CO2和气态水时释放的热量为 。
(2)已知:TiO2(s)+2Cl2(g) TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g) 2CO(g) ΔH=-221 kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如右图所示 ),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN
),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________kJ能量。
N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________kJ能量。
(4)阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:
2H2+O2 2H2O,电解质溶液为稀H2SO4溶液,电池放电时是将___________能转化为__________能。其电极反应式分别为:负极_________________,正极____________________。
-
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。已知:C3H8(g)+5O2(g)—→3CO2(g)+4H2O(l)+2220.0kJ
C3H6(g)+4.5O2(g)—→3CO2(g)+3H2O(l)+2049kJ
下列说法正确的是( )。
A. 1molC3H8(g)与5molO2(g)反应生成3molCO2(g)和4molH2O(g)放出热量大于2220.0kJ
B. 1molC3H6与4.5molO2反应生成3molCO2和3molH2O放出热量等于2049.0kJ
C. 丙烷分子储存的能量大于丙烯分子
D. 丙烷转化为丙烯的过程是一个吸热过程
-
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).已知:C3H8(g)+5O2(g)-→3CO2(g)+4H2O(l)+2220.0kJ;C3H6(g)+4.5O2(g)-→3CO2(g)+3H2O(l)+2049kJ,下列说法正确的是( )
A.1molC3H8(g)与5molO2(g)反应生成3molCO2(g)和4molH2O(g)放出热量大于2220.0kJ
B.1molC3H6与4.5molO2反应生成3molCO2和3molH2O放出热量等于2049.0kJ
C.丙烷分子储存的能量大于丙烯分子
D.丙烷转化为丙烯的过程是一个吸热过程
-
已知:
H2(g)+ O2(g)═H2O(l)△H=﹣285.8kJ/mol;
O2(g)═H2O(l)△H=﹣285.8kJ/mol;
C3H8(g)+5O2(g)═3CO2(g)+4H2O(l)△H=﹣2220.0kJ/mol;
H2O(l)═H2O(g)△H=+44.0kJ/mol.
(1)写出丙烷燃烧生成CO2和气态水的热化学方程式:
(2)实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热6262.5kj,则混合气体中H2和C3H8的体积比为多少?
-
已知下列两个热化学方程式:
H2(g)+1/2O2(g)=H2O(l) △H=-285.8kJ·mol-1
C3H8(g)+5O2(g)= 3CO2(g)+4H2O(l) △H=-2220.0kJ·mol-1
(1)实验测得H2和C3 H8的混合气体共5 mol,完全燃烧生成液态水时放热6264.5kJ,则混合气体中H2和C3 H8的体积比是_______________;
(2)已知:H2O(l)==H2O(g) △H=+44.0kJ·mol-1,写出丙烷燃烧生成CO2和气态水的热化学方程式__________________________________________________ 。
-
已知下列两个热化学方程式:
2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l) △H=-2220.0kJ·mol-1
实验测得氢气和丙烷的混和气体共5 mol完全燃烧时放热3363.2kJ,则混和气体中氢气与丙烷的物质的量分别是多少?
-
已知下列两个热化学方程式;
H2(g)+ O2(g)═H2O(1);△H=-285.0kJ/mol
O2(g)═H2O(1);△H=-285.0kJ/mol
C3H8(g)+5O2(g)═3CO2(g)+4H2O(1);△H=-2220.0kJ/mol
(1)实验测得H2和C3H8的混合气体共5mol,完全燃烧生成液态水时放热3360kJ,则混合气体中H2和C3H8的体积比是______.
(2)已知:H2O(1)=H2O(g);△H=+44.0kJ/mol
写出丙烷燃烧生成CO2和气态水的热化学方程式______.
-
已知下列两个热化学方程式2H2(g)+O2(g)=2H2O(1) △H=-571.6 kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(1) △H=-2220.0 kJ/mol
实验测得,5mol氢气和丙烷的混合气体完全燃烧时放热3847kJ,则混合气体中氢气与丙
烷的体积比是()
A. 1:3 B. 3:1 C. 1:4 D. 1:1
-
(1)已知下列两个热化学方程式:
C3H8(g)+5O2(g) =3CO2(g)+4H2O(l) ΔH=-2220.0 kJ·mol-1
H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
则0.5 mol丙烷燃烧生成CO2和气态水时释放的热量为___________________。
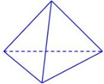
(2)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如下图所示),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________ kJ能量。
N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________ kJ能量。
(3)阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:
2H2+O2 =2H2O,电解质溶液为稀H2SO4溶液,电池放电时是将_________能转化为___________能。其电极反应式分别为:
负极_________________________,正极_____________________________。
-
(1)已知下列两个热化学方程式:
C3H8(g)+5O2(g) =3CO2(g)+4H2O(l) ΔH=-2220.0 kJ·mol-1
H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
则0.5 mol丙烷燃烧生成CO2和气态水时释放的热量为 。
(2)已知:TiO2(s)+2Cl2(g)=TiCl4(l)+O2(g) ΔH=+140 kJ·mol-1
2C(s)+O2(g)=2CO(g) ΔH=-221 kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式: 。
(3)科学家已获得了极具理论研究意义的N4分子,其结构为正四面体(如图所示),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出 kJ能量。
N键吸收941kJ热量,则1molN4气体转化为2molN2时要放出 kJ能量。

(4)阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池总反应为:2H2+O2=2H2O,电解质溶液为稀H2SO4溶液,电池放电时是将 能转化为 能。其电极反应式分别为:负极 ,正极 。
 ),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molN
),与白磷分子相似。已知断裂1molN—N键吸收193kJ热量,断裂1molNN键吸收941kJ热量,则1molN4气体转化为2molN2时要放出______________kJ能量。

