-
(16分)X、Y、Z是三种短周期元素。已知三种元素的原子序数按X、Y、Z的顺序依次增大,且原子序数之和为33,最外层电子数之和为11。在周期表中,X、 Z上下相邻,Y、Z左右相邻。
(1)X、 Y、Z的元素符号分别为________、________、________。
(2) Y的氧化物是________性氧化物,X、Z的最高价氧化物的水化物酸性强弱为________ >
________(填物质的化学式)。
(3) X和Z分别能与氧形成XO2和ZO2,XO2在固态时属于________晶体,ZO2在固态时属于________晶体;XO2的电子式为________。
(4)Y的最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式为________。
高一化学填空题简单题查看答案及解析
-
X、Y、Z、M、W为五种短周期元素,X、Y、Z是原子序数依次递增的同周期元素,最外层电子数之和为15,X与Z可形成XZ2分子;Y与M形成的气态化合物在标准状态下的密度为0.76g/L;W的质子数是X、Y、Z、M四种元素质子数之和的一半。下列说法正确的是
A. 原子半径W>Z>Y>X>M
B. 将XZ2通入W单质与水反应后的溶液中,生成的盐一定只有一种
C. 由X、Y、Z、M四种元素共同形成的化合物中一定有共价健可能有离子键
D. CaX2、CaM2、CaZ2等3种化合物中,阳离子与阴离子个数比均为1:2
高一化学单选题中等难度题查看答案及解析
-
短周期主族元素 W、 X、 Y、 Z 的原子序数依次增大,W的最外层电子数是内层电子数的3倍,X所在的周期数是最外层电子数的3倍,由 W、 X、 Y 三种元素形成的一种盐溶于水后,加入盐酸,产生的无色气体能使品红褪色。下列说法正确的是( )
A. W 与 X 可形成至少两种化合物
B. X 的简单离子与 Z 的简单离子具有相同的电子层结构
C. 最高价氧化物对应水化物的酸性: Y>Z
D. 简单气态氢化物的稳定性: W<Y
高一化学单选题中等难度题查看答案及解析
-
A、B、C均为短周期元素,它们在周期表中的位置如图所示.已知:B、C两元素原子最外层电子数之和等于A元素原子最外层电子数的2倍;B、C两元素的核电荷数之和是A元素原子序数的4倍.则A、B、C分别是( )
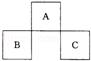
A.C、Al、P B.N、Si、S C.0、P、Cl D.F、S、Ar
高一化学选择题中等难度题查看答案及解析
-
A、B、C均为短周期元素,它们在周期表中的位置如图所示.已知:B、C两元素原子最外层电子数之和等于A元素原子最外层电子数的2倍;B、C两元素的核电荷数之和是A元素原子序数的4倍.则A、B、C分别是( )
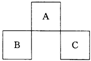
A.C、A.l、P
B.N、Si、S
C.0、P、Cl
D.F、S、Ar高一化学选择题中等难度题查看答案及解析
-
A、B、C均为短周期元素,它们在周期表中的位置如图所示.已知:B、C两元素原子最外层电子数之和等于A元素原子最外层电子数的2倍;B、C两元素的核电荷数之和是A元素原子序数的4倍.则A、B、C分别是( )
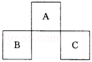
A. C、Al、P B. N、Si、S C. 0、P、Cl D. F、S、Ar
高一化学选择题中等难度题查看答案及解析
-
A、B、C均为短周期元素,它们在周期表中的位置如左图所示。已知:B、C两元素原子最外层电子数之和等于A元素原子最外层电子数的2倍;B、C两元素的核电荷数之和是A元素原子序数的4倍。则A、B、C分别是
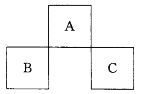
A. C、Al、P B. N、Si、S
C. O、P、Cl D.F、S、Al
高一化学单选题中等难度题查看答案及解析
-
已知X、Y、Z、W四种元素分布在元素周期表中的三个不同短周期元素里,且原子序数依次增大,X、W同主族,Y、Z为同周期的相邻元素,W原子的质子数等于Y、Z原子最外层电子数之和,Z原子最外层电子数是次外层电子数的3倍.试推断:
(1)写出X、Y的元素符号:X______、Y______.
(2)W+和Z2-的核外电子排布相同,两种微粒半径大小关系为______.
(3)由X、Y、Z所形成的离子化合物的化学式是______,它与W的最高价氧化物的水化物的溶液反应时的离子方程式是______.
(4)已知拆开1mol X-X键、1mol Y≡Y、1mol Y-X键分别需要吸收的能量为436kJ、946kJ、391kJ.则由X2和Y2反应生成1mol YX3,需要______(填“放出”或“吸收”)的热量是______kJ.高一化学解答题中等难度题查看答案及解析
-
已知X、Y、Z、W四种元素分别是元素周期表中三个连续短周期的元素,且原子序数依次增大。X、W同主族,Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z 原子的最外层电子数之和。Z原子最外层电子数是次外层电子数的3倍,试推断:
(1)上述元素两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为 ,含有离子键和非极性
共价键的化合物的电子式为 ;含有极性共价键和非极性共价键的化合物的电子式为 。
(2)由X、Y、Z所形成的常见离子化合物是 (写化学式),该化合物与[W的最高价氧化物对应水化物的浓溶液加热时反应的离子方程式为 。
高一化学推断题困难题查看答案及解析
-
(12分)A、B、C、D、E是五种短周期元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
物质组成
甲
乙
丙
丁
化合物中各元素
原子个数比
A和C
1:1
B和A
1:4
D和E
1:3
B和E
1:4
请回答下列问题:
⑴C的氢化物与乙相比较,稳定性强弱关系(用相应的化学式表示): _____>___
⑵元素E在周期表中的位置为第 周期 族
⑶请写出两种与乙具有相同电子数的非单核离子的化学式:_____和_____
⑷把D的单质放到NaOH溶液中,反应的化学方程式为:______________________
⑸写出甲的电子式:________________
⑹有200mL MgCl2和丙的混合溶液,其中c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3 mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1 NaOH 溶液的体积是: _____
高一化学填空题简单题查看答案及解析