(1)请将NaBiO3之外的反应物与生成物分别填入以下空格内.

(2)反应中,被氧化的元素是______,氧化剂是______.
(3)将氧化剂与还原剂及其已配平的化学计量数填入下列空格中,并标出电子转移的方向和数目.
高三化学解答题中等难度题

高三化学解答题中等难度题

高三化学解答题中等难度题查看答案及解析

高三化学解答题中等难度题查看答案及解析
某反应体系中有物质:Bi2(SO4)3、NaMnO4、H2O、MnSO4、NaBiO3、Na2SO4、H2SO4。
(1)请将NaBiO3之外的反应物与生成物分别填入以下空格内。
(2)反应中,被氧化的元素是____________,氧化剂是___________。
(3)将氧化剂与还原剂及其已配平的化学计量数填入下列空格中,并标出电子转移的方向和数目。
高三化学填空题中等难度题查看答案及解析
Ⅰ、已知将浓盐酸滴入高锰酸钾溶液中,产生黄绿色气体,而溶液的紫红色褪去。现有一个氧化还原反应的体系中共有KCl.Cl2.H2SO4.H2O.KMnO4.MnSO4.K2SO4七种物质:
(1)该反应中,化合价升高的反应物是 。
(2)写出一个包含上述七种物质的氧化还原反应方程式:
(3)上述反应中,氧化剂是 ,1 mol氧化剂在反应中得到 mol电子。
Ⅱ、某研究性学习小组利用下列装置制备漂白粉,并进行漂白粉有效成分的质量分数测定

(1)装置④中的x试剂为________。
(2)装置③中发生反应的化学方程式为________。该反应是放热反应,反应温度较高时有副反应发生。改进该实验装置以减少副反应发生的方法是________
_________________________。
(3)测定漂白粉有效成分的质量分数
称取1.000 g漂白粉于锥形瓶中,加水溶解,调节溶液的pH,以淀粉为指示剂,用0.1000 mol·L-1 KI溶液进行滴定,溶液出现稳定浅蓝色时为滴定终点。反应原理为:
3ClO-+ I- = 3Cl-+ IO3- IO3- + 5I- + 3H2O = 6OH- + 3I2
实验测得数据如下表所示。
| 滴定次数 | 1 | 2 | 3 |
| KI溶液体积/mL | 19.98 | 20.02 | 20.00 |
该漂白粉中有效成分的质量分数为________。若滴定过程中未充分振荡溶液局部变浅蓝色时就停止滴定,则测定结果将________(填“偏高”、“偏低”或“无影响”)
高三化学实验题极难题查看答案及解析
高三化学解答题中等难度题查看答案及解析
将NaBiO3固体(黄色,微溶)加入到MnSO4和H2SO4的混合溶液里,加热,溶液显紫色(Bi3+无色)。配平该反应的离子方程式:
________NaBiO3+________Mn2++________________________Na++________Bi3++_______________+______________。
高三化学填空题中等难度题查看答案及解析
已知KBiO3+MnSO4+H2SO4→Bi2(SO4)3+KMnO4+H2O+K2SO4(未配平),利用上述化学反应设计成如图所示原电池(盐桥中装有含琼胶的饱和K2SO4溶液),下列说法正确的是( )

A.电池工作时,电子移向为石墨Ⅰ→溶液→盐桥→溶液→石墨Ⅱ
B.电池工作时,盐桥中的K+移向甲烧杯
C.甲烧杯中发生的电极反应为Mn2+﹣4e﹣+4H2O═MnO4﹣+8H+
D.电池工作一段时间后乙烧杯中溶液的pH增大
高三化学选择题简单题查看答案及解析
给出下列氧化还原反应,试回答下列问题。
(1)KMnO4+ KI+ H2SO4 K2SO4+ MnSO4 + I2十 H2O
配平化学反应方程式 被还原的元素 ,发生氧化反应的物质 。
(2)3Cl2 + 6NaOH5NaCl + NaClO3 + 3H2O
用双线桥标出电子转移的方向和数目 氧化剂与还原剂的物质的量之比为 ,氧化产物是 。
(3)11P+15CuSO4+24H2O=6H3PO4+15H2SO4+5Cu3P(反应中Cu3P中的P为负三价)。
该反应中Cu2+表现 性(填氧化或还原);11molP中被P氧化的P是 mol
高三化学填空题困难题查看答案及解析
(10分)某化学反应的反应物和产物如下:
KMnO4 + KI+ H2SO4→ MnSO4 + I2 + KIO3 + K2SO4 + H2O
(1)该反应的氧化剂是________。________
(2)如果该反应方程式中I2和KIO3的化学计量数都是5
①KMnO4的化学计量数是________ 。
②在下面的化学式上标出电子转移的方向和数目
KMnO4 + KI + H2SO4 →
(3)如果没有对该方程式中的某些化学计量数作限定,可能的配平化学计量数有许多组。原因是________。
高三化学填空题简单题查看答案及解析
银锌蓄电池应用广泛,放电时总反应为Zn+Ag2O2+H2O==Zn(OH)2+Ag2O,某小组以银锌蓄电池为电源,用惰性电极电解饱和Na2SO4溶液制备H2SO4和NaOH,设计如图所示装置。连通电路后,下列说法正确是
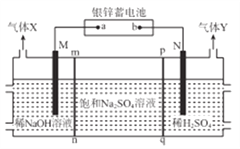
A. 电池的a极反应式为Ag2O2+H2O+2e-=Ag2O+2OH-
B. 气体Y为H2
C. pq膜适宜选择阳离子交换膜
D. 电池中消耗65gZn,理论上生成1mol 气体X
高三化学单选题困难题查看答案及解析