-
下表为元素周期表的一部分,a、b、c…为部分元素.回答下列问题:
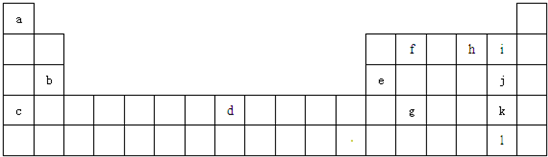
(1)请写出上述元素d的价电子排布式___________;
(2)请写出j的单质与a、h形成的化合物发生反应的化学方程式___________;
(3)请比较b、e、j三种元素的第一电离能由大到小的顺序___________(写元素符号);
(4)请写出e元素最高价氧化物对应的水合物与a、c、h三种元素形成的化合物反应的离子方程式___________;
(5)j、k、l三种元素之间能以原子个数比1:1两两形成互化物,这些互化物的性质类似于这些元素单质的性质.请写出k、l的互化物的电子式___________,它是由___________键形成的(根据原子轨道的重叠程度填写)。
高二化学填空题中等难度题查看答案及解析
-
下表为元素周期表的一部分,a、b、c……为部分元素。回答下列问题:

(1)请写出上述元素c原子基态核外电子排布式_______________; d+基态核外电子排布式_______________________________。
(2)请写出一个能比较f、h非金属性强弱的反应的化学方程式___________________。
(3)请比较f、h、i 三种元素的第一电离能由大到小的顺序________(写元素符号);b、e、j三种元素的电负性由大到小的顺序________(写元素符号)。i2-与b+两种微粒半径大小: i2-___b+ (填>、=或<)。
(4)请写出e 元素最高价氧化物对应的水化物与a、b、i三种元素形成的化合物反应 的离子方程式___________________________________________。
高二化学填空题中等难度题查看答案及解析
-
下表为元素周期表的一部分。请回答下列问题:
①
②
③
④
⑤
⑥
⑦
⑧
⑨
(1)上述元素中,属于d区的是________(填元素符号)。
(2)写出元素⑨的基态原子的价电子排布式___________________________。
(3)元素第一电离能为③___④,电负性③___④(填“>”或“<”)。
(4)元素③气态氢化物分子为_______分子(填“极性”或“非极性”)。向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为_______________________________________。
(5)元素⑥的单质的晶体中原子的堆积方式如下图甲所示,其晶胞特征如下图乙所示,原子之间相互位置关系的平面图如下图丙所示.
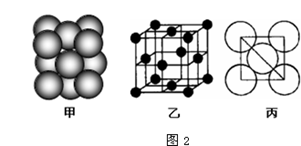
若已知⑥的原子半径为dcm,NA代表阿伏加德罗常数的值,元素⑥的相对原子质量为M,则一个晶胞中⑥原子的个数为______,该晶体的密度为_________(用M、NA、d表示).
高二化学简答题中等难度题查看答案及解析
-
(9分)下表为元素周期表的一部分,a、b、c……为部分元素。回答下列问题:
a
f
h
i
b
e
j
c
d
g
k
l
(1)请写出d在元素周期表中的位置 ;
(2)请写出上述元素k的核外电子排布式 ;
(3)b、e、j三种元素的电负性由大到小的顺序 (写元素符号);此三种元素的第一电离能由大到小的顺序 (写元素符号);
(4)g、e两种元素的最高价氧化物对应的水合物的化学性质相似,请写出e元素最高价氧化物对应的水化物与a、c、h三种元素形成的化合物反应的离子方程式 ;
(5)j、k、l三种元素之间能以原子个数比1∶1两两形成互化物,这些互化物的性质类似于这些元素单质的性质。请写出k、l的互化物的电子式 ,它是由 键形成的 化合物(填“离子”或“共价”)。
高二化学填空题中等难度题查看答案及解析
-
(14分)下表为元素周期表的一部分,a、b、c……为部分元素。回答下列问题:
a
f
h
i
b
e
j
c
d
g
k
l
(1)请写出上述元素d3+的核外电子排布式 ;
(2)请写出j的单质与a、h形成的化合物发生反应的化学方程式 ;
(3)请比较b、e、j三种元素的电负性由大到小的顺序 (写元素符号);此三种元素的第一电离能由大到小的顺序 (写元素符号);
(4)g、e两种元素的最高价氧化物对应的水合物的化学性质相似,请写出e元素最高价氧化物对应的水合物与a、c、h三种元素形成的化合物反应的离子方程式 ;
(5)j、k、l三种元素之间能以原子个数比1∶1两两形成互化物,这些互化物的性质类似于这些元素单质的性质。请写出k、l的互化物的电子式 ,它是由 键(根据原子轨道的重叠程度填写)形成的 化合物(填“离子”或“共价”)。
高二化学填空题困难题查看答案及解析
-
物质结构与性质下表为元素周期表的一部分。请回答下列问题:
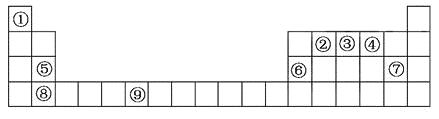
(1)上述元素中,属于s区的是_________(填元素符号)。
(2)写出元素⑨的基态原子的价电子排布图_______。
(3)元素的第一电离能:③______④(选填“大于”或“小于”)。
(4)元素③气态氢化物的VSEPR模型为____;该分子为___分子(选填“极性”或“非极性”)。向硫酸铜溶液中逐滴加入其水溶液,可观察到的现象为_____________。
(5)元素⑥的单质的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。
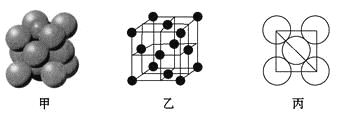
若已知⑥的原子半径为dcm,NA代表阿伏加德罗常数,元素⑥的相对原子质量为M,请回答:晶胞中⑥原子的配位数为____________,该晶体的密度为___________(用字母表示)。
高二化学综合题中等难度题查看答案及解析
-
下表为元素周期表的一部分,a、b、c…为部分元素.回答下列问题:
(1)请写出上述元素d3+的核外电子排布式______;a f y h i b e j c d d g l
(2)请写出e元素的原子电子轨道表示式______;
(3)ya3分子的电子式是______,其分子的空间构型是______,
(4)b、e两种元素中,金属性较强的是______;第一电离能大的是______.(填元素符号)
(5)h的i形成hi2分子杂化类型是______ fh32-的空间构型分别为______.高二化学解答题中等难度题查看答案及解析
-
下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
a
f
y
h
i
b
e
j
c
d
d
g
l
(1)请写出上述元素d3+的核外电子排布式________;
(2)请写出e元素的原子价电子轨道表示式________;
(3)ya3分子的电子式是________ ,其分子的空间构型是________ ,
(4)b、e两种元素中,金属性较强的是;第一电离能大的是_______.(填元素符号)
(5)h的i形成hi2分子杂化类型是________ fh3-的空间构型分别为_______________
高二化学填空题中等难度题查看答案及解析
-
下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
a
b
c
d
e
f
g
d
h
[
(1)请写出上述元素h的基态原子核外电子排布式________;
(2)比较e、g两种元素的气态氢化物的稳定性________(写化学式);
(3)b2a4分子的结构式是________ ,该分子中存在的σ键与π键的个数比为________;
(4)c、d两种元素中第一电离能较大的是________(写元素符号),其原因是________;
(5)已知f的氢氧化物与水电离出的OH—可形成配位键,则生成的含有配位键的离子的结构简式为________(标出配位键)。
高二化学填空题中等难度题查看答案及解析
-
(13分)下表为元素周期表的一部分,a、b、c…为部分元素。回答下列问题:
a
f
y[
h
i
b
e
j
c
d
d
g
l
(1)请写出上述元素g的核外电子排布式________;
(2)请比较b、e两种元素的第一电离能________(写元素符号),其原因是________
________
(3)试比较i、j两种元素的气态氢化物的稳定性________(写化学式)
(4)f2a4分子的结构式是________ ,该分子中存在的σ键与π键的个数比为________
高二化学填空题中等难度题查看答案及解析