如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是

A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的pH约为1
B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a
C.电池工作时,甲烧杯中由水电离出的c(H+)逐渐减小
D.乙池中的氧化产物为SO42-
高三化学选择题中等难度题
如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是

A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的pH约为1
B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a
C.电池工作时,甲烧杯中由水电离出的c(H+)逐渐减小
D.乙池中的氧化产物为SO42-
高三化学选择题中等难度题
如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是

A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的pH约为1
B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a
C.电池工作时,甲烧杯中由水电离出的c(H+)逐渐减小
D.乙池中的氧化产物为SO42-
高三化学选择题中等难度题查看答案及解析
如图所示,装置在常温下工作(溶液体积变化忽略不计)。闭合K,灯泡发光。下列叙述中不正确的是
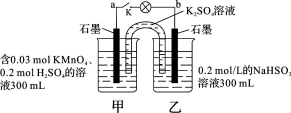
A.当电路中有1.204×1022个电子转移时,乙烧杯中溶液的pH约为1
B.电池工作时,盐桥中的K+移向甲烧杯,外电路的电子方向是从b到a
C.电池工作时,甲烧杯中由水电离出的c(H+)逐渐减小
D.乙池中的氧化产物为SO42-
高三化学选择题中等难度题查看答案及解析
常温下,取20mL某浓度的盐酸作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如图所示。下列叙述正确的是
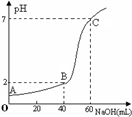
A. 所用盐酸的浓度是0.09mol·L-1,NaOH溶液浓度为0.03mol·L─1
B. 在B点,溶液中离子浓度关系为:c(Cl─)>c(Na+)>c(OH-)>c(H+)
C. A、B、C三点水的电离程度大小依次为:A>B>C
D. 滴定前,锥形瓶用待测液润洗,导致盐酸浓度偏低
高三化学选择题困难题查看答案及解析
常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定假设盐酸与NaOH溶液混合后体积变化忽略不计
,滴定过程中溶液的pH变化如图所示。下列叙述正确的是
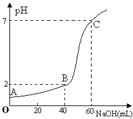
A.所用HCl的浓度是,NaOH溶液浓度为
B.在B点,溶液中离子浓度关系为:
C.A.三点水的电离程度大小依次为:
D.滴定前,锥形瓶用待测液润洗,导致HCl浓度偏低
高三化学单选题简单题查看答案及解析
常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定假设盐酸与NaOH溶液混合后体积变化忽略不计
,滴定过程中溶液的pH变化如图所示。下列叙述正确的是

A.所用HCl的浓度是,NaOH溶液浓度为
B.在B点,溶液中离子浓度关系为:
C.A.三点水的电离程度大小依次为:
D.滴定前,锥形瓶用待测液润洗,导致HCl浓度偏低
高三化学单选题简单题查看答案及解析
常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定假设盐酸与NaOH溶液混合后体积变化忽略不计
,滴定过程中溶液的pH变化如图所示。下列叙述正确的是
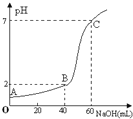
A.所用HCl的浓度是,NaOH溶液浓度为
B.在B点,溶液中离子浓度关系为:
C.A.三点水的电离程度大小依次为:
D.滴定前,锥形瓶用待测液润洗,导致HCl浓度偏低
高三化学单选题简单题查看答案及解析
常温下,取20mL某浓度的HCl作为待测液,用一定物质的量浓度的NaOH溶液进行滴定(假设盐酸与NaOH溶液混合后体积变化忽略不计),滴定过程中溶液的pH变化如右图所示。下列叙述正确的是
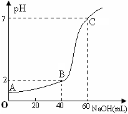
A.所用HCl的浓度是0.09mol·L─1,NaOH溶液浓度为0.03mol·L─1
B.在B点,溶液中离子浓度关系为:c(Cl─)>c(H+)>c(Na+)>c(OH─)
C.A、B、C三点由水的电离产生的c(H+)大小依次为:A>B>C
D.滴定前,锥形瓶用待测液润洗,导致HCl浓度偏低
高三化学选择题中等难度题查看答案及解析
常温下,向100 mL 0.01 mol·L-1HA溶液中逐滴加入0.02 mol·L-1MOH溶液,图中所示曲线表示混合溶液的pH变化情况(体积变化忽略不计)。下列叙述正确的是
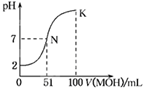
A.HA为弱酸,MOH为强碱
B.pH=7时,HA与MOH恰好完全反应
C.在N点,c(A-)=c(M+) + c(MOH)
D.在K点,c(M+)>c(A-)>c(OH-)>c(H+)
高三化学选择题中等难度题查看答案及解析
下图两个装置中,液体体积均为200 mL,开始工作前电解质溶液的浓度均为0.5 mol/L,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化,下列叙述正确的是
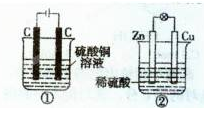
A.产生气体体积:①=②
B.溶液的pH变化:①减小,②增大
C.电极反应式:①中阳极为4 OH--4e-=2H2O+O2↑②中负极为2H++2e-=H2↑
D.①中阴极质量增加,②中正极质量减小
高三化学选择题中等难度题查看答案及解析
下图两个装置中,液体体积均为200 mL,开始工作前电解质溶液的浓度均为0.5 mol/L,工作一段时间后,测得有0.02 mol电子通过,若忽略溶液体积的变化,下列叙述正确的是
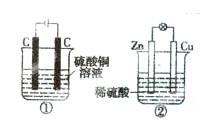
A.产生气体体积:①=②
B.溶液的pH变化:①减小,②增大
C.电极反应式:①中阳极为4 OH--4e-=2H2O+O2↑②中负极为2H++2e-=H2↑
D.①中阴极质量增加,②中正极质量减小
高三化学选择题简单题查看答案及解析