-
无水四氯化锡是无色易流动的液体。熔点-33℃,沸点114.1℃。遇潮湿空气,水解而生成锡酸和氯化氢。下图是实验室制备无水四氯化锡并对产品蒸馏,制得纯净无水氧化锡的实验设计(加热及夹持装置已略去)。

(1)装置A中反生反应的离子方程式_______________________。
(2)上述实验仪器口连接顺序为__________________________________。
(3)装置E中盛装试剂的名称为_________;上述实验正确的操作顺序为_____________。
①点燃装置A处酒精灯;②点燃装置B处酒精灯;③打开恒压漏斗活塞。
(4)装置G中仪器X的名称为___________。装置F的作用为_________________。
(5)将四氯化锡慢慢加水生成SnO2胶体和六氯合锡酸[H2[SnC16]],该反应的化学反应方程式为______________________。
(6)设计实验测定盐酸与MnO2反应的最低浓度,进行了如下操作:
I将装置A中液体加热至不再产生黄绿色气体为止,冷却过滤。
Ⅱ取上述滤液10mL稀释到400mL
III取稀释后溶液25.00mL加入指示剂进行滴定,滴定终点消耗0.2mol ·L-1的NaOH溶液19.25mL。
①上述条件下Mn2+开始沉淀的pH为5.2,则滴定时最好选用的指示剂为_____________。
②通过上述数据计算,盐酸与MnO2反应的最低浓度为__________(结果保留两位小数)。
-
二氯化锡可用于染料、香料、制镜、电镀等工业,是一种重要的化工原料。实验室制备二氯化锡可分三个过程完成,具体实验如下:
已知:①常温下四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃,易溶于水。
②二氯化锡:遇水强烈水解,在浓盐酸中溶解度大且有利于SnCl2·2H2O的生成。
I.四氯化锡的制备。所需装置如图所示:
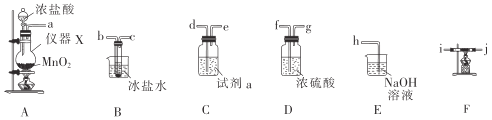
(1)仪器X的名称是___。
(2)试剂a是___,冰盐水的作用是__。
(3)按气流从左到右的顺序连接好装置:a___。
II.SnCl2·2H2O的制备
将装置B中得到的无色液体全部倒入锥形瓶中并加入适量浓盐酸,慢慢加入锡粉直至不能溶解,过滤后即得到SnCl2·2H2O。
(4)加入适量浓盐酸的作用是___。
(5)加入锡粉发生的反应为___。
III.SnCl2·2H2O的脱水,步骤如下:
a.将得到的SnCl2·2H2O置于干燥的50mL烧杯中,加入足量醋酸酐(CH3COOOCCH3)溶解。
b.将烧杯放入通风橱内,约5分钟搅拌一次,30分钟后在干燥的布氏漏斗上过滤。
c.用3~5mL乙醚淋洗产品,将产品转移至表面血,放入干燥器中干燥30分钟后,称重。
(6)SnCl2·2H2O脱水步骤a中加入醋酸酐后得到的有机物的结构简式是___。
(7)设计实验检测制得的SnCl2中是否有SnCl4:___。
-
锡为第IVA族具有可变价的金属元素,其单质沸点为2260℃。四氯化锡(SnCl4)是无色液体,熔点-33℃,沸点114℃,极易水解,在潮湿的空气中发烟。实验室中可用氯气与过量金属锡通过下图装置制备SnCl4 (夹持装置已略去)。
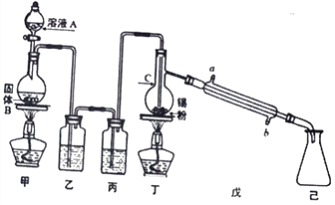
(1)仪器C的名称为___________,装置乙中的试剂是_____________。
(2)装置甲中发生反应的化学方程式为___________________________________。
(3)氯气与锡的反应类似与铁的反应,但该实验中对装置丁要持续加热,其原因是_____________。
(4)你认为该实验装置需要进行的改进是:__________________________________________。
(5)用下列方法和步骤测定所用金属锡样品的纯度(杂质不参加反应)
①将2.000g锡完全溶于过量稀盐酸中,并用所得溶液去还原过量的FeCl3稀溶液,最后得100.00mL 溶液。写出第二步反应的离子方程式:_____________________________。
②取①所得溶液amL用0.100 mol·L-1 的K2Cr2O7溶液滴定,发生如下反应:6FeCl2+ K2Cr2O7+ 14HCl=6FeCl3+2KCl+2CrCl3+7H2O。
K2Cr2O7溶液应注入到____式(填"酸或碱”) 滴定管中。到达滴定终点时用去bmL。则样品中锡的质量分数为_______%(用含a、b 的最简代数式表示)。
-
氯气与金属锡在加热时反应可以用来制备SnCl4 。已知:四氯化锡是无色液体,熔点-33 ℃,沸点114 ℃。SnCl4 极易水解,在潮湿的空气中发烟。实验室可以通过下图装置制备少量SnCl4 (夹持装置略)。
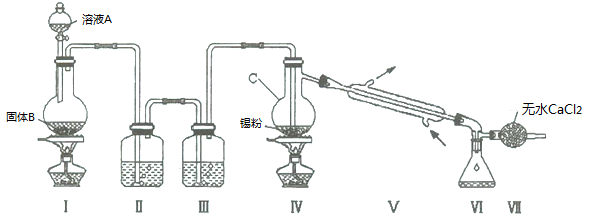
(1)仪器C的名称为 ;
(2)装置Ⅰ中发生反应的离子方程式为 ;
(3)装置Ⅱ中的最佳试剂为 ,装置Ⅶ的作用为 ;
(4)该装置存在的缺陷是: ;
(5)如果没有装置Ⅲ,在Ⅳ中除生成SnCl4 外,还会生成的含锡的化合物的化学式为 ;
(6)若Ⅳ中用去锡粉11.9 g,反应后,Ⅵ中锥形瓶里收集到24.8 g SnCl4 ,则SnCl4 的产率为 。
-
四氯化锡是无色液体,熔点-33℃,沸点114℃。氯气与金属锡在加热时反应可以用来制备SnCl4 , SnCl4 极易水解,在潮湿的空气中发烟。实验 室可以通过下图装置制备少量SnCl4 (夹持装置略)。
室可以通过下图装置制备少量SnCl4 (夹持装置略)。
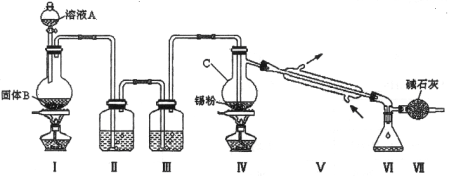
(1)仪器C的名称为: ;
(2)装置 Ⅰ中发生反应的离子方程式为:
Ⅰ中发生反应的离子方程式为:  ;
;
(3)装置Ⅱ中的最佳试剂为 ,装置Ⅶ的作用为 ;
(4)若装置连接顺序为Ⅰ—Ⅱ一Ⅳ一Ⅴ一Ⅵ一Ⅶ,在Ⅳ中除生成SnCl4 外,还会生成的含锡的化合物的化学式为 。
(5)Ⅳ中加热的作用之一是促进氯气与锡粉反应,加热的另一作用为 ;
(6)若Ⅳ中用去锡粉11.9 g,反应后,Ⅵ中锥形瓶里收集到23.8 g SnCl4 ,则SnCl4 的产率为 。
-
四氯化锡常用于染色的媒染剂等,工业上常用氯气与金属锡反应制备四氯化锡。已知SnCl4为无色液体,熔点-33℃,沸点114℃,极易水解,在潮湿的空气中发烟。实验室可用下列装置合成四氯化锡(夹持装置略)。
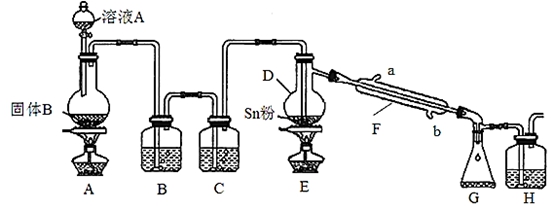
(1)装置D的名称为 ;
(2)冷凝水应从 (填“a”或“b”)口进入F中;
(3)装置A中固体B为黑色粉末,写出烧瓶中发生反应的化学反应方程式为 ;
(4)假设没有装置C,在D中除生成SnCl4外,可能得到的副产物为 ;
(5)装置E中加热的目的是 、 ;
(6)装置H中盛放足量的FeBr2溶液可吸收尾气中的氯气,其反应的离子反应方程式为 。
(7)该实验装置存在设计缺陷,你的改进措施为 。
(8)若装置A中标准状况下生成6.72L气体,假设不计气体损耗且Sn足量,反应完毕后在G 中锥形瓶里收集到37.20 g SnCl4,则SnCl4的产率为 (已知SnCl4相对分子质量为261)。
-
四氯化锡常用于染色的媒染剂等,工业上常用氯气与金属锡反应制备四氯化锡。已知SnCl4为无色液体,熔点-33℃,沸点114℃,极易水解,在潮湿的空气中发烟。实验室可用下列装置合成四氯化锡(夹持装置略)。
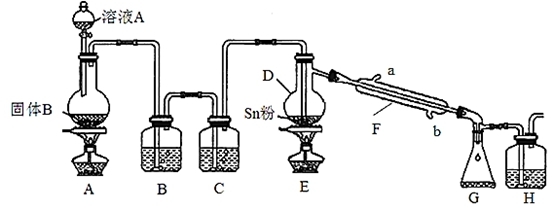
(1)装置D的名称为 ;
(2)冷凝水应从 (填“a”或“b”)口进入F中;
(3)装置A中固体B为黑色粉末,写出烧瓶中发生反应的化学反应方程式为 ;
(4)假设没有装置C,在D中除生成SnCl4外,可能得到的副产物为 ;
(5)装置E中加热的目的是 、 ;
(6)装置H中盛放足量的FeBr2溶液可吸收尾气中的氯气,其反应的离子反应方程式为 。
(7)该实验装置存在设计缺陷,你的改进措施为 。
(8)若装置A中标准状况下生成6.72L气体,假设不计气体损耗且Sn足量,反应完毕后在G 中锥形瓶里收集到37.20 g SnCl4,则SnCl4的产率为 (已知SnCl4相对分子质量为261) 。
-
四氯化锡可用作媒染剂、有机合成中氯化的催化剂等。实验室制备四氯化锡所需的有关装置和信息如下:
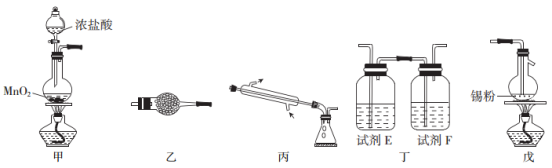
有关信息:①将金属锡熔融,通入干燥氯气进行反应,生成四氯化锡;②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃;③四氯化锡易水解。
回答下列问题:
(1)装置甲中反应容器的名称是____________;试剂E和F分别是___________、____________。
(2)装置甲中发生反应的化学方程式为_____________________;
装置戊中发生反应的化学方程式为______________________。
(3)上述各装置的连接顺序是甲→_________→___________→_________(填装置标号),实验开始时点燃的酒精灯是_________(填“甲”或“戊”)。
(4)装置乙的作用是______________________________。
(5)实验所得SnCl4中因溶解了Cl2而略显黄色,提纯SnCl4的方法是__________(填标号)。
a.用NaOH溶液洗涤 b.升华 c.重结晶 d.蒸馏 e.过滤 f.萃取
(6)四氯化锡暴露于空气中与空气中水分反应生成白烟,有强烈的刺激性,原因是___________(用化学方程式表示)。
-
四氯化锡用作媒染剂和有机合成的氯化催化剂,实验室制备四氯化锡的反应、装置示意图和有关信息如下:
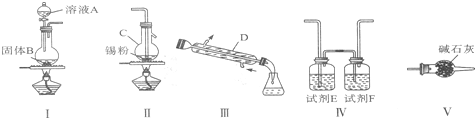
有关信息:
①将金属锡熔融,通入干燥氯气进行反应,生成四氯化锡。
②无水四氯化锡是无色易流动的液体,熔点-33℃,沸点114.1℃。
⑧暴露于空气中与空气中的水分反应生成白烟,有强烈的刺激性,遇水分解。
回答下列问题:
(1)仪器C的名称是 。
(2)制备无水四氯化锡各装置的连接顺序是( )→( )→( )→( )→( )(填装置序号)。
(3)装置V的作用是 。
(4)若无装置V存在,在装置Ⅲ中除生成SnCl4外,还存在的副产物化学式为 。
(5)若Ⅱ中用去锡粉5.95 g,反应后,Ⅲ中锥形瓶里收集到12.0 g SnCl4,则SnCl4的产率为 。
-
四氯化锡可用作媒染剂、有机合成中氯化的催化剂等。实验室制备四氯化锡所需的有关装置和信息如下:
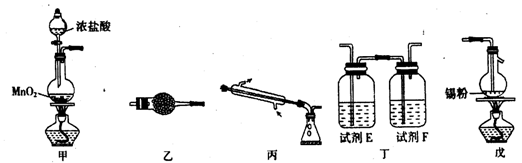
有关信息:①将金属锡熔融,通入干燥氯气进行反应,生成四氯化锡;
②无水四氯化锡是无色易流动的液体,熔点-33℃ ,沸篇114.1℃;
③四氯化锡易水解。
回答下列问题:
(1)装置甲中反应容器的名称是__________;试剂E 和F 分别是________、________。
(2)装置甲中发生反应的化学方程式为_______;装置戊中发生反应的化学方程式为______________。
(3)上述各装置的连接顽序是甲→______→______→______→______(填装置标号),实验开始时点燃的酒精灯是_________(填“甲”或“戊”)。
(4)装置乙的作用是___________。
(5)实验所得SnCl4中因溶解了Cl2而略显黄色,提纯SnCl4的方法是_________(填标号)
A.用Na0H溶液洗涤蒸馏 B.升华 c.重结晶 D.蒸馏 e.过滤 f.萃取
(6)四氯化锡暴露于空气中与空气中水分反应生成白雾,有强烈的刺激性气味,原因是:___________(用化学方程式表示)。









