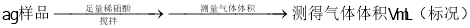-
硝酸银是一种无色晶体,常用于照相、制镜、印刷、医药等。其水溶液和固体常被保存在棕色试剂瓶中。硝酸银不稳定,受热分解生成固体、NO2 和 O2 。为了验证 AgNO3 受热分解的产物,某同学设计了以下实验,实验所用的装置如图(图中加热、夹持仪器等均略去):

实验步骤:
a.仪器连接后,放入AgNO3固体之前,关闭K,微热硬质玻璃管A;
b.称取 AgNO3 固体1.7g 置于A中,先通一段时间N2,再关闭K,用酒精灯加热硬质玻璃管A;
c.待样品完全分解,装置A冷却至室温,称量,测得剩余固体的质量为1.08 g。
请回答下列问题:
(1)使用酒精灯对AgNO3固体加热的操作方法是_________________。
(2)步骤a的操作目的是__________________。
(3)步骤b中先通一段时间的N2的目的是_____________________。
(4)装置C瓶中盛装的药品名称为_____________(合理即可),装置D中可观察到的实验现象为__________________。
(5)根据实验现象和称量结果,请写出该装置中AgNO3固体受热分解的化学方程式__________________。
(6)从实验安全角度考虑该装置存在缺陷,应如何改进?__________________。
-
硝酸银是一种无色晶体,常用于照相、制镜、印刷、医药等。其水溶液和固体常被保存在棕色试剂瓶中,硝酸银不稳定,受热分解生成固体、NO2和O2。为了研究AgNO3的受热分解产物的性质,某同学设计了以下实验:实验所用的装置如图(图中加热、夹持仪器等均略去):

实验步骤为:a.仪器连接后,放入AgNO3固体之前,关闭k,微热硬质玻璃管A。
b.称取AgNO3固体1.7g置于A中,先通入一段时间N2,再关闭k,用酒精灯加热硬质玻璃管A。
c.待样品完全分解,A装置冷却至室温、称量,测得剩余园体的质量为1.08g。……
请回答下列问题:
(1)使用酒精灯对AgNO3固体加热的操作方法是________________________。
(2)步骤a的操作目的是_________________________________________。
(3)步骤b中先通入一段时间N2的操作目的是_______________________________。
(4)装置C瓶中盛装的药品名称为___________,装置D中可观察到的实验现象为___________。
(5)设计实验证明AgNO3分解产物中气体的体积比________________________________。
(6)从实验安全角度考虑该实验装置有缺陷,应如何改进?_____________________。
-
硝酸银是一种无色晶体,易溶于水。用于照相乳剂、镀银、制镜、印刷、医药、染毛发等,也用于电子工业。硝酸银不稳定,易发生如下反应:
①2AgNO3(s)=2Ag(s)+ 2NO2(g)+O2(g) △H1>0
②2NO2(g)  N2O4(g) △H2<0
N2O4(g) △H2<0
(1)实验室配制硝酸银溶液的方法是:将一定量硝酸银固体溶于浓硝酸中,加水稀释至指定体积。“硝酸”的作用是___________________。
(2)2AgNO3(s) =2Ag(s)+N2O4(g)+O2(g) △H=______________ (用含△H1、△H2的式子表示)。
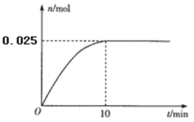
(3)温度T1时,在0.5L的恒容密闭容器中投入3.4 g AgNO3(s)并完全分解测得混合气体的总物质的量(n)与时间(t)的关系如图所示。

①下列情况能说明体系达到平衡状态的是_________(填字母)
a.固体质量不再改变 b.O2的浓度不再改变
c.NO2的体积分数不再改变 d.混合气体的密度不再改变
②若达到平衡时,混合气体的总压强p=0. 3MPa。反应开始到
10min内N2O4的平均反应速率为___________ MPa·min-1。在该温度下2NO2(g) N2O4(g)的平衡常数Kp=___________(MPa)-1(结果保留2位小数)。
N2O4(g)的平衡常数Kp=___________(MPa)-1(结果保留2位小数)。
[提示:用平衡时各组分分压替代浓度计算的平衡常数叫压强平衡常数(Kp),组分的分压(P1) =平衡时总压(p)×该组分的体积分数( )]
)]
③实验测得:υ正=υ(NO2)消耗=k正c2(NO2),υ逆=2υ(N2O4) 消耗=k逆c(N2O4),k正、k逆为速率常数只受温度影响。则化学平衡常数K与速率常数k正、k逆的数学关系是K=___________。若将容器的温度改变为T2时其k正=k逆,则T1______T2(填“>”、“<”或“=")
(4)NO与O2反应生成NO2的反应历程为:第一步NO+NO N2O2 (快速平衡)
N2O2 (快速平衡)
第二步N2O2+O2=2NO2 (慢反应),下列叙述正确的是___________(填标号)。
A. υ(第一步的正反应) <υ(第二步的反应) B.总反应快慢由第二步决定
C. 第二步的活化能比第一步的高 D.第二步中N2O2与O2的碰撞100%有效
-
硝酸银是一种无色晶体,易溶于水。用于照相乳剂、镀银、制镜、印刷、医药、染毛发等,也用于电子工业。硝酸银不稳定,易发生如下反应:
①2AgNO3(s)=2Ag(s)+ 2NO2(g)+O2(g) △H1>0
②2NO2(g)  N2O4(g) △H2<0
N2O4(g) △H2<0
(1)实验室配制硝酸银溶液的方法是:将一定量硝酸银固体溶于浓硝酸中,加水稀释至指定体积。“硝酸”的作用是___________________。
(2)2AgNO3(s) =2Ag(s)+N2O4(g)+O2(g) △H=______________ (用含△H1、△H2的式子表示)。
(3)温度T1时,在0.5L的恒容密闭容器中投入3.4 g AgNO3(s)并完全分解测得混合气体的总物质的量(n)与时间(t)的关系如图所示。
①下列情况能说明体系达到平衡状态的是_________(填字母)
a.固体质量不再改变 b.O2的浓度不再改变
c.NO2的体积分数不再改变 d.混合气体的密度不再改变
②若达到平衡时,混合气体的总压强p=0. 3MPa。反应开始到
10min内N2O4的平均反应速率为___________ MPa·min-1。在该温度下2NO2(g) N2O4(g)的平衡常数Kp=___________(MPa)-1(结果保留2位小数)。
N2O4(g)的平衡常数Kp=___________(MPa)-1(结果保留2位小数)。
[提示:用平衡时各组分分压替代浓度计算的平衡常数叫压强平衡常数(Kp),组分的分压(P1) =平衡时总压(p)×该组分的体积分数( )]
)]
③实验测得:υ正=υ(NO2)消耗=k正c2(NO2),υ逆=2υ(N2O4) 消耗=k逆c(N2O4),k正、k逆为速率常数只受温度影响。则化学平衡常数K与速率常数k正、k逆的数学关系是K=___________。若将容器的温度改变为T2时其k正=k逆,则T1______T2(填“>”、“<”或“=")
(4)NO与O2反应生成NO2的反应历程为:第一步NO+NO N2O2 (快速平衡)
N2O2 (快速平衡)
第二步N2O2+O2=2NO2 (慢反应),下列叙述正确的是___________(填标号)。
A. υ(第一步的正反应) <υ(第二步的反应) B.总反应快慢由第二步决定
C. 第二步的活化能比第一步的高 D.第二步中N2O2与O2的碰撞100%有效
-
 (三草酸合铁酸钾晶体)为翠绿色晶体,可用于摄影和蓝色印刷,110℃失去结晶水,230℃分解。某化学研究小组对
(三草酸合铁酸钾晶体)为翠绿色晶体,可用于摄影和蓝色印刷,110℃失去结晶水,230℃分解。某化学研究小组对 受热分解生成的气体产物和固体产物进行探究。
受热分解生成的气体产物和固体产物进行探究。
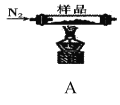
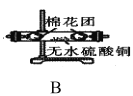
实验I:探究实验所得的气体产物,按下图装置进行实验(夹持仪器已略去,部分装置可重复使用)。



(1)实验室常用饱和 和饱和
和饱和 的混合液制
的混合液制 ,反应的化学方程式为_____________。
,反应的化学方程式为_____________。
(2)装置的连接顺序为:A→__→__→__→__→__→F(填各装置的字母代号)。
(3)检查装置气密性后,先通一段时间 ,其目的是________,实验结束时熄灭A、C两处的酒精灯,继续通
,其目的是________,实验结束时熄灭A、C两处的酒精灯,继续通 至常温,其目的是__________。
至常温,其目的是__________。
(4)实验过程中观察到F中的溶液变浑浊,C中有红色固体生成,则气体产物____(填化学式)。
(实验二)分解产物中固体成分的探究
(5)定性实验:经检验,固体成分含有 。
。
定量实验:将固体产物加水溶解、过滤洗涤、干燥,得到含铁样品。完成上述实验操作,需要用到下列仪器中的__________(填仪器编号)。
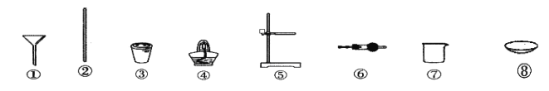
设计下列三种实验方案分别对该含铁样品进行含量的测定
(甲方案)
(乙方案)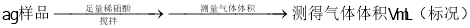
(丙方案)

你认为以上方案中可以确定样品组成的有_____________方案。
(6)经测定产物中 ,写出
,写出 分解的化学方程式_________。
分解的化学方程式_________。
-
AgNO3是中学化学常用试剂,某兴趣小组设计如下实验探究其性质。
I. AgNO3的热稳定性
AgNO3受热易分解,用下图装置加热AgNO3固体,试管内有红棕色气体生成,一段时间后,在末端导管口可收集到无色气体a。
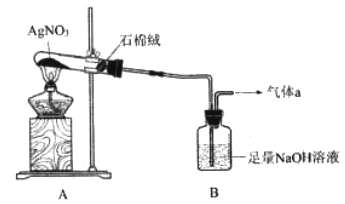
(1)实验室检验气体a的方法为_______________________________________。
(2)已知B中只生成一一种盐,据此判断AgNO3受热分解的化学方程式为______________。
(3)从安全角度考虑,上述实验装置存在一处明显缺陷,改进措施为______________________。II. AgNO3与盐溶液的反应
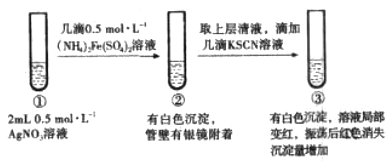
(4)甲同学认为试管②中产生银镜是Fe2+所致,其离子方程式为_____________________;
乙同学认为要判断该观点正确,需增加如下实验,取2 mL0.5mol/L AgNO3溶液于试营中,向其中满加几滴____________,若只产生白色远淀,证明甲同学观点正确。
(5)已知:AgSCN为白色沉淀。试管③中红色褪去的原因为__________________________(请从平衡移动的角度解释)。
(6)设计实验证明Ksp(AgI)sp(AgSCN)。
限选试剂:0.1 mol/L AgNO3溶液、0.1mol/LKI溶液、0.1mol/LKSCN 溶液___________________________________________________________。
-
化合物PH4I是一种白色晶体,受热不稳定,易分解产生PH3。PH3是无色剧毒气体, 广泛用于半导体器件和集成电路生产的外延、离子注入和掺杂。
(1)在2L真空密闭容器中加入一定量PH4I固体,T1℃ 时发生如下反应: PH4I(s) ⇌ PH3(g) + HI(g)
①下列可以作为反应达到平衡的判据是_____。
A.容器内气体的压强不变
B.容器内 HI 的气体体积分数不变
C.容器内 PH4I 质量不变
D.容器内气体的密度不变
E.容器内气体的平均相对分子质量不变
②t1时刻反应达到平衡后,在t2时刻维持温度不变瞬间缩小容器体积至1L,t3时刻反应重新达到 平衡。在下图中画出t2~t4 时段的υ正、υ逆随时间变化图______。
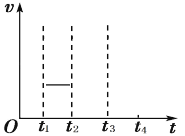
(2)PH4I固体分解产生的PH3和HI均不稳定,在一定温度下也开始分解。在2L真空密闭容器中加 入一定量PH4I固体,已知在T2℃ 时存在如下反应:
Ⅰ PH4I(s) ⇌ PH3(g) + HI(g) ΔH1
Ⅱ 4 PH3(g)⇌ P4(g) + 6 H2(g) ΔH2
Ⅲ 2 HI(g)⇌ H2 (g) + I2(g) ΔH3
①已知:298K,101kPa,H-P键、P-P键、H-H键的键能分别为322 kJ·mol-1、200 kJ·mol-1、436 kJ·mol-1试计算ΔH2 =______________。
②各反应均达平衡时,测得体系中 n(PH3)=a mol ,n(P4)=b mol ,n(H2)=c mol ,则 T2℃时 反应I的平衡常数K值为___________________。(用a、b、c表示)
③维持温度不变,缩小体积增大压强,达到新的平衡后,发现其它各成分的物质的量均发生变化,而n(I2)基本不变,试解释可能原因_____。
-
草酸铵[(NH4)2C2O4] 为无色柱状晶体,不稳定 ,受热易分解,可用于测定 Ca2+、Mg2+的含量。
I.某同学利用如图所示实验装置检验草酸铵的分解产物。
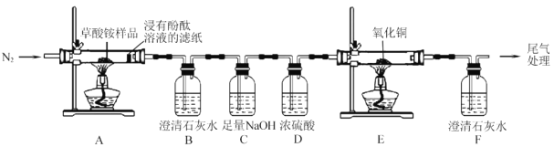
(1)实验过程中,观察到浸有酚酞溶液的滤纸变红,装置 B 中澄清石灰水变浑浊,说明分解产物中含有__________________(填化学式);若观察到__________________,说明分解产物中含有 CO。草酸铵分解的化学方程式为______________________。
(2)反应开始前 ,通入氮气的目的是________________________。
(3)装置 C 的作用是_______________________。
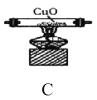
(4)还有一种分解产物在一定条件下也能还原CuO , 该反应的化学方程式为__________。
II.该同学利用草酸铵测定血液中钙元素的含量 。
(5)取 20.00 mL 血液样品 ,定容至 l00m L, 分别取三份体积均为25.00 mL 稀释后的血液样品,加入草酸铵,生成草酸钙沉淀,过滤,将该沉淀溶于过量稀硫酸中,然后用 0.0l00mol/L KMnO4 溶液进行滴定。滴定至终点时的实验现象为___________。三次滴定实验消耗 KMnO4 溶液的体积分别为0.43mL , 0.41 m L , 0.52mL, 则该血液样品中钙元素的含量为________m mol/L。
-
草酸铵[(NH4)2C2O4] 为无色柱状晶体,不稳定 ,受热易分解,可用于测定 Ca2+、Mg2+的含量。
I.某同学利用如图所示实验装置检验草酸铵的分解产物。
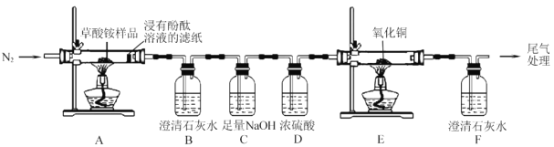
(1)实验过程中,观察到浸有酚酞溶液的滤纸变红,装置 B 中澄清石灰水变浑浊,说明分解产物中含有__________________(填化学式);若观察到__________________,说明分解产物中含有 CO。草酸铵分解的化学方程式为______________________。
(2)反应开始前 ,通入氮气的目的是________________________。
(3)装置 C 的作用是_______________________。
(4)还有一种分解产物在一定条件下也能还原CuO , 该反应的化学方程式为__________。
II.该同学利用草酸铵测定血液中钙元素的含量 。
(5)取 20.00 mL 血液样品 ,定容至 l00m L, 分别取三份体积均为25.00 mL 稀释后的血液样品,加入草酸铵,生成草酸钙沉淀,过滤,将该沉淀溶于过量稀硫酸中,然后用 0.0l00mol/L KMnO4 溶液进行滴定。滴定至终点时的实验现象为___________。三次滴定实验消耗 KMnO4 溶液的体积分别为0.43mL , 0.41 m L , 0.52mL, 则该血液样品中钙元素的含量为________m mol/L。
-
草酸铵[(NH4)2C2O4]为无色柱状晶体,不稳定,受热易分解,可用于测定Ca2+、Mg2+的含量。
I.某同学利用如图所示实验装置检验草酸铵的分解产物。
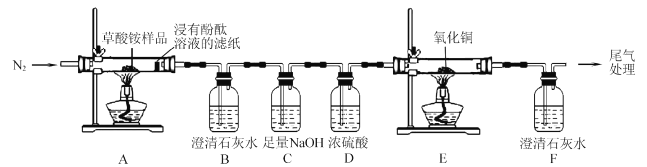
(l)实验过程中,观察到浸有酚酞溶液的滤纸变红,装置B中澄清石灰水变浑浊,说明分解产物中含有____(填化学式);若观察到____, 说明分解产物中含有CO2草酸铵分解的化学方程式为____。
(2)反应开始前,通人氮气的目的是____。
(3)装置C的作用是 ____。
(4)还有一种分解产物在一定条件下也能还原CuO,该反应的化学方程式为 _____。
Ⅱ.该同学利用草酸铵测定血液中钙元素的含量。
(5)取20. 00mL血液样品,定容至l00mL,分别取三份体积均为25. 00mL稀释后的血液样品,加入草酸铵,生成草酸钙沉淀,过滤,将该沉淀溶于过量稀硫酸中,然后用0. 0l00mol/LKMnO4溶液进行滴定。滴定至终点时的实验现象为____。三次滴定实验消耗KMnO4溶液的体积分别为0.43mL,0.4lmL,0.52mL,则该血液样品中钙元素的含量为__________ mmol/L。