-
R、Q、X、Y、Z是原子序数依次增大的五种短周期主族元素,R与Q形成的气态化合物的水化物显碱性,X、Y、Z三种元素族序数之和为10,Y单质能与强碱溶液反应,Z元素原子最外层电子数是电子层数的两倍。
(1)Z在周期表中的位置_______________;X、Y、Z三种元素形成的简单离子半径由大到小的顺序是________________________。(用离子符号回答)
(2)X和R两种元素按原子个数比1:1组成的化合物的电子式为____________。
(3)写出Y、Z两种元素最高价氧化物对应的水化物相反应的离子方程式:_____________。
(4)水的沸点远高于Z元素的氢化物的沸点,原因是_________________。
(5)Q4是一种Q元素的新单质,可用作推进剂或炸药,推算其分子中含有_____对共用电子。
(6)由R、Q两元素组成的一种液态化合物W常用作还原剂,W分子中含有18个电子,W分子的结构式为_____________________。W与氢氧化铜悬浊液反应生成氧化亚铜,同时产生一种稳定的气态单质,该反应的化学方程式为_____________________。
高一化学综合题中等难度题查看答案及解析
-
W、X、Y、Z、M、G五种短周期元素,原子序数依次增大。W,Z同主族,可形成离子化合物ZW;Y , M同主族,可形成MY2, MY3两种分子;X的气态氢化物水溶液呈碱性。
请回答下列问题:
(1)Y在元素周期表中的位置为 ;
(2)上述五种元素的最高价氧化物对应的水化物酸性最强的是 (写化学式)
(3) W、Y、Z、G形成的简单离子的半径大小顺序是 (用化学符号表示)
(4)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有 (任写两个)
(5)Y与M的氢化物中,热稳定性差的是 (填化学式),沸点高的是 (填化学式)
(6)ZW的电子式为 ,W2Y2的电子式为 ,用电子式表示Z2M的形成过程: 。
(7)MY2和G2均能使品红溶液褪色,常温常压下若将相同体积的MY2和G2气体同时通入品红溶液,品红溶液 (填“褪色”或“不褪色”),请用相关离子方程式解释原因 。
(8)已知
化合物
MgO
Al2O3
MgCl2
AlCl3
类型
离子化合物
离子化合物
离子化合物
共价化合物
熔点/℃
2800
2050
714
191
工业制镁时,电解MgCl2而不电解MgO的原因是是 ;制铝时,电解Al2O3而不电解AlCl3的原因是 。
(9)最近意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的N4分子。N4分子结构如下图所示,已知断裂1 mol N—N吸收167 kJ热量,生成1 mol N≡N入出942kJ。根据以上信息和数据,下列说法正确的是 。
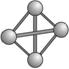
A.N4属于一种新型化合物 B.N4晶体熔点高,硬度大
C.相同质量的N4的能量高于N2 D.1molN4转变为N2将吸收882kJ的能量.
高一化学填空题困难题查看答案及解析
-
.(19分)W、X、Y、Z、M、G六种主族元素分属三个短周期,且原子序数依次增大。Y是地壳中含量最多的元素;M与Y同主族;G与Z形成的化合物是厨房常用的的调味品;X的简单气态氢化物水溶液呈碱性。请回答下列问题:
(1)M在元素周期表中的位置为_________,X的简单气态氢化物的电子式为_____________,W、Y、Z、M、G形成的简单离子的半径大小顺序是___________________(用相应的离子符号表示)。
(2)Y与M的氢化物中,热稳定性更好的是______(填化学式),原因是_______________
(3)由 W、Y、Z、M组成的两种盐(均含有以上四种元素)的溶液反应可产生MY2气体,写出其反应的离子方程式________________________
(4)如图,A、B两极均为惰性电极,a是Z与G形成的饱和溶液,实验开始 时,同时在两边各滴入几滴酚酞试液,则
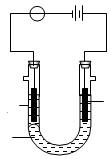
①电解池中A极上的电极反应式为 。在A极附近观察到的现象是 。
②B电极上的电极反应式为 ,检验该电极反应产物的方法是______________________
(5)最近意大利罗马大学的Funvio Cacace等人获得了极具理论研究意义的X4分子。X4分子结构如下图所示,已知断裂lmolX-X吸收167kJ热量,生成1mo1X2放出942kJ热量。根据以上信息和数据,下列说法正确的是____________。
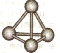
A.X4沸点比P4(白磷)高,属于原子晶体
B.lmol X4气体转变为X2放出882kJ热量
C.X4与X2互为同素异形体
(6)发射“神六”时用X2W4作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。已知生成1mol水蒸气时放热284kJ,写出X2W4 (g)和NO2(g)反应的热化学方程式__________________,已知H2O(l)==H2O(g) ΔH =+44kJ/mol,则16g X2W4 (g)与NO2反应生成液态水时放出的热量是________kJ。
同时,X2W4可作为新型燃料电池的燃料,在氧气中燃烧生成氮气和水,请利用X2W4、氧气与KOH溶液组成碱性燃料电池,写出该电池负极的电极反应式_______________,指出电解质溶液中OH-离子向________极移动。
高一化学填空题困难题查看答案及解析
-
W、X、Y、Z、M、G六种元素分属三个短周期,且原子序数依次增大。W、Z同主族,可形成离子化合物ZW;Y、M同主族,可形成MY2、MY3两种分子;X的气态氢化物水溶液呈碱性。请回答下列问题:
(1)Y在元素周期表中的位置为_________,上述元素的最高价氧化物对应的水化物酸性最强的是_____(写化学式),W、Y、Z、M形成的简单离子的半径大小顺序是___________________(用化学符号表示),G的离子结构示意图:_______________。
(2) Y与M的氢化物中,热稳定性更好的是____________(填化学式),原因是____________________________________________________________。
(3)Z2Y2的电子式为__________,ZW与水反应放出气体的化学方程式为_______________________________________________________________________。
(4)X2W4可作为新型燃料电池的燃料,在氧气中燃烧生成氮气和水,请利用X2W4、氧气与KOH溶液组成碱性燃料电池,写出该电池负极的电极反应式________________________,指出电解质溶液中OH-离子向________极移动。
高一化学填空题中等难度题查看答案及解析
-
W、X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。W、Z同主族,可形成离子化合物ZW;Y、M同主族,可形成MY2、MY3两种分子;X的气态氢化物水溶液呈碱性
请回答下列问题:
(1)Y在元素周期表中的位置为_________,上述元素的最高价氧化物对应的水化物酸性最强的是_____(写化学式),W、Y、Z、M形成的简单离子的半径大小顺序是___________________(用化学符号表示)。
(2) Y、G的单质或两元素之间形成的化合物可作水消毒剂的有_______(写单质的化学式)、_________(写出化合物的化学式)。
(3) Y与M的氢化物中,热稳定性更好的是____________(填化学式),原因是_____________________
(4) ZW的电子式为__________,ZW与水反应放出气体的化学方程式为__________________________。
(5)最近意大利罗马大学的Funvio Cacace等人获得了极具理论研究意义的X4分子。X4分子结构如下图所示,已知断裂lmolX-X吸收167kJ热量,生成1mo1X2放出942kJ热量。根据以上信息和数据,下列说法正确的是____________。
A.X4沸点比P4(白磷)低,属于原子晶体
B.lmol X4气体转变为X2吸收882kJ热量
C.X4与X2互为同素异形体
(6)发射“神六”时用X2W4作为火箭发动机的燃料,NO2为氧化剂,反应生成N2和水蒸气。已知声称1mol水蒸气时放热283.9KJ,写出X2W4 (g)和NO2(g)反应的热化学方程式______________________________________
同时,X2W4可作为新型燃料电池的燃料,在氧气中燃烧生成氮气和水,请利用X2W4、氧气与KOH溶液组成碱性燃料电池,写出该电池负极的电极反应式________________________,指出电解质溶液中OH-离子向________极移动。
高一化学填空题中等难度题查看答案及解析
-
已知:J、L、M、R、T是原子序数依次增大的短周期主族元素;J元素最低负化合价的绝对值与其原子最外层电子数相等;L的最简单气态氢化物甲的水溶液显碱性;M是地壳中含量最多的金属元素;R形成简单的阴离子R2-与Ar的电子层结构相同.则
(1)M的离子电子式为______;
(2)元素T在周期表中的位置是______;
(3)用电子式表式JR2的形成过程______;
(4)M和T形成的化合物(MT3)在潮湿的空气中冒白色烟雾,反应的化学方程式为:______.(提示:此反应为非氧化还原反应).
(5)在微电子工业中,甲的水溶液可作刻蚀剂H2O2 的清除剂,所发生反应的产物不污染环境,其化学方程式为______.高一化学解答题中等难度题查看答案及解析
-
A、B、C、D为原子序数依次增大的短周期元素,A元素气态氢化物的水溶液呈碱性,B为最活泼的非金属元素,C元素原子的电子层数是最外层电子数的3倍,D元素最高化合价为+6价。
(1)A元素气态氢化物的电子式为______;B在元素周期表中的位置为________。
(2)DBn做制冷剂替代氟利昂,对臭氧层完全没有破坏作用,是一种很有发展潜力的制冷剂。该物质的摩尔质量为146 g·mol-1,则该物质的化学式为_____。已知DBn在温度高于45℃时为气态,DBn属于____晶体。该物质被称为人造惰性气体,目前广泛应用于电器工业,在空气中不能燃烧,请从氧化还原角度分析不能燃烧的理由_________。
(3)C与氢元素组成1∶1的化合物,与水发生剧烈反应生成碱和一种气体,写出该反应的化学反应方程式____________,生成1mol气体转移的电子的数目为______个。
(4)A和C两元素可形成离子化合物甲。取13.0g化合物甲,加热使其完全分解,生成A的单质和C的单质,生成的A单质气体折合成标准状况下的体积为6.72L。化合物甲分解的化学方程式为______________________________。
(5)D元素的+4价含氧酸钠盐在空气中容易变质,设计实验方案证明该盐已经变质____。
高一化学综合题中等难度题查看答案及解析
-
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,乙位于第ⅤA族,甲和丙同主族,丁的最外层电子数和电子层数相等,则下列说法正确的是( )
A. 原子半径:甲>丙
B. 单质的还原性:丁>丙
C. 乙的氢化物是同族中氢化物还原性最强的
D. 乙、丙、丁的最高价氧化物对应的水化物能相互反应
高一化学单选题中等难度题查看答案及解析
-
短周期元素甲乙丙丁的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁的最外层电子数和电子层数相等,则( )
A. 原子半径:丁>丙>乙>甲
B. 单质的还原性:丁>丙>甲
C. 甲、乙、丙的氧化物均为共价化合物
D. 乙、丙、丁的最高价氧化物对应的水化物能相互反应
高一化学单选题中等难度题查看答案及解析
-
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态氢化物的水溶液呈碱性,乙位于第VA族,甲与丙同主族,丁原子最外层电子数与电子层数相等,则
A.原子半径:乙>丙>丁
B.单质的还原性:丁>丙>甲
C.甲、乙、丙的氧化物均为共价化合物
D.乙、丙、丁的最高价氧化物对应的水化物能相互反应
高一化学选择题简单题查看答案及解析