-
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X是元素周期表中原子半径最小的元素,X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。 请回答下列问题:
(1)Y在元素周期表中的位置为 ,ZX的电子式为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),非金属气态氢化物还原性最强的是 (写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作消毒剂的有 、 (写出其中两种物质的化学式)。
(4)X2M的标准燃烧热ΔH=-a kJ·mol-1 ,写出表示X2M标准燃烧热的热化学方程式: 。
-
X、Y、Z、M、G五种元素分属三个短周期, 且原子序数依次增大。X、Z同主族, 可形成离子化合物ZX; Y、M同主族, 可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式), 非金属气态氢化物还原性最强的是 (写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有 、 (写出其中两种物质的化学式,一种为单质,另一种为化合物)。
(4)ZX的电子式为 。
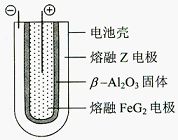
(5)熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下图),反应原理为:
2Z+ FeG2 Fe+ 2ZG
Fe+ 2ZG
放电时, 电池的正极反应式为 ,充电时, (写物质名称)电极接电源的负极。
-
有A、B、C、D、E、F六种短周期的主族元素、原子序数依次增大,其中A、D元素的原子最外电子层均只有一个电子,且A和D可形成离子化合物;C、F同主族,B元素位于元素周期表中第二周期,且原子最外层电子数占核外电子总数的3/4,F元素原子最外电子层比同周期的E元素原子的最外电子层多4个电子,请回答:
(1)写出A、D两种元素组成的化合物的电子式________;
(2)写出B、D、E三种元素组成的常见化合物的名称________;
(3)工业生产E的方法是________;
(4)D、E、F三元素最高价氧化物对应的水化物相互之间发生反应的离子方程式为:
________、
________、
________。
-
A、B、C、D、E、F六种短周期主族元素的原子序数依次增大,且知:
①A与B能形成多种气态化合物,B与D能形成两种常见气态化合物,D与E能形成两种离子化合物;
②B、C、D是同一周期相邻的三种元素,且有C和E的原子序数之和等于A和F的原子序数之和;
③E元素的原子半径大于F元素的原子半径.
请回答:
(1)E元素在元素周期表的位置是______,E与D按原子个数为1:1形成的化合物的电子式是______,所含的化学键有______.
(2)B和D形成的两种气态化合物中含有三个原子的化合物的结构式是______,将其通入足量NaAlO2溶液,现象是______,离子方程式为______.
(3)由A、C、F三种元素能组成一种离子化合物,检验其阳离子的方法是(用离子方程式表示)______ NH3↑+H2O
-
X、Y、Z、M、G五种主族元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物 ZX;Y、M同主族,可形成MY2、MY3两种分子。
请回答下列问题:
(1)Y在元素周期表中的位置为 ;
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),非金属气态氢化物还原性最强的是 (写化学式);
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有 、
(写出其中两种物质的化学式);
(4)ZX与水反应放出气体的化学方程式为 ;
(5)探究同主族元素性质的一些共同规律,是学习化学的重要方法之一。元素 E位于第四周期,与元素 Y同主族。在下表中列出对 H2EO3各种不同化学性质的推测,举例并写出相应的化学方程式(化学方程式中 E用元素符号表示)
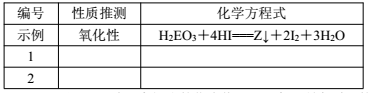
(6)由碳元素(C)、Y和 M三种元素组成的化合物 CYM中,所有原子的最外层满足 8电子结构。写出该化合物的电子式(电子式中 Y、M用元素符号表示)______________________。
-
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X的单质是一种理想能源,X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为__________。
(2)上述元素中,非金属气态氢化物还原性最强的是_________(写化学式);Y和Z形成的含有共价键的化合物的电子式为_________。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有_________。(写出其中两种物质的化学式)
(4)ZX与水剧烈反应产生X的单质,其化学方程式为_________。
-
(6分)X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),非金属气态氢化物还原性最强的是 (写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有______________(写出其中两种物质的化学式)。
(4)ZX的电子式为 。
-
X、Y、Z、M、G五种元素分属三个短周期;且原子序数依次增大。X、Z同主族;可形成离子化合物ZX;Y、M同主族;可形成MY2、MY3两种分子。
请回答下列问题:
(1)Y在元素周期表中的位置为___。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是___(写化学式);非金属气态氢化物还原性最强的是___(写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有___(写出其中两种物质的化学式)。
(4)X2M的燃烧热ΔH=-a kJ·mol-1;写出X2M燃烧反应的热化学方程式:_____。
(5)ZX的电子式为________;ZX与水反应放出气体的化学方程式为_______。
-
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主
族,可形成离子化合物ZX,Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),
非金属气态氢化物还原性最强的是 (写化学式)。
(3)X2M的燃烧热△H=-a kJ·mol-1,写出X2M燃烧反应的热化学方程式: 。
(4)ZX的电子式为 ;ZX与水反应放出气体的化学方程式为 。
-
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主
族,可形成离子化合物ZX,Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),
非金属气态氢化物还原性最强的是 (写化学式)。
(3)X2M的燃烧热△H=-a kJ·mol-1,写出X2M燃烧反应的热化学方程式: 。
(4)ZX的电子式为 ;ZX与水反应放出气体的化学方程式为 。