-
A、B、C、D、E、F、G是前四周期(除稀有气体)原子序数依次增大的七种元素,A的原子核外电子只有一种运动状态;B、C的价电子层中未成对电子数都是2;B、C、D同周期;E核外的s、p能级的电子总数相筹;F与E同周期且第一电离能比E小;G的+1价离子(G+)的各层电子全充满。回答下列问题:(相关问题用元素符号表示)
(1)写出E的基态原子的电子排布式________________________。
(2)B与C可形成化合物BC和BC2,BC2属于__________(填“极性”、“非极性”)分子,1 mol BC含有π键为____________________mol。
(3)由元素A、C、G组成的离子[G(A2C)4]2+在水溶液中显天蓝色,不考虑空间结构,[G(A2C)4]2+的结构可用示意图表示为__________(配位键用→标出)。
(4)测定A、D形成的化合物的相对分子质量时,实验测定值一般高于理论值的原因是_______。
(5)由元素A、B、F组成的原子个数比9 : 3 : 1的一种物质,分子中含三个相同的原子团,其结构简式为________________,分子中F原子的杂化方式为__________,该物质遇水爆炸,生成白色沉淀和无色气体,反应的化学方程式为____________________。
高二化学填空题困难题查看答案及解析
-
周期表前四周期的元素A、B、C、D、E、F,原子序数依次增大,A是周期表中原子半径最小的元素,B的基态原子中只有1个未成对电子,C基态原子中有7种不同运动状态的电子,D的最外层电子数是其所处周期数的3倍,E与D同主族,F的一价阳离子最外层有18个电子。回答下列问题:
(1)F在周期表中的位置是_____________,它的基态原子的电子排布式为_____________
(2)A元素与其他元素形成的含氧酸中,酸根呈三角锥结构的酸是_________,该酸的中心原子的杂化方式为_________
(3)CA3极易溶于水,试从下图中判断CA3溶于水后形成CA3·H2O的合理结构为_____(填字母代号),推理依据是___________
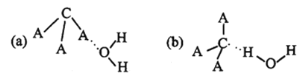
(4)元素B可形成H3BO3,已知H3BO3的电离方程式为H3BO3+2 H2O
[B(OH)4]一+H3O+
①基态B、D原子的第一电离能由小到大的顺序为__________(用元素符号表示)
②[B(OH)4]一中B原子的杂化类型为_______________
③写出一种与H3O+互为等电子体的分子的化学式:___________
④H3BO3晶体在热水中的溶解度大于冷水中的溶解度的原因为__________________
高二化学综合题中等难度题查看答案及解析
-
前四周期原子序数依次增大的元素A、B、C、D、E中,A的基态原子核外3个能级上有电子,且每个能级上的电子数相等,B原子核外电子有7种不同的运动状态,C元素原子核外的M层中只有2对成对电子,D+与C2-的电子数相等,E元素位于元素周期表的ds区,且基态原子价电层电子均已成对。
回答下列问题:
(1)E2+的外围电子排布图为________________。
(2)五种元素中电负性最小的是________(填元素符号),CAB-离子中,A原子的杂化方式是________。
(3)AB-、D+和E2+三种离子组成的化学物质D2E(AB)4,该化合物中存在一个复杂离子,该离子的化学式为________,配位体是________。
(4)C和E两种元素组成的一种化合物的晶胞如图所示。
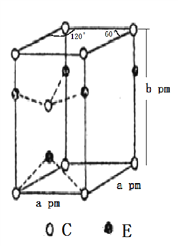
①该化合物的化学式为________,E的配位数为________,C采取________(填“简单立方”、“体心立方”、“六方最密”或“面心立方最密”)堆积;
②列式表示该晶体的密度:________g·cm-3。(NA表示阿伏加德罗常数的值)
高二化学综合题中等难度题查看答案及解析
-
短周期的7种元素A、B、C、D、E、F、G的原子序数依次增大,其中A原子中的电子只有1种运动状态,且与B同主族,C的基态原子2p能级上只有1个电子,F与A可形成两种常温下的液态化合物;F与G同主族。根据上述描述,请回答下列问题:
(1)上述7种元素中电负性最小的元素与A元素形成的化合物的电子式为______(用具体元素符号表示电子式),基态原子的一电离能最大的元素是_____(填元素符号)。
(2)1molD3A6链状分子中含有的σ键数为________。
(3)已知A2F2的分子结构如图所示:
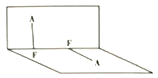
①用电离方程式表示呈弱酸性的原因:______________。
②A2F2的沸点比A2F高的原因:_______________。
高二化学综合题中等难度题查看答案及解析
-
X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子;X、Z中未成对电子数均为2; U的氧化物是第三周期元素形成的常见两性氧化物;W的内层电子全充满,最外层只有1个电子。请回答下列问题:
(1)X、Y、Z的电负性从大到小的顺序是_______ (用元素符号表示,下同)。三种元素的第一电离能由大到小的顺序为__________。
(2)写出Y的价电子排布式____,W同周期的元素中,与W原子最外层电子数相等的元素还有________。
(3)根据等电子体原理,可知化合物XZ的结构式是________, YZ2-的VSEPR模型是________。
(4)X、Y、Z的简单氢化物的键角从大到小的顺序是________ (用化学式表示),原因是_____________。
(5)Y的氢化物易液化的原因是___________。
(6)XZ32-的立体构型是________,其中X原子的杂化轨道类型是________,互为等电子体的离子________。
(7)用氢键表示式写出Z的氢化物中存在的氢键________。
高二化学推断题中等难度题查看答案及解析
-
原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期,其中A原子核只有一个质子;B原子核外电子有6种不同的运动状态,B与C可形成正四面体型分子,D原子外围电子排布为3d104s1。
请回答下列问题:
(1)这四种元素中电负性最大的是________(填元素符号)、第一电离能最小的是________(填元素符号) ;
(2)C所在的主族元素气态氢化物中,沸点最低的是________(填化学式);
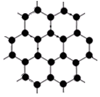
(3)B元素可形成多种单质,其中“只有一层原子厚”的物质,被公认为目前世界上已知的最薄、最坚硬、传导电子速度最快的新型材料,该材料晶体结构如图所示,其原子的杂化类型为________;
(4)D的醋酸盐晶体局部结构如图,该晶体中含有的化学键是________(填选项序号);
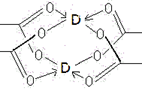
①极性键 ②非极性键 ③配位键 ④金属键
(5)某学生所做的有关D元素的实验流程如下图:

已知D的硫化物为黑色难溶性物质,请书写第⑤反应的离子方程式:________。
高二化学填空题中等难度题查看答案及解析
-
原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期,自然界中存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
(1)这四种元素中电负性最大的元素,其基态原子的价电子排布图为_____________。
(2)C所在主族的前四种元素分别与A形成的化合物,沸点由高到低的顺序是_______(填化学式),呈现如此递变规律的原因是_______________。
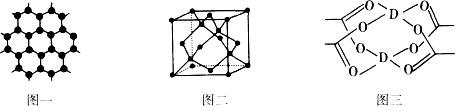
(3)B元素可形成多种单质,一种晶体结构如图一所示,其原子的杂化类型为__________,另一种的晶胞如图二所示,该晶胞的空间利用率为__________,若此晶胞中的棱长为356.6 pm,则此晶胞的密度为________
(保留两位有效数字)。(
)。
(4)D元素形成的单质,其晶体内含有的微粒间作用力是_________,D的醋酸盐晶体局部结构如图三,请用箭头标出图中的配位键。_____
高二化学推断题困难题查看答案及解析
-
短周期元素X、Y、Z、W、Q的原子序数依次增大,且只有一种金属元素.其中X与W处于同一主族,Z元素原子半径在短周期中最大(稀有气体除外).W、Z之间与W、Q之间原子序数之差相等,五种元素原子最外层电子数之和为21,下列说法正确的是
A.Y的简单离子半径小于Z的简单离子半径
B.Z最高价氧化物对应的水化物分别与X、Y最高价氧化物对应的水化物反应生成1mol水时所放出的热量相同
C.Y的简单气态氢化物在一定条件下可被Q单质氧化
D.Q可分别与X、Y、Z、W形成化学键类型相同的化合物
高二化学选择题中等难度题查看答案及解析
-
现有A、B、X、Y、Z五种短周期元素,原子序数依次增大.它们的性质或原子结构如下表:
请回答:元素 性质或原子结构 A 原子核内只有一个质子 B 单质是空气中含量最多的气体 X 原子的最外层电子数是次外层电子数的3倍 Y 短周期元素中原子半径最大的元素 Z 最高正化合价与最低负化合价的代数和为6
(1)X元素在元素周期表中的位置是______.
(2)Z单质通入Y 的最高价氧化物对应水化物的溶液中,可以得到漂白液,相应反应的离子方程式为______.
(3)化合物甲由A和B两种元素组成且质量比为3:14.甲与X单质在催化剂、加热条件下发生的反应是工业上制取硝酸的基础,写出该反应的化学方程式______△4NO+6H2O高二化学解答题中等难度题查看答案及解析
-
已知X、Y、Z、W、K、L六种元素均位于周期表的前四周期,且原子序数依次增大。元素X是周期表中原子半径最小的元素;Y原子核外电子有6种不同的运动状态;W位于第2周期,其原子的核外成对电子数是未成对电子数的3倍;K的+1价阳离子的核外有3层电子且各层均处于全满状态;L位于ds区,它的基态原子的N层上只有2个电子。
请回答下列问题:(答题时,X、Y、Z、W、K、L用所对应的元素符号表示)
(1)ZX5为离子化合物,写出它的电子式_________________。
(2) K的基态原子的电子排布式是______________________。
(3) Y、Z、W元素的第一电离能由大到小的顺序是__________________。
(4)第一电离能I1(L)__I1(K)(填“大于”或“小于”),原因是________________
(5)Y2X4是石油炼制的重要产物之一, 1mol Y2X4分子中含σ键为______mol;
(6)肼(Z2H4)可用作火箭燃料,其原理是:Z2O4(l)+2Z2H4(l)=3Z2(g)+4H2O(g),若反应中有4mol Z-H键断裂,则形成的π键有_________mol.

(7)Z、K两元素形成的某化合物的晶胞结构如图所示,则Z原子的配位数是______。
高二化学综合题中等难度题查看答案及解析