-
(1)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ.则表示甲烷燃烧热的热化学方程式为________.
(2)下表中的数据表示破坏1mol化学键需消耗的能量:根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)=CF4(g)+4HF(g)△H=________.
| 化学键 | C-H | C-F | H-F | F-F |
| 键能 | 414 | 489 | 565 | 158 |
(3)发射卫星用N2H4气体为燃料,NO2气体为氧化剂,两者反应生成N2和水蒸气,已知:
N2 (g)+2O2 (g)=2NO2 (g)△H1=+67.7kJ•mol-1;
2H2 (g)+O2 (g)=2H2O(g)△H2=-484kJ•mol-1;
N2H4 (g)+O2 (g)=N2 (g)+2H2O(g)△H3=-534kJ•mol-1;
H2O(1)=H2O(g)△H5=+44.0kJ•mol-1.
写出N2H4气体与NO2气体反应生成氮气和液态水的热化学方程式:________
(4)下列说法正确的是(填序号)________:
A.同温度下,0.1mol•L-1NH4Cl溶液中NH4+的浓度比0.1mol•L-1氨水中NH4+的浓度大;
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
C.对于Al(OH)3(s)⇌Al(OH)3(aq)⇌Al3+(aq)+3OH-(aq),前段为溶解平衡,后段是电离平衡;
D.除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3的大.
-
(9分)(1)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ。则表示甲烷燃烧热的热化学方程式为_________________________________________________。
(2)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1):
| 化学键 | C—H | C—F | H—F | F—F |
| 键能 | 414 | 489 | 565 | 158 |
根据键能数据计算以下反应的反应热△H:
CH4(g)+4F2(g)= CF4(g)+4HF(g) △H=______________________。
(3) 下列说法正确的是(填序号)__ __:
A 相同温度下,0.1 mol•L-1NH4Cl溶液中NH4+的浓度比0.1 mol•L-1氨水中NH4+的浓度大;
B 用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
C 电解饱和食盐水时,阳极得到氢氧化钠溶液和氢气;
D 对于Al(OH)3(s) Al(OH)3(aq)
Al(OH)3(aq) Al3+(aq)+3OH-(aq),前段为溶解平衡,后段是电离平衡;
Al3+(aq)+3OH-(aq),前段为溶解平衡,后段是电离平衡;
E.除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3的大;
-
I、依据事实,写出下列反应的热化学方程式。
(1)在25 ℃、101 kPa下,1 g甲烷燃烧生成CO2和液态水时放热55.625 kJ。则表示甲烷燃烧热的热化学方程式为________________________。
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为______________。
(3)在25 ℃、101 kPa条件下,C(s)、H2(g)、CH3COOH(1)的燃烧热分别为393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,则2C(s)+2H2(g)+O2(g)===CH3COOH(1)的反应热ΔH为________。
II、锌锰干电池是应用最普遍的电池之一。其基本反应为:
X极:Zn-2e-===Zn2+
Y极:2MnO2+2NH +2e-===Mn2O3+2NH3+H2O
+2e-===Mn2O3+2NH3+H2O
(1)X是电池的________(填“正”或“负”,下同)极,Y是电池的________极。
(2)该电池总反应的离子方程式为:_______________________。
(3)若反应消耗16.25gZn,则电池中转移电子的物质的量为________。
-
(1)在25℃、101kPa下,16g甲烷燃烧生成CO2和液态水时放热889.6kJ。则表示甲烷燃烧的热化学方程式为_________________________________________________。
(2) 下列说法正确的是(填序号)____________:(漏选得1分,错选、多选得0分)
A.相同温度下,0.1 mol?L-1NH4Cl溶液中NH4+的浓度比0.1 mol?L-1氨水中NH4+的浓度大;
B.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
C.电解饱和食盐水时,阳极得到氢氧化钠溶液和氢气;
D.对于Al(OH)3(s) Al(OH)3(aq)
Al(OH)3(aq) Al3+(aq)+3OH-(aq),前段为溶解平衡,后段是电
Al3+(aq)+3OH-(aq),前段为溶解平衡,后段是电
离平衡;
E. 除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比
MgCO3的大;
-
能源问题是人类社会面临的重大课题。甲醇是未来重要的绿色能源之一。
(1)已知:在25℃、101kPa下,1mol甲烷燃烧生成CO2和液态水时放热890.31kJ。请写出甲烷燃烧热的热化学方程式__________。
(2)由CO2和H2合成甲醇的化学方程式为:CO2(g)+3H2(g) CH3OH(g)+H2O(g).在其他条件不变的情况下,实验测得温度对反应的影响如下图所示(注:T1、T2均大300℃) 。
CH3OH(g)+H2O(g).在其他条件不变的情况下,实验测得温度对反应的影响如下图所示(注:T1、T2均大300℃) 。
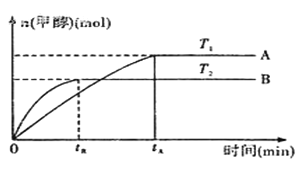
①合成甲醇反应的△H__________(填“>”、“<”或“=”)0。
②平衡常数的表达式为:__________。温度为T2时的平衡常数__________(填“>”、“<”或“=”)温度为T1时的平衡常数。
-
按要求写出下列方程式
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式是:________
(2)已知在25℃、101kPa时,CO的燃烧热为283kJ/mol,相同条件下,若2molCH4完全燃烧生成液态水,所放出的热量为1molCO完全燃烧放出热量的6.3倍,CH4完全燃烧反应的热化学方程式是:________
(3)Al(OH)3的电离反应方程式:________
(4)H2S的电离反应方程式:________
(5)NaHSO4溶于水的电离方程式________
-
依据事实,写出下列反应的热化学方程式。
(1) 在 25℃、 101kPa 下,1g液态乙醇燃烧生成 CO2 和液态水时放热 29.7 kJ。则表示乙醇燃烧热的热化学方程式为_____________________________。
(2)已知拆开1mol H-H键,1mol N-H 键,1mol N≡N 键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2 反应生成NH3 的热化学方程式为____________________________ 。
(3)① P4(白磷,s) + 5O2(g)= P4O10(s) ΔH = -2983.2 kJ/mol② P(红磷,s) + 5/4O2(g)= 1/4 P4O10(s)ΔH = -738.5 kJ/mol,则白磷转化为红磷的热化学方程式为___________________。相同状况下,能量较低的是_____________。
(4)③C(s)+  O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为____。写出CO燃烧的热化学方程式__________。
O2(g) = CO(g) ΔH = -110.5 kJ·mol-1,④ C(s) + O2(g) = CO2(g) ΔH = -393.5 kJ·mol-1,则燃烧36g C(s)生成CO2,放出的热量为____。写出CO燃烧的热化学方程式__________。
-
依据事实,写出下列反应的热化学方程式。
(1)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为 。
(2)用CH4催化还原NOx可以消除氮氧化物的污染。例如:
CH4(g)+4NO2(g) =4NO(g)+CO2(g)+2H20(g) △H=-574 kJ·mol-1
CH4(g)+4NO(g) =2N2(g)+CO2(g)+2H2O(g) △H=-1160 kJ·mol-1
若用标准状况下4.48L CH4还原NO2至N2整个过程中转移的电子总数为 (阿伏加德罗常数的值用NA表示),放出的热量为__ _____kJ。
-
依据事实,写出下列反应的热化学方程式。
(1)在25℃、101 kPa下,1 g甲醇燃烧生成CO2和液态水时放热22.68 kJ。则表示甲醇燃烧热的热化学方程式为 。
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为 。
(3)NA为阿伏加德罗常数,C2H2(g)完全燃烧生成CO2和液态水的反应,有5NA个电子转移时,放出650 kJ的热量,该反应的热化学方程式为 。
-
(1)在25℃、101 kPa下,1 6g甲醇( )燃烧生成CO2和液态水时放热362.88 kJ。则表示甲醇燃烧热的热化学方程式为 。
)燃烧生成CO2和液态水时放热362.88 kJ。则表示甲醇燃烧热的热化学方程式为 。
(2)已知热化学方程式:SO2(g)+ O2(g)
O2(g) SO3(g)△H=―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为 。
SO3(g)△H=―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为 。
Al(OH)3(aq)
Al3+(aq)+3OH-(aq),前段为溶解平衡,后段是电离平衡;
