钛合金被誉为二十一世纪的金属,具有广泛的用途.金属钛可用下列方法提炼:
①TiO2+2C+2Cl2TiCl4+2CO ②TiCl4+2Mg
2MgCl2+Ti
对上述两个反应,下列有关叙述正确的是
A. 反应①中Cl2是还原剂 B. 反应①中碳元素被还原反应
C. ②中钛元素被氧化 D. 反应②中TiCl4是氧化剂
高二化学选择题中等难度题
钛合金被誉为二十一世纪的金属,具有广泛的用途.金属钛可用下列方法提炼:
①TiO2+2C+2Cl2TiCl4+2CO ②TiCl4+2Mg
2MgCl2+Ti
对上述两个反应,下列有关叙述正确的是
A. 反应①中Cl2是还原剂 B. 反应①中碳元素被还原反应
C. ②中钛元素被氧化 D. 反应②中TiCl4是氧化剂
高二化学选择题中等难度题
钛合金被誉为二十一世纪的金属,具有广泛的用途。金属钛可用下列方法提炼:
① TiO2+2C+2Cl2TiCl4+2CO
② TiCl4+2Mg2MgCl2+Ti
对上述两个反应,下列有关叙述正确的是
A.反应①中碳元素被还原 B.反应②中钛元素被氧化
C.反应①中Cl2是还原剂 D.反应②中TiCl4是氧化剂
高二化学选择题中等难度题查看答案及解析
钛合金被誉为二十一世纪的金属,具有广泛的用途。金属钛可用下列方法提炼:
① TiO2+2C+2Cl2TiCl4+2CO;② TiCl4+2Mg
2MgCl2+Ti
对上述两个反应,下列有关叙述正确的是
A.反应①中碳元素被还原 B.反应②中钛元素被氧化
C.反应①中Cl2是还原剂 D.反应②中TiCl4是氧化剂
高二化学选择题中等难度题查看答案及解析
钛合金被誉为二十一世纪的金属,具有广泛的用途.金属钛可用下列方法提炼:
①TiO2+2C+2Cl2TiCl4+2CO ②TiCl4+2Mg
2MgCl2+Ti
对上述两个反应,下列有关叙述正确的是
A. 反应①中Cl2是还原剂 B. 反应①中碳元素被还原反应
C. ②中钛元素被氧化 D. 反应②中TiCl4是氧化剂
高二化学选择题中等难度题查看答案及解析
钛合金被誉为二十一世纪的金属,具有广泛的用途。金属钛可用下列方法提炼:
①TiO2+2C+2Cl2TiCl4+2CO
②TiCl4+2Mg2MgCl2+Ti
对上述两个反应,下列有关叙述正确的是
A. 反应①中碳元素被还原 B. 反应②中钛元素被氧化
C. 反应①中Cl2是还原剂 D. 反应②中TiCl4是氧化剂
高二化学选择题中等难度题查看答案及解析
铜是人类最早发现和使用的金属之一,铜及其合金的用途广泛。粗铜中含有少量铁、锌、银、金等杂质,工业上可用电解法精炼粗铜制得纯铜,下列说法正确的是
A. 精铜做阳极,粗铜做阴极
B. 可用AgNO3溶液做电解质溶液
C. 电解时,阴极反应为Cu – 2e- === Cu2+
D. 电解后,可用阳极泥来提炼金、银
高二化学单选题中等难度题查看答案及解析
铜、铁都是日常生活中常见的金属,它们的单质及其化合物在科学研究和工农业生产中具有广泛用途。
请回答以下问题:
(1)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
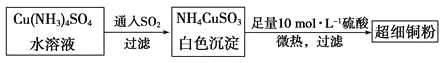
①Cu2+的价电子排布图________________; NH4CuSO3中N、O、S三种元素的第一电离能由大到小顺序为_______________________(填元素符号)。
②SO42-的空间构型为_____________,SO32-离子中心原子的杂化方式为__________。
(2)请写出向Cu(NH3)4SO4水溶液中通入SO2时发生反应的离子方程式:___________。
(3)某学生向CuSO4溶液中加入少量氨水生成蓝色沉淀,继续加入过量氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体。
①下列说法正确的是________
a.氨气极易溶于水,是因为NH3分子和H2O分子之间形成3种不同的氢键
b.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
c.Cu(NH3)4SO4所含有的化学键有离子键、极性共价键和配位键
d.Cu(NH3)4SO4组成元素中电负性最大的是氮元素
②请解释加入乙醇后析出晶体的原因_____________________.
高二化学综合题中等难度题查看答案及解析
(16分)钠及其化合物具有广泛的用途。
(1)工业上制备金属钠的常用方法是 (用离子方程式表示)。
(2)用Na2CO3熔融盐作电解质,CO、O2、CO2为原料可组成新型电池。该电池的结构如图所示:
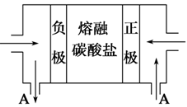
正极的电极反应式为 ,电池工作时物质A可循环使用,A物质的化学式为 。
(3)常温下,浓度均为0.1 mol·L-1的下列五种钠盐溶液的pH如下表:
| 溶质 | CH3COONa | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 11.6 | 10.3 | 11.1 |
上述盐溶液的阴离子中,结合H+能力最强的是 ,根据表中数据,浓度均为0.01 mol·L-1下列四种酸的溶液分别稀释100倍,pH变化最大的是 (填序号)。
a.HCN b.HClO c.CH3COOH d.H2CO3
(4)实验室中常用NaOH来进行尾气处理、洗气和提纯。
①常温下,当300 mL 1 mol·L-1的NaOH溶液吸收4.48 L(折算成标准状况)SO2时,所得溶液pH>7,则溶液中各离子浓度由大到小的顺序为 。
②已知几种离子开始沉淀时的pH如下表:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
当向含相同浓度Cu2+、Mg2+、Fe2+的溶液中滴加某浓度的NaOH溶液时, (填离子符号)先沉淀,Ksp[Fe(OH)2] Ksp[Mg(OH)2](填“>”、“=”或“<”)。
高二化学填空题困难题查看答案及解析
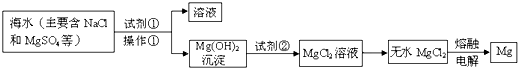
高二化学解答题中等难度题查看答案及解析
碱金属及其化合物在生活和化工生产中具有广泛的用途,下列说法正确的是
A.钠钾合金能用作原子反应堆的导热剂是由于二者是活泼金属易失电子
B.用饱和碳酸氢钠制造灭火剂比用饱和碳酸钠制造灭火剂的效果好
C.碳酸钠可用于制造洗涤剂,因为碳酸钠是碱
D.五彩缤纷的焰火是K单质燃烧所致
高二化学选择题困难题查看答案及解析
金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高强度和铝的低密度。其单质和化合物具有广泛的应用价值。氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2 (如图1)。

图中的M是短周期金属元素,M的部分电离能如下表:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/kJ·mol-1 | 738 | 1451 | 7733 | 10540 | 13630 |
请回答下列问题:
(1)Ti的基态原子外围电子排布式为_______________。
(2)M是_______(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为_______。
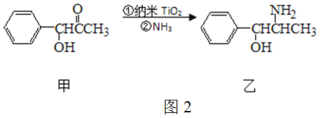
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示。化合物甲的分子中一个苯环的σ键有____个,化合物乙中碳,氧,氮三个原子对应的第一电离能由大到小的顺序为____________。
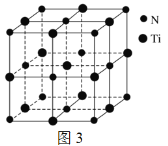
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a×10-10 cm,则该氮化钛的密度为______ g·cm-3(NA为阿伏加德罗常数的值,只列计算式)。
(5)图3中Ti3+可形成配位数为6的空间构型,问它构成的立体构型为______面体。
高二化学综合题中等难度题查看答案及解析