如图所示是298 K时N2与H2反应过程中 ,能量变化的曲线图.下列叙述正确的是
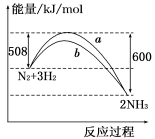
A.该反应的热化学方程式为: N2+3H22NH3 ΔH=-92 kJ/mol
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热改变
D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1
高二化学选择题困难题
如图所示是298 K时N2与H2反应过程中 ,能量变化的曲线图.下列叙述正确的是

A.该反应的热化学方程式为: N2+3H22NH3 ΔH=-92 kJ/mol
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热改变
D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1
高二化学选择题困难题
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是
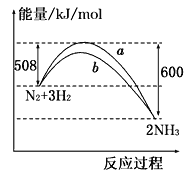
A. 该反应的热化学方程式为:N2 + 3H2 2NH3, △H = -92kJ·mol-1
B. 在温度体积一定的条件下, 通入lmol N2和3molH2反应后放出的热量为92kJ
C. b曲线是加入催化剂时的能量变化曲线
D. 加入催化剂, 该化学反应的ΔH不改变
高二化学null简单题查看答案及解析
如图所示是298K时,N2与H2反应过程中能量变化的曲线图,下列叙述正确的是
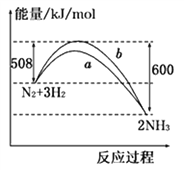
A. 该反应的热化学方程式为:N2+ 3H2 2NH3, △H = -92kJ·mol-1
B. 加入催化剂, 该化学反应的ΔH不改变
C. b曲线是加入催化剂时的能量变化曲线
D. 在温度体积一定的条件下, 通入lmol N2和3molH2反应后放出的热量为92kJ
高二化学单选题中等难度题查看答案及解析
如图是298K 时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是 ( )
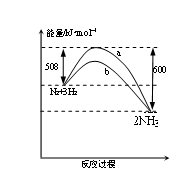
A. 该反应的热化学方程式为:
N2(g) + 3H2(g) 2NH3(g) ΔH = 92kJ·mol-1
B.b曲线是升高温度时的能量变化曲线
C. 加入催化剂, 该化学反应的活化能和反应热都改变
D. 在温度体积一定的条件下, 通入lmol N2和3molH2 反应后放出的热量为Q1kJ, 若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ 则184>Q2 >2Q1
高二化学选择题简单题查看答案及解析
右图是298K 时N2与H2反应过程中能量变化的曲线图。下列叙述不正确的是
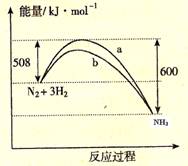
A. 该反应的热化学方程式为:N2(g) + 3H2(g) 2NH3(g), △H = -92kJ·mol-1
B. b曲线是加入催化剂时的能量变化曲线
C. 加入催化剂, 该化学反应的活化能和反应热都改变
D. 在温度体积一定的条件下, 通入lmol N2和3molH2 反应后放出的热量为Q1kJ, 若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ 则184>Q2 >2Q1
高二化学选择题简单题查看答案及解析
右图是298K 时N2与H2反应过程中能量变化的曲线图。下列叙述不正确的是( )
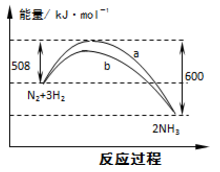
A.该反应的热化学方程式为:N2(g) + 3H2(g) 2NH3(g) ΔH = -92kJ·mol-1
B.b曲线是加入催化剂时的能量变化曲线
C.加入催化剂, 该化学反应的活化能和反应热都改变
D.在温度体积一定的条件下, 通入lmol N2和3molH2 反应后放出的热量为Q1kJ, 若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ 则184>Q2 >2Q1
高二化学选择题简单题查看答案及解析
右图是298K 时N2与H2反应过程中能量变化的曲线图。下列叙述不正确的是

A. 该反应的热化学方程式为:N2(g) + 3H2(g) 2NH3(g) ΔH = -92kJ·mol-1
B. b曲线是加入催化剂时的能量变化曲线
C. 加入催化剂, 该化学反应的活化能和反应热都改变
D. 在温度体积一定的条件下, 通入lmol N2和3molH2 反应后放出的热量为Q1kJ, 若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ 则184>Q2 >2Q1
高二化学选择题简单题查看答案及解析
上图是298K 时N2与H2反应过程中能量变化的曲线图。下列叙述错误的是
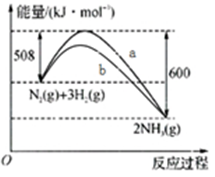
A.该反应的热化学方程式为:N2(g) + 3H2(g) 2NH3(g) ΔH =-92kJ·mol-1
B.b曲线是加入催化剂时的能量变化曲线
C.加入催化剂, 该化学反应的活化能和反应热都改变
D.在温度体积一定的条件下, 通入lmol N2和3molH2 反应后放出的热量为Q1kJ, 若通入2mol N2和6mol H2 反应后放出的热量为Q2kJ 则184>Q2 >2Q1
高二化学选择题中等难度题查看答案及解析
如图所示是298 K时N2与H2反应过程中 ,能量变化的曲线图.下列叙述正确的是

A. 该反应的热化学方程式为: N2+3H22NH3ΔH=-92 kJ/mol
B. a曲线是加入催化剂时的能量变化曲线
C. 加入催化剂,该化学反应的反应热改变
D. 在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2kJ,则184>Q2>2Q1
高二化学单选题简单题查看答案及解析
如图所示是298 K时N2与H2反应过程中 ,能量变化的曲线图.下列叙述正确的是

A.该反应的热化学方程式为: N2+3H22NH3 ΔH=-92 kJ/mol
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热改变
D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1
高二化学选择题困难题查看答案及解析
如图所示是298 K时N2与H2反应过程中 ,能量变化的
曲线图.下列叙述正确的是
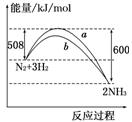
A.该反应的热化学方程式为:N2+3H22NH3 ΔH=-92 kJ/mol
B.a曲线是加入催化剂时的能量变化曲线
C.加入催化剂,该化学反应的反应热改变
D.在温度、体积一定的条件下,通入1 mol N2和3 mol H2反应后放出的热量为Q1 kJ,
若通入2 mol N2和6 mol H2反应后放出的热量为Q2 kJ,则184>Q2>2Q1
高二化学选择题简单题查看答案及解析