-
元素周期表是学习物质结构和性质的重要工具,元素周期律反映了元素性质的周期性变化规律。
(1)元素A的原子最外层电子排布式为nsnnpn,该原子最外层共有________种不同运动状态的电子,该原子核外共有________种能量不同的电子。元素A与氢元素形成的分子,其空间结构可能是(填序号)________。
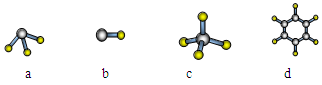
(2)下列变化规律中正确的是 ________。
A.金属K、Na、Mg的熔沸点由低到高
B.C1-、Br-、I-的失电子能力由弱到强
C.H+、Li+、H-的半径由大到小
D.H3PO4、HClO4、H2SO4的酸性由弱到强
(3)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如下表所示,其中A的电子式为________ ,E的化学式为________。
| 氢化物 | A | B | HF | D | E |
| 沸点/℃ | 1317 | 100 | 19.5 | 33 | 164 |
-
【化学—选修3:物质结构和性质】(15分)
元素周期表是研究元素原子结构及性质的重要工具。现有X、Y和Z三种元素,其原子序数依次减小。X元素原子的4p轨道上有3个未成对电子,Y元素原子的最外层2p轨道上有2个未成对电子,X跟Y可形成化合物X2Y3。Z元素既可以形成正一价离子也可形成负一价离子。请回答下列问题:
(1)Y元素原子的价层电子的轨道表示式为______________,该元素的名称是_____;
(2)在X与Z形成的化合物XZ3中,X的杂化类型是 ,该化合物的空间构型为_____________;短周期元素形成的化合物中与XZ3互为等电子体的是 ;
(3)请写出X的两种含氧酸的化学式 、 ,其中酸性较强的是 。
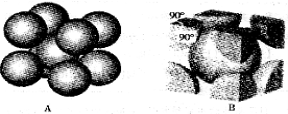
(4)Q与Z同主族。Q单质的晶胞如下图所示,若设该晶胞的密度为ag/cm3,阿伏加德罗常数为NA,Q原子的摩尔质量为M,则表示Q原子半径的计算式为 。
-
元素周期表是学习和研究化学的重要工具。按要求回答下列问题:
A、B、C、D、E是短周期元素,其原子序数依次增大。A、C两元素的最外层只有一个电子,C离子的电子层结构与周期表中非金属性最强的元素的阴离子的电子层结构相同;元素A可以和B形成A2B和A2B2两种分子;化合物甲和乙的每个分子中均含有5个原子,甲是由元素D与A组成,其分子的核外电子总数为18,乙是由元素D与E组成;化合物丙是由C与E组成的。
(1)元素B、D、E的元素符号依次为_______、_______、______。
(2)上述5种元素形成的分子中,除甲分子外,核外电子总数也为18的有___(填分子式)
(3)D的氧化物在高温下可以与C的碳酸盐发生反应,其化学反应方程式为________;化合物乙遇水剧烈反应有白雾生成,其反应的化学方程式为___________。
(4)用500mL容量瓶配制400mL 1mol/L的丙溶液,需要丙的质量为________;配制过程中除用到容量瓶外,还需要的玻璃仪器有___________________。电解所配制的400mL溶液,当电路中通过1mol电子时,理论上可收集到的气体在标准状况下的体积为_________L。
-
元素在周期中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
A.由于氟位于周期中表中的第VIIA族,所以HFO也可以称为次氟酸
B.短周期元素形成离子后,最外层都达到8电子稳定结构
C.第三周期元素的最高正化合价等于它所处的主族序数
D.质量数相同的原子,最外层电子数相同,化学性质也相同
-
[化学——选修物质结构与性质](15分)
在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,它们的原子最外层电子数依次为2、2、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数为18,E、D两元素处于同族,且在该族元素中,E的气态氢化物的沸点最高。
(1)B元素在周期表中的位置;(2分)
D元素基态原子电子排布式为_____________________________。(2分)
(2)E的气态氢化物在同族元素中沸点最高的原因是:
________。(2分)
(3)A、C两元素第一电离能________>________。(填元素符号)(2分)
(4)B元素能形成多种配合物。元素之间形成配合物的条件是:一方是能够提供孤对电子的原子,另一方是________的原子。(2分)
(5)A元素可与氢元素形成离子化合物,电子式为_______________;(2分)这种离子化合物可与水反应,化学方程式为________________________________。(3分)
-
元素在元素周期表中的位置,反映了元素的原子结构和元素的性质。下列说法正确的是
( )
A.同一元素不可能既表现金属性,又表现非金属性
B.短周期元素形成离子后,最外层都达到8 电子稳定结构
C.第三周期元素的最高正化合价等于它所处的主族序数
D.同一主族元素的原子,最外层电子数相同,化学性质完全相同
-
[选修物质结构与性质](15分)
A、B、C、D、E、F为六种短周期元素,它们核电荷数依次递增。已知:B原子核外最外层电子数是次外层电子数的两倍,电子总数是E原子总数的1/2,F是同周期元素中原子半径最小的元素;D2-与E2+的电子层结构相同。B与D可以形成三原子化合物甲。A是非金属元素,且A、C、F可形成离子化合物乙。请回答:
(1)C单质的电子式________,F元素原子的电子排布式________,E元素的原子结构示意图是________。
(2)化合物乙中含有的化学键是________。
(3)化合物甲为固体时属于________晶体,E单质在一定条件下与甲反应的化学方程式为________。
(4)如图立方体中心的“·”表示B单质所形成的原子晶体中的一个原子,请在立方体的顶点用“·”表示出与之紧邻的B原子
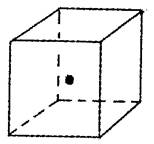
-
【化学——选修物质结构与性质】(15分)A、B、C、D都是元素周期表中的短周期元素,它们的核电荷数依次增大。第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素,D原子的S电子与P电子数相等,E是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请用对应的元素符号或化学式回答下列问题:
(1)A、B、C的电负性由小到大的顺序为 __;D的稳定离子核外有 种运动状态的电子 .
(2)A的最高价氧化物对应的水化物分子中其中心原子采取 杂化。
(3)已知A、C形成的化合物分子甲与B的单质分子结构相似, 1 mol甲中含有 键的数目为 。
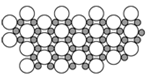
(4)科学家发现硼化D在39K时呈超导性,在硼化D晶体的理想模型中,D原子和硼原子是分层排布的,一层D一层硼相间排列。下图是该晶体微观空间中取出的部分原子沿Z轴方向的投影,白球是D原子投影,黑球是硼原子投影,图中的硼原子和D原子投影在同一平面上。根据图示确定硼化D的化学式为_______。
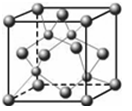
(5)E的外围电子排布式是 ;E的氢化物的晶体结构如下图所示,此氢化物化学式是 ;写出此氢化物在氯气中燃烧的化学方程式 。
-
[化学—选修3:物质结构与性质]已知:G、Q、R、T、X、Y、Z都是周期表中前四周期的元素,它们的核电荷数依次增大。G的简单阴离子最外层有2个电子,Q原子最外层电子数是内层电子数的两倍,X元素最外层电子数与最内层电子数相同;T2R的晶体类型是离子晶体,Y原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于原子晶体;在元素周期表中Z元素位于第10列。回答下列问题:
(1)Z原子的核外电子排布式是 。
(2)X以及与X左右相邻的两种元素,其第一电离能由小到大的顺序为 。
(3)QR2分子中,Q原子采取__________杂化,写出与QR2互为等电子体的一种分子和一种离子的化学式: ; 。
(4)分子式为Q2G6R的物质有两种,其中一种易溶于水,原因是 ;T的氯化物的熔点比Y的氯化物的熔点高,原因是 。
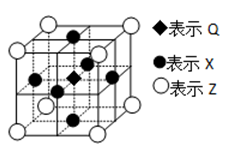
(5)据报道,由Q、X、Z三种元素形成的一种晶体具有超导性,其晶体结构如右图所示。晶体中距每个X原子周围距离最近的Q原子有__________个。
-
【化学--物质结构与性质】
A、B、C都是元素周期表中的短周期元素,它们的核电荷数依次增大.第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为________.
(2)A的最高价氧化物对应的水化物分子中其中心原子采取________杂化.
(3)与A、B形成的阴离子(AB-)互为等电子体的分子有________.
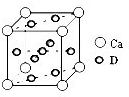
(4)基态D原子的核外电子排布式为________,右图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比为________.
(5)向D的高价态硫酸盐溶液中逐滴滴加B的氢化物水溶液至过量,先出现沉淀,最后沉淀溶解形成溶液.写出此沉淀溶解的离子方程式:________.