现将浓度相等、体积分别为V1、V2的H2SO4、NaOH溶液混合,测量混合液温度,结果如图(已知:V1+V2=60mL)。下列叙述错误的是 ( )
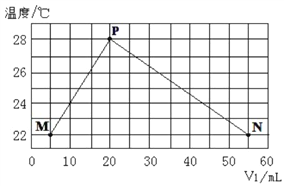
A. 实验的环境温度低于22℃ B. 混合溶液的导电能力:M>N
C. P点混合溶液呈中性 D. 若将H2SO4改为CH3COOH,P点温度低于28℃
高二化学选择题困难题
现将浓度相等、体积分别为V1、V2的H2SO4、NaOH溶液混合,测量混合液温度,结果如图(已知:V1+V2=60mL)。下列叙述错误的是 ( )

A. 实验的环境温度低于22℃ B. 混合溶液的导电能力:M>N
C. P点混合溶液呈中性 D. 若将H2SO4改为CH3COOH,P点温度低于28℃
高二化学选择题困难题
现将浓度相等、体积分别为V1、V2的H2SO4、NaOH溶液混合,测量混合液温度,结果如图(已知:V1+V2=60mL)。下列叙述错误的是 ( )

A. 实验的环境温度低于22℃ B. 混合溶液的导电能力:M>N
C. P点混合溶液呈中性 D. 若将H2SO4改为CH3COOH,P点温度低于28℃
高二化学选择题困难题查看答案及解析
现将浓度相等、体积分别为V1、V2的CH3COOH、NaOH溶液混合,测量混合液温度,结果如图(已知:V1+V2=50 mL)。下列叙述错误的是( )
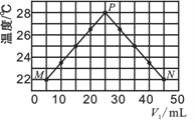
A. 实验的环境温度低于 22℃
B. P点的混合溶液的pH=7
C. 混合溶液的导电能力:M > N
D. 若将CH3COOH改为HCl,P点温度高于 28℃
高二化学单选题困难题查看答案及解析
现将浓度相等、体积分别为V1、V2的CH3COOH、NaOH溶液混合,测量混合液温度,结果如图(已知:V1+V2=50mL).下列叙述正确的是

A.若将CH3COOH改为HCl,P点温度高于28℃
B.从M到N过程中c(H+)逐渐减小
C.混合溶液的导电能力:N>M
D.实验的环境温度等于22℃
高二化学选择题困难题查看答案及解析
某研究小组将V1 mL 0.50 mol/L H2SO4溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验装置和实验结果如下图所示(实验中始终保持V1+V2=50 mL)。回答下列问题:

(1)如图所示实验装置中有一个明显的 错误________。
(2)为了减少实验误差,实验过程中将NaOH溶液_______(选填“一次”或“分多次”)倒入盛有稀硫酸的小烧杯中。溶液混 合后,准确读取混合溶液的______,记为终止温度。
(3)研究小组做该实验时环境温度_____22 ℃(填“高于”、“低于”或“等于”),判断的依据是_____________。
(4)由题干及图形可知,V1︰V2=____________时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为___________mol/L。
(5)若通过实验测定及有关计算知此反应共放出a kJ的热量,请写出此反应的热化学方程式:_____________________________________________________________________
高二化学实验题中等难度题查看答案及解析
(题文)将V1 mL 1.00 mol·L-1HCl溶液V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是( )
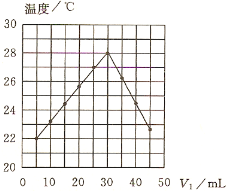
A. 做该实验时环境温度为22 ℃
B. 该实验表明化学能可以转化为热能
C. NaOH溶液的浓度约是1.00 mol·L-1
D. 该实验表明有水生成的反应都是放热反应
高二化学单选题简单题查看答案及解析
(题文)将V1 mL 1.00 mol·L-1HCl溶液V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是( )
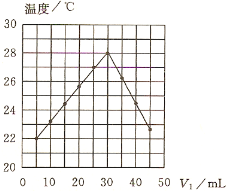
A. 做该实验时环境温度为22 ℃
B. 该实验表明化学能可以转化为热能
C. NaOH溶液的浓度约是1.00 mol·L-1
D. 该实验表明有水生成的反应都是放热反应
高二化学单选题简单题查看答案及解析
将V1 mL 1.00 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是( )
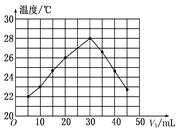
A. 做该实验时环境温度为22℃
B. NaOH溶液的浓度约为1.00 mol/L
C. 该实验表明有水生成的反应都是放热反应
D. 该实验表明化学能可以转化为热能
高二化学选择题中等难度题查看答案及解析
将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。下列叙述正确的是( )
A.做该实验时环境温度为22 ℃ B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约是1.00 mol/L D.该实验表明有水生成的反应都是放热反应
高二化学单选题简单题查看答案及解析
(1)某研究小组将V1 mL 1.0 mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50 mL)。由题干及图形可知,V1∶V2=________时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为__________mol/L。若NaOH溶液用相同浓度和体积的下列溶液代替,则对中和热数值测定结果将如何影响(填“偏大”、“偏小”、“无影响”):KOH溶液______;氨水(NH3·H2O)___________。
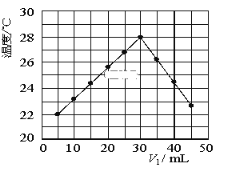
(2)用惰性电极进行电解下列电解质溶液。
①电解氯化铜溶液,在阴极上和阳极上析出产物的物质的量之比为___________
②MnO2可做超级电容器材料,电解MnSO4溶液可制得MnO2,其阳极的电极反应式_________________
(3)室温下,0.1mol/L的亚硝酸(HNO2)、次氯酸的电离常数Ka分别为: 7.1 10-4, 2.98 10-8。将0.1mol/L的亚硝酸稀释100倍,c(H+)将_______(填“不变”、“增大”、“减小”)。写出HNO2、HClO、NaNO2、NaClO四种物质之间发生的复分解反应的离子方程式_______________。
(4)酸HX和碱AOH恰好完全中和时溶液的pH等于7,酸HY和碱BOH恰好完全中和时溶液的pH也等于7,酸HX和碱BOH恰好完全中和时溶液的pH小于7,请推断
①以上酸碱中必为弱电解质的是_______________
②比较两种酸HX和HY的酸性强弱 ___________>___________
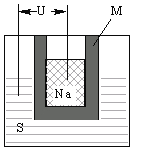
(5)如图为钠硫高能电池的结构示意图,该电池的工作温度为320 ℃左右,电池反应为2Na+xSNa2Sx,正极的电极反应式为_________。与铅蓄电池相比,当消耗相同质量的负极活性物质时,钠硫电池的理论放电量是铅蓄电池的__________
倍。
(6)已知常温下Fe(OH)3和Mg(OH)2的Ksp分别为8.010-38、1.0
10-11,向浓度均为0.1 mol/L的FeCl3、MgCl2的混合溶液中加入碱液,要使Fe3+完全沉淀而Mg2+不沉淀,应该调节溶液pH的范围是________。(已知lg 2=0.3)
高二化学综合题中等难度题查看答案及解析
将V1 mL 1.00 mol·L-1 HCl溶液和V2 mL 未知浓度的NaOH溶液混合均匀后,测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL)。
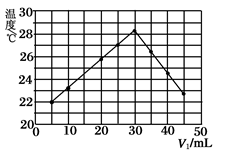
下列叙述正确的是
A.做该实验时环境温度为22 ℃
B.该实验表明化学能可以转化为热能
C.NaOH溶液的浓度约为1.00 mol·L-1
D.该实验表明有水生成的反应都是放热反应
高二化学选择题困难题查看答案及解析