-
研究发现:一节电池烂在地里,能够使一平方米的土地失去利用价值。废旧电池的危害上要集中在其中所含的少量重金属上。将废旧锌锰电池回收处理,既能减少它对环境的污染,又能实现废电池的资源化利用。
(1)回收填料中的二氧化锰和氯化铵。已知:废旧干电池填料的主要成分为二氧化锰、炭粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水。回收物质的流程如图所示。
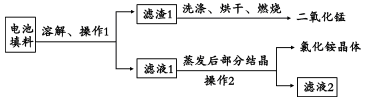
① 操作中先将电池填料研碎的目的是:________________。
② 操作l和操作2的名称都是___________,该操作中玻璃棒的作用是___________。
③ 灼烧滤渣l的目的是______________________。
(2)回收二氯化锰:将废旧锌锰电池处理,得到含锰混合物,向该混合物加入浓盐酸并加热。
①写出MnOOH与浓盐酸反应的化学方程式:________________。
② 锰回收新方法:向废旧锌锰电池内的混合物[主要成分MnOOH、Zn(OH)2]中加入一定量的稀硫酸和稀草酸(H2C2O4),并不断搅拌至无CO2产生为止,写出MnOOH参与反应的化学方程式______________。与使用浓盐酸回收锰相比,新方法的优点是___________(答l点即可)。
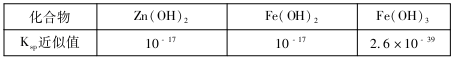
(3)用废电池的锌皮可用于回收制作ZnSO4·7H2O。过程中,需除去锌皮中的少量杂质铁,其方法是:常温下,加入稀H2SO4和H2O2,铁溶解变为Fe3+,加碱调节pH为4,使溶液中的Fe3+转化为Fe(OH)3沉淀,此时溶液中c(Fe3+)=_________。继续加碱调节pH为____时,锌开始沉淀(假定Zn2+浓度为0.1mol/L)。部分难溶的电解质溶度积常数(Ksp)如下表:
-
化学与生活、生产、社会关系密切。下列叙述正确的是
A.废旧电池应集中回收进行填埋处理
B.少量钠、钾要在干燥的试剂瓶中保存妥善保管
C.目前治理白色污染的方法主要是减少使用、加强回收和再利用
D.为了防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰
-
Ni-MH电池在工农业生产和日常生活中具有广泛用途,废旧电池中含有大量金属元素,其回收利用具有非常重要的意义。一种利用废Ni-MH电池正极材料(主要含有Ni(OH)2,还含有少量Fe、Cu、Ca、Mg、Mn、Zn的氢氧化物)制备电子级硫酸镍晶体的工艺流程如下图所示:

回答下列问题:
(1)“浸出”时温度、硫酸浓度、浸出时间对镍浸出率的影响如下图:
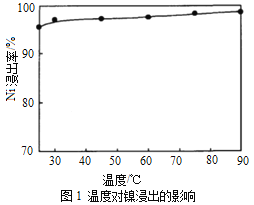
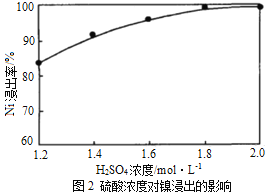
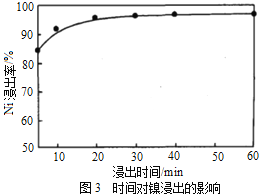
则“浸出”时最适宜的条件为_______________。
(2)在“滤液1”中加入双氧水可将Fe2+转化为难溶的针铁矿(FeOOH),写出反应的离子方程式:______________。
(3)“滤液2”中加入NaF 可将滤液中Ca2+、Mg2+转化为难溶的CaF2和MgF2。当加入过量NaF后,所得“滤液3”中c(Mg2+)∶c(Ca2+)=0.67,则MgF2 的溶度积为_____________[已知Ksp(CaF2)=1.10×10-10]。
(4)向“滤液3”中加入(NH4)2S2O8可以除锰,在此过程中(NH4)2S2O8与MnSO4反应生成含锰元素的一种黑色不溶物、硫酸铵及硫酸,写出该反应的化学方程式___________________。
(5)向“滤液4”加入有机萃取剂后,Zn2+与有机萃取剂(用HA表示) 形成易溶于萃取剂的络合物ZnA2·2HA。该过程可以表示为:Zn2++4HA ZnA2·2HA+2H+
ZnA2·2HA+2H+
①已知加入萃取剂后,锌的萃取率随料液pH 变化如图所示。试分析pH 增大时,锌的萃取率逐渐增大的原因是___________________。
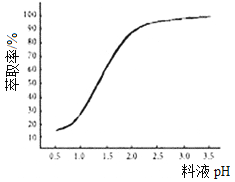
②“操作X”的名称是_____________。
(6)上述回收镍的过程中,使用了1kg 含镍37.1%的正极材料,最终得到纯净的NiSO4·7H2O 1.686kg,则镍的回收率为_______________。
-
化学与人类的生产、生活密切相关。下列说法正确的是( )
A.废旧电池应集中处理的首要原因是回收利用其中的金属材料
B.新型冠状病毒对人类健康构成严重威胁,常用95%的酒精作新冠消毒剂
C.油脂属于高分子化合物,使用一定的油脂能促进人体对某些维生素的吸收
D.将少量二氧化硫添加于红酒中可以起到杀菌和抗氧化作用,是法律允许的做法
-
废旧锂离子电池的回收利用意义重大,其正极废料的主要成分是 ,铝、炭黑及其他杂质,回收利用的流程如图1:
,铝、炭黑及其他杂质,回收利用的流程如图1:
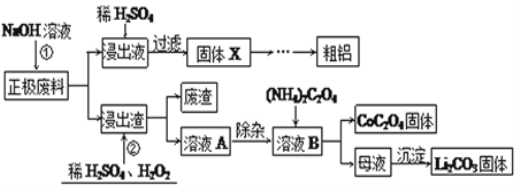
图1
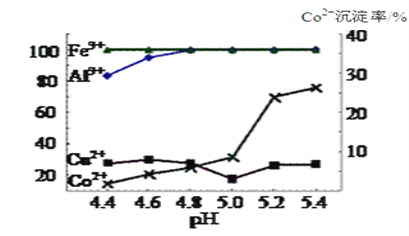
图2
已知A溶液主要的金属离子是 、
、 ,还含有少量
,还含有少量 、
、 、
、 .
.
 步骤
步骤 中铝溶解的离子方程式为 ______ ,固体X的成分是 ______ ;
中铝溶解的离子方程式为 ______ ,固体X的成分是 ______ ;
 步骤
步骤 中
中 固体溶解的化学方程式为 ______ ,该反应的还原剂是 ______ ;
固体溶解的化学方程式为 ______ ,该反应的还原剂是 ______ ;
 实验表明溶液A中各种金属离子的沉淀率随pH的变化如图2,除杂时加入氨水调节溶液的pH,可除去杂质离子是 ______ ;
实验表明溶液A中各种金属离子的沉淀率随pH的变化如图2,除杂时加入氨水调节溶液的pH,可除去杂质离子是 ______ ;
 母液中含量最大三种离子是 ______ ;
母液中含量最大三种离子是 ______ ;
 从1000g锂离子电池正极材料
从1000g锂离子电池正极材料 元素含量为
元素含量为 中可回收
中可回收 质量为 ______
质量为 ______  已知回收率为
已知回收率为 ,
, 的化学式量为74).
的化学式量为74).
-
废旧锂离子电池的回收利用意义重大,其正极废料的主要成分是LiCoO2、铝、炭黑及其他杂质,回收利用的流程如下图。
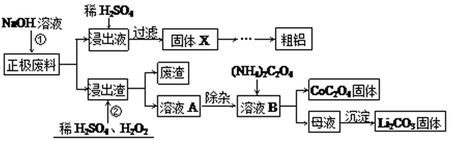
已知“溶液A”中主要金属离子是Co2+、Li+,还含有少量Fe3+、Al3+、Cu2+。
(1)写出步骤①中溶解铝的离子方程式:___________________,写出固体X到粗铝过程中所涉及的化学方程式:________________________。
(2)步骤②加入H2SO4和物质Y,物质Y可能为________(填序号)。
a.KMnO4溶液 b.稀硝酸溶液 c. H2O2溶液
写出步骤②中LiCoO2固体溶解的化学方程式:_______________________。
(3)实验表明溶液A中各种金属离子的沉淀虑随pH的变化如下图,现向溶液A中加入氨水,除去杂质离子________(填离子符合),应调节pH范围为_____________。
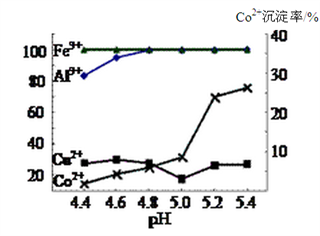
(4)母液中主要的溶质为_________________。
(5)从2kg锂离子电池正极材料(Li元素含量为7%)中可回收LiCO3的质量为_______g。(已知回收率为85%)
-
废旧锂离子电池的回收利用的意义重大,其正极废料的主要成分是LiCoO2、铝、炭黑及其他杂质,回收利用的流程如下:
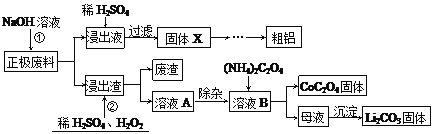
已知“溶液A”中主要金属离子是Co2+、Li+,还含有少量Fe3+、Al3+、Cu2+。
(1)步骤①中铝溶解的离子方程式为_________________,固体X的成分是_________。
(2)步骤②中LiCoO2固体溶解的化学方程式为_______________ ,该反应的还原剂是_______。
(3)母液中含量最大的三种离子是_________。
(4) (NH4)2C2O4是一种化学实验室常用的试剂,预测其溶解性___________(填“可溶于水”或“不溶于水”)。一定温度下,(NH4)2C2O4固体可分解出NH3和CO等物质,思考其它的产物并写出其分解的化学方程式__________________。
-
锂离子电池应用十分广泛,从废旧钻酸锂(LiCoO2)锂离子电池中回收铝、铁、钴、锂等元素成了重要的研究课题。现欲利用图19所示的工艺流程回收废旧电池中的某些金属资源(部分条件未给出)。回答下列问题:
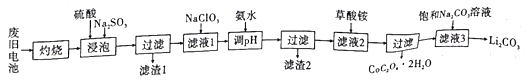
已知:①滤液1中阳离子有H+、Co2+、Fe2+、Al3+、Li+等;
②两种物质不同温度下的溶解度如下表所示:
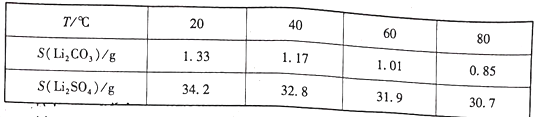
(1)钴酸锂( LiCoO2)钴元素的化合价为___________。
(2)浸泡时加入Na2SO3的主要目的是______________________;可用盐酸代替H2SO4和Na2SO3的混合液,但缺点是______________________。
(3)滤液1中加入NaClO3的主要目的是______________________(用离子方程式表示)。
(4)为了使Fe3+、Al3+沉淀完全(通常认为金属离子浓度小于或等于10-5mo·L-1时已沉淀完全)加入氨水调节pH的最小值是___________。(已知:Ksp[Fe(OH)3]=1.0×10-39,Ksp[Al(OH)3]=2.7×10-34,1g3=0.52)
(5)滤液3中加入饱和Na2CO3溶液,过滤后,需要用“热水洗涤”的原因是___________。
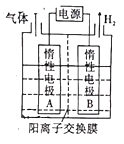
(6)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,利用如图所示的装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为___________(填化学式)溶液;阳极电极反应式为______________________;电解过程中Li+向___________(填“A”或“B”)电极迁移。
-
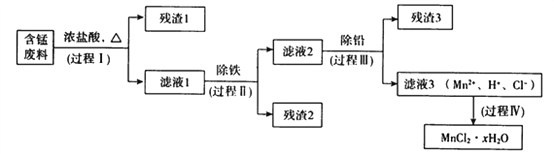
以废旧锌锰电池初步处理分选出的含锰废料(MnO2、MnOOH、MnO 及少量Fe、Pb等) 为原料制备高纯MnCl2·xH2O,实现锰的再生利用。其工作流程如下:
资料a.Mn的金属活动性强于Fe;Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
资料b.生成氢氧化物沉淀的pH
| Mn(OH)2 | Pb(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 8.1 | 6.5 | 1.9 |
| 完全沉淀时 | 10.1 | 8.5 | 3.2 |
注: 金属离子的起始浓度为0.1 mol·L-1
(1)过程Ⅰ的目的是浸出锰。经检验滤液1中含有的阳离子为Mn2+、Fe3+、Pb2+和H+。
①MnOOH 与浓盐酸反应的离子方程式是_______________________________。
②检验滤液1中只含Fe3+不含Fe2+的操作和现象是:_________________________________________。
③Fe3+由Fe2+转化而成,可能发生的反应有:
a.2Fe2++Cl2=2Fe3+2Cl-
b.4Fe2++O2+4H+=2Fe3++2H2O
c.……
写出c的离子方程式:____________________。
(2)过程Ⅱ的目的是除铁。有如下两种方法,
ⅰ.氨水法:将滤液1先稀释,再加适量10%的氨水,过滤。
ⅱ.焙烧法:将滤液1浓缩得到的固体于290℃焙烧,冷却,取焙烧物,加水溶解,过滤,再加盐酸酸化至pH 小于5.5。
已知:焙烧中发生的主要反应为2FeCl3+3O2=2Fe2O3+3Cl2,MnCl2和PbCl2不发生变化。
①氨水法除铁时,溶液pH 应控制在_____________之间。
②两种方法比较,氨水法除铁的缺点是____________。
(3)过程Ⅲ的目的是除铅。加入的试剂是____________。
(4)过程Ⅳ所得固体中的x的测定如下,取m1g样品,置于氯化氢氛围中加热至失去全部结晶水时,质量变为m2g。则x=____________。
-
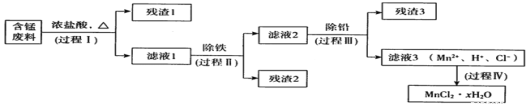
以废旧锌锰电池初步处理分选出的含锰废料(MnO2、MnOOH、MnO及少量Fe、Pb等)为原料制备高纯MnCl2·xH2O,实现锰的再生利用。其工作流程如下:
资料a:Mn的金属活动性强于Fe;Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
资料b:生成氢氧化物沉淀的pH
| Mn(OH)2 | Pb(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 8.1 | 6.5 | 1.9 |
| 完全沉淀时 | 10.1 | 8.5 | 3.2 |
注:金属离子的起始浓度为0.1 mol·L-l
(1)过程I的目的是浸出锰。经检验滤液1中含有的阳离子为Mn2+、Fe3+、Pb2+和H+。
①MnO2与浓盐酸反应的离子方程式是____________。
②检验滤液1中只含Fe3+不含Fe2+的操作和现象是:分别取两份少量滤液1于试管中,一份__________;另一份 ________________。
③Fe3+由Fe2+转化而成,可能发生的反应有:
a. 2Fe2++Cl2= 2Fe3++2Cl- b.4Fe2++O2+4H+=4Fe3++2H2O
c.…… 写出c的离子方程式:____________________。
(2)过程Ⅱ的目的是除铁。有如下两种方法:
i.氨水法:将滤液1先稀释,再加适量10%的氨水,过滤。
ii.焙烧法:将滤液l浓缩得到的固体于290℃焙烧,冷却,取焙烧物加水溶解、过滤,滤液再加盐酸酸化至合适pH。
已知:焙烧中发生的主要反应为2FeCl3+3O2 2Fe2O3+3Cl2,焙烧时MnCl2和PbCl2不发生变化。
2Fe2O3+3Cl2,焙烧时MnCl2和PbCl2不发生变化。
①氨水法除铁时,溶液pH应控制在__________之间。
②两种方法比较,氨水法除铁的缺点是____________。
(3)过程Ⅲ的目的是除铅。加入的试剂是____________。
(4)过程Ⅳ所得固体中的x的测定如下:取m1g样品,置于氮气氛围中加热至失去全部结晶水时,固体质量减轻m2g。则x=________。
















