-
锌是一种重要的过渡金属,锌及其化合物有着广泛的应用。
(1)指出锌在周期表中的位置:第________周期,第________族,________区。
(2)Zn形成金属晶体,其金属原子堆积属于下列______模式。
A.简单立方 B.钾型 C.镁型 D.铜型
(3)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式________;葡萄糖分子中碳原子的杂化方式为________。
(4)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子属于________(填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,NH3位于正四面体的顶点,试在右下图中表示[Zn(NH3)4]2+中Zn2+与NH3之间的化学键______。

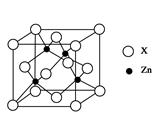
(5)下图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为______________________。该化合物晶体的熔点比干冰高得多,原因是____________________。

(6)与锌同周期,最外层有3个未成对电子的元素名称是________,该元素最高价氧化物对应水化物的酸性比溴的最高价氧化物对应水化物的酸性________(填“强”或“弱”)。
-
锌是一种过渡金属,锌及其化合物有着广泛的应用。
(1)指出锌在周期表中的位置:第________周期,第________族,________区。
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式__________________;葡萄糖分子中碳原子的杂化方式为______________。
(3)Zn2+能与NH3形成配离子[Zn(NH3)4]2+。配位体NH3分子属于________________(填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,NH3位于正四面体的顶点,则[Zn(NH3)4]2+中中心离子的杂化轨道类型是_____________。
(4)上图表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为___________________;该化合物晶体的熔点比干冰高得多,原因是______________________________________________。
(5)与锌同周期,最外层有3个未成对电子的元素名称是________________,该元素最高价氧化物对应水化物的酸性比溴的最高价氧化物对应水化物的酸性___________(填“强”或“弱”)。
-
锌是一种重要的金属,锌及其化合物有着广泛的应用.
①指出锌在周期表中的位置:第______周期,第______族,属于______区.
②葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂.写出Zn2+基态电子排布式______;葡萄糖分子中碳原子杂化方式有______.
③Zn2+能与NH3形成配离子[Zn(NH3)4]2+.配位体NH3分子属于______(填“极性分子”或“非极性分子”);在[Zn(NH3)4]2+中,Zn2+位于正四面体中心,N位于正四面体的顶点,试在图1中表示出[Zn(NH3)4]2+中Zn2+与N之间的化学键.
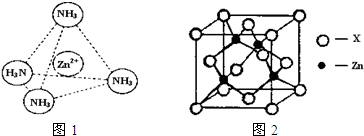
④如图2表示锌与某非金属元素X形成的化合物晶胞,其中Zn和X通过共价键结合,该化合物的化学式为______;该化合物晶体的熔点比干冰______(填写“高”或“低”),原因是______.
-
(1)锌是一种重要的金属,锌及其化合物有着广泛的应用。
①指出锌在周期表中的位置:第____ ____周期,第_____ ___族,基态Zn原子的电子排布式_____________________。
②葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。葡萄糖分子中碳原子杂化方式有________
(2)判断含氧酸强弱的一条经验规律是:含氧酸分子结构中含非羟基氧原子数越多,该含氧酸的酸性越强。含氧酸酸性强弱与非羟基氧原子数的关系如下表所示:

已知:亚磷酸(H3PO3)和亚砷酸(H3AsO3)分子式相似,但它们的酸性差别很大,H3PO3是中强酸,H3AsO3既有弱酸性又有弱碱性。由此可推出:
①H3PO3的结构式为_____________,H3PO3与过量的NaOH溶液反应的化学方程式为__________________;
②H3AsO3的结构式为_____________,在H3AsO3中加入浓盐酸,反应的化学方程式为_____________。
-
铝、铁是重要的金属,其单质及化合物有着广泛的应用,完成下列填空:
(1)铝元素在周期表中的位置是 ,写出其最高价氧化物对应水化物的电离方程式 。
(2)画出铁原子的结构示意图 。与铁同周期的主族元素中,最高价氧化物对应水化物中,碱性最强的化合物与酸性最强的化合物的化学反应方程式为 。
(3)在FeC13稀溶液中滴加KSCN溶液后呈红色,反应的离子方程式是 ;在其中加入少量KCl固体,溶液的颜色 (选填“变深”,“变浅”或“不变”)。
(4)若先往FeCl3溶液中加入足量NaF溶液,再滴加溶液,则不呈红色,若再加入足够量FeC13溶液,又会呈现红色。请试对上述实验现象作出解释 。
-
(8分)铁、铝、铜及其化合物在生产、生活中有着广泛的应用。请回答下列问题:
(1)铝元素在周期表中位置 ,铝离子的结构示意图为 。
(2)Fe3+、Al3+、Cu2+三种金属阳离子氧化性由强到弱的排列顺序是 。制造电路板的工艺中,FeCl3溶液可以蚀刻铜箔,该反应的离子方程式为 。
(3)与明矾相似,硫酸铁也可用作净水剂,但在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是 。
(4)下表中,对陈述Ⅰ、Ⅱ的正确性的判断都正确的是 (填字母序号)。
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | 铁是地壳中含量最高的金属元素 | 铁是人类最早使用的金属材料 | Ⅰ对;Ⅱ对。 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔对熔化的铝有较强的吸附作用 | Ⅰ对;Ⅱ错。 |
| C | 铝粉可以和氧化铁粉末发生铝热反应 | 铝热反应是工业炼铁最常用方法 | Ⅰ对;Ⅱ错。 |
| D | 铜在潮湿空气中表面会生成铜绿 | 可用铜容器盛放浓硫酸 | Ⅰ对;Ⅱ对。 |
(5)某校兴趣小组为测定一种铁铝硅合金(FexAlySiz)粉末的组成,提出如下方案:准确称取1.46 g该合金粉末,加入过量盐酸,充分反应后过滤,测得剩余固体的质量为0.07 g。向滤液中滴加足量NaOH浓溶液,充分搅拌、过滤、洗涤得到固体。再将所得固体充分加热、灼烧,得到红棕色粉末1.60 g。通过计算确定此合金的组成为________(填化学式)。
-
镁合金及镁的化合物在生产、生活中有着广泛的应用。
(1)镁在元素周期表中的位置是__________________。
(2)用水氯镁石(主要成分为MgCl2·6H2O)制备金属镁的关键流程如下:

该工艺中可循环使用的物质有______________。
(3)储氢材料Mg(AlH4)2在110~200 ℃的反应为Mg(AlH4)2=MgH2+2Al+3H2↑,每转移6 mol电子生成氢气的物质的量为________mol。
(4)碱式碳酸镁密度小,是橡胶制品的优良填料,可用复盐MgCO3·(NH4)2CO3·2H2O作原料制备。制备过程中,需要用到卤水(氯化镁溶液)。某科研小组用沉淀滴定法分析产品中Cl-的含量,称取6.100 0 g产品用适量硝酸溶解,经稀释等步骤最终配得500 mL的溶液。
a.准确量取25.00 mL 待测液,用0.100 0 mol/L AgNO3标准液滴定,滴定前后滴定管中的液面读数如图所示,则滴定过程中消耗标准液的体积为________mL。
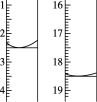
b.
| AgCl | AgBr | AgI | Ag2CrO4 |
| Ksp | 2×10-10 | 5.4×10-13 | 8.3×10-17 | 2×10-12 |
| 颜色 | 白 | 淡黄 | 黄 | 砖红 |
参照上表数据及信息分析,滴定时可以作指示剂的是________(填数字序号)。
①CaCl2 ②NaBr ③NaI ④K2CrO4
-
前四周期的元素及其化合物在生产、生活、化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)写出基态Ti原子的电子排布式_________________,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有______种。
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+ 易被氧化成Fe3+的原因是_______。
(3)SCN-离子可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S)。
①写出与SCN-互为等电子体的一种微粒_______________(分子或离子);
②硫氰酸分子中π键和σ键的个数之比为___________;
(4)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是 ______ (填元素符号)
| 元素 | 氟 | 氯 | 溴 | 碘 |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
②根据价层电子对互斥理论,预测ClO4-的空间构型为_______形,C1O2- 中Cl原子的杂化方式为_________。
③元素C、O、F、H的电负性由大到小的顺序为______________________。
-
铁、铜及其化合物在日常生产、生活有着广泛的应用。请回答下列问题:
(1)铁在元素周期表中的位置是________________。
(2)配合物Fe(CO)x常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于___________(填晶体类型)。Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=_______;Fe(CO)x在一定条件下发生反应:Fe(CO)x(s) Fe(s)+xCO(g)。已知反应过程中只断裂配位键,由此判断该反应所形成的化学键类型为_________。
Fe(s)+xCO(g)。已知反应过程中只断裂配位键,由此判断该反应所形成的化学键类型为_________。
(3)写出CO的一种常见等电子体分子的结构式____________;两者相比较沸点较高的为__________(填化学式)。CN-中碳原子杂化轨道类型为__________,C、N、O三元素的第一电离能最大的为_______(用元素符号表示)。
(4)铜与Cl形成化合物的晶胞如图所示(黑点代表铜原子)。
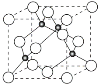
①该晶体的化学式为________。它可与浓盐酸发生非氧化还原反应,生成配合物H2CuCl3,反应的化学方程式为___________________。
②已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于______(填“离子”、“共价”)化合物。
-
Co、Ni的化合物在生产生活中有着广泛的应用。
(1) 元素在周期表中的位置是4周期,_________族。基态Co原子的电子排布式为____________。
元素在周期表中的位置是4周期,_________族。基态Co原子的电子排布式为____________。
(2)乙二胺NH2-CH2-CH2-NH2(缩写符号en)中N原子的杂化方式为________杂化。en可以与Co形成配合物[Co(en)2Cl2]Cl·HCl·2H2O,配离子结构如下图所示,中心离子的配位数为________,配合物晶体中可能存在的作用力有___________。
A、离子键 B、极性共价键 C、非极性共价键 D、配位键 E、氢键
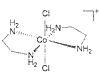
(3)NiO晶体结构如图1所示,其中离子坐标参数A为(0,0,0),B为( ),则C离子(面心处)坐标参数为_______________。
),则C离子(面心处)坐标参数为_______________。
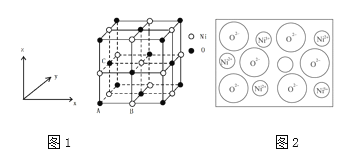
(4)天然氧化镍晶体中总是存在晶体缺陷,如图2所示。NiXO晶体中x值为 ,若晶体中的Ni分别为
,若晶体中的Ni分别为 、
、 ,此晶体中
,此晶体中 与
与 的最简整数比为______。
的最简整数比为______。









