-
Cu、Fe、Se、Co、S、P等元素常用于化工材料的合成。请回答下列问题:
(1)Fe3+最外层电子排布式为___________,其核外共有_____种不同运动状态的电子。Fe3+比Fe2+更稳定的原因是_______________________________________。
(2)硒为第四周期元素,相邻的元素有砷和溴,则三种元素的电负性从大到小的顺序为_________________(用元素符号表示),SeO2分子的空间构型为___________________。
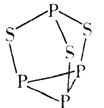
(3)P4S3可用于制造火柴,其分子结构如图所示。P4S3分子中硫原子的杂化轨道类型为__________,每个P4S3分子中含孤电子对的数目为_______________。
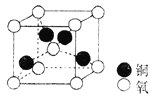
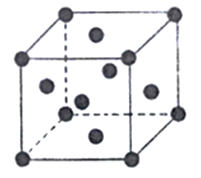
(4)铜的某种氧化物晶胞结构如图所示,若该晶胞的边长为a cm,则该氧化物的密度为________g·cm-3。(设阿伏加德罗常数的值为NA)。
-
Cu、Fe、Se、Co、S、P等元素常用于化工材料的合成。请回答下列问题:
(1)Fe3+最外层电子排布式为___________,其核外共有_____种不同运动状态的电子。Fe3+比Fe2+更稳定的原因是_______________________________________。
(2)硒为第四周期元素,相邻的元素有砷和溴,则三种元素的电负性从大到小的顺序为_________________(用元素符号表示),SeO2分子的空间构型为___________________。
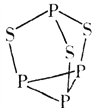
(3)P4S3可用于制造火柴,其分子结构如图所示。P4S3分子中硫原子的杂化轨道类型为__________,每个P4S3分子中含孤电子对的数目为_______________。
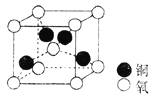
(4)铜的某种氧化物晶胞结构如图所示,若该晶胞的边长为a cm,则该氧化物的密度为________g·cm-3。(设阿伏加德罗常数的值为NA)。
-
Cu、Fe、Se、Co、Si常用于化工材料的合成。请回答下列问题:
(1)铁离子(Fe3+)最外层电子排布式为______,其核外共有______种不同运动状态的电子。Fe3+比Fe2+更稳定的原因是____________________________________。
(2)硒为第四周期元素,相邻的元素有砷和溴,则三种元素的电负性从大到小的顺序为________(用元素符号表示)。
(3)Na3[Co(NO2)6]常用作检验K+的试剂,在[Co(NO2)6]3-中存在的化学键有____、_____。
(4)C与N能形成一种有毒离子CN-,能结合Fe3+形成配合物,写出一个与该离子互为等电子体的极性分子的分子式_____,HCN分子的空间构型为____________。
(5)单晶硅的结构与金刚石的结构相似,若将金刚石晶体中一半的C原子换成Si原子且同种原子间不成键,则得如图所示的金刚砂(SiC)结构。

在SiC晶体中,C原子的杂化方式为_________,每个Si原子被_______个最小环所共有。
(6)已知Cu的晶胞结构如图,棱长为acm,又知Cu的密度为pg/cm3,则用a、p的代数式表示阿伏伽德罗常数为____mol-1。
-
 、
、 、
、 、
、 、S、P等元素常用于化工材料的合成。回答下列问题:
、S、P等元素常用于化工材料的合成。回答下列问题:
(1)钴原子的基态电子排布式为_______________________。
(2) 有________几种不同的运动状态的电子,
有________几种不同的运动状态的电子, 比
比 更稳定的原因是_________。
更稳定的原因是_________。
(3)硒为第四周期元素,相邻元素有砷和溴,则三种元素的电负性从大到小的顺序为_________(用元素符号表示)。
(4) 的熔点为340℃,加热易升华,固体
的熔点为340℃,加热易升华,固体 属于______晶体。
属于______晶体。 的空间构型为_____。
的空间构型为_____。
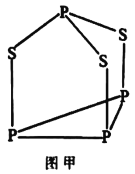
(5)  可用于制造火柴,其分子结构如图甲所示。
可用于制造火柴,其分子结构如图甲所示。 分子中S的杂化方式为______。每个
分子中S的杂化方式为______。每个 分子中含有的孤电子对的数目为_________。
分子中含有的孤电子对的数目为_________。
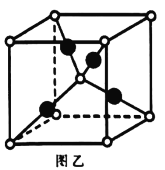
(6)铜的某种氧化物晶胞结构如图乙所示,该氧化物的化学式为____________。若该晶胞的边长为 ,阿伏加德罗常数值为
,阿伏加德罗常数值为 ,则该氧化物的密度为_________
,则该氧化物的密度为_________
-
铅及其化合物可用于蓄电池、耐酸设备及X射线防护材料等。回答下列问题:
(1)铅是碳的同族元素,比碳多4个电子层,铅在元素周期表的位置为______ ____,Fe3O4可写成FeO·Fe2O3的形式,如果将Pb3O4也写成相对应的形式应为:______________
(2)PbO2与浓盐酸共热生成黄绿色气体,反应的化学方程式为___________________。PbO2可由PbO与次氯酸钠溶液反应制得,其反应的离子方程式为______________。
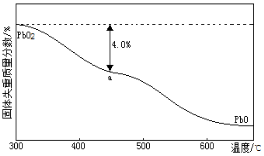
(3)PbO2在加热过程发生分解的失重曲线如右图所示,已知失重曲线上的a点为样品失重4.0%(即 ×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n_______________,____________。
×100%)的残留固体,若a点固体组成表示为PbOx或mPbO2·nPbO,计算x值和m︰n_______________,____________。
-
氰化钠(NaCN)是重要的化工原料,常用于化学合成、冶金工业等。回答下列问题:
(1)下列标志中,应贴在装有氰化钠容器上的是 。

(2)写出NaCN的电子式 。
(3)可用纯碱、焦炭、氨气反应制取NaCN,写出反应的化学方程式,并用单线桥标明电子转移的方向和数目 。
(4)现代采金技术先以NaCN溶液在自然环境中浸取粉碎的含金(Au)矿石,得到Na[Au(CN)2](二氰合金酸钠)溶液,再用锌还原Na[ Au(CN)2]生成金。“浸取”反应的氧化剂是 ,消耗的锌与生成的金的物质的量之比为 。
(5)工业利用NaCN制备蓝色染料的流程如下:
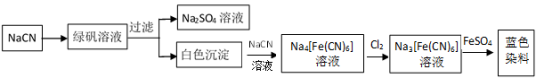
通入Cl2时发生反应的离子方程式为_ _,该蓝色染料的化学式为 。
-
含镁、氮、磷、砷等元素的化合物在化工生产、药物化学及催化化学等领域应用广泛。回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是_____(填序号)。
A.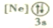 B.
B.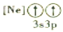 C.
C.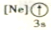 D.
D.
(2)晶格能又叫点阵能。它是1mol 离子化合物中的正、负离子从相互分离的气态结合成离子晶体时所放出的能量。MgO 晶格能可通过如图所示的Borm Haber循环计算得到。
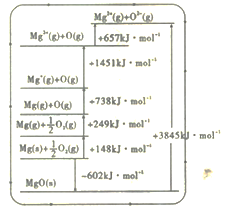
Mg的第二电离能为______kJ·mol-1;MgO的晶格能为___________kJ·mol-1。
(3)乙二胺(H2NCH2CH2NH2) 是一种有机化合物,其中N原子的杂化类型是____,该有机化合物能与Mg2+、Cu2+等金属离子形成稳定环状离子,其原因是______,其中与乙二胺形成的化合物稳定性相对较高的是_______(填 “Mg2+ ”或“Cu2+” )。
(4) PCl5是一种白色固体,加热到160°C不经过液态阶段就变成蒸气,测得180°C下的蒸气密度(折合成标准状况)为9.3g·L-1,分子的极性为零,P-Cl键长为204pm和211pm两种。在180°C下PCl5蒸气中存在的分子形式为____(填化学式),分子的空间构型为______,P、Cl的电负性由大到小顺序为________。
(5)砷和铟组成的一种化合物属于半导体材料,其晶胞结构如图所示。已知晶胞的参数为a pm,阿伏加德罗常数的值为NA,则该晶体的密度为_____g. cm-3 (用含a和NA的代数式表示)。
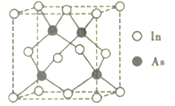
-
氰化钠(NaCN)是重要的化工原料,常用于化学合成、冶金工业等.回答下列问题:
(1)可用纯碱、焦炭、氨气反应制取 NaCN,同时还有水生成,写出反应的化学方程式,并标明电子转移的方向和数目______________;
(2)现代采金技术先以NaCN溶液在自然环境中浸取粉碎的含金(Au)矿石,得到 Na[Au(CN)2](二氰合金酸钠)溶液,再用锌还原 Na[Au(CN)2]生成金,“浸取”反应的还原产物是______________;
(3)下图为用含NaCN的废水合成黄血盐(K4Fe(CN)6)的主要工艺流程如图:
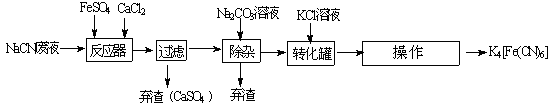
已知相同温度下溶解度:Na4Fe(CN)6>K4Fe(CN)6
① 实验室用NaCN固体配制NaCN溶液时,应先将其溶于______________溶液,再用蒸馏水稀释。
②在转化罐中发生反应的化学方程式为______________。
③加入碳酸钠溶液主要目的是______________。
④“操作”环节具体为______________。
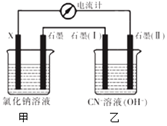
(4)CN -可以造成水体污染,某小组用如下方法对此污水进行处理如下图装置模拟电化学法处理CN -,有关结果见表.
| 实验序号 | 电极(X) | NaCl溶液浓度(mol/L) | 甲中石墨表面通人气体 | 电流计读数(A) |
| (1) | Fe | 0.l | 空气 | I |
| (2) | Al | 0.1 | 空气 | 1.5Ⅰ |
| (3) | Fe | 0.1 | 02 | 2Ⅰ |
| (4) | Al | 0.5 | 空气 | 1.6Ⅰ |
①若乙池中石墨(I)极产生无毒无害的物质,其电极反应式为___________;
②该实验表明电化学法处理CN -时,影响处理速率的因素有___________、___________(任答两点)
-
氰化钠(NaCN)是重要的化工原料,常用于化学合成、冶金工业等。回答下列问题:
(1)下列标志中,应贴在装有氰化钠容器上的是____________

(2)写出NaCN的电子式____________。
(3)可用纯碱、焦炭、氨气反应制取NaCN,写出反应的化学方程式,并用单线桥标明电子转移的方向和数目 。
(4)现代采金技术先以NaCN溶液在自然环境中浸取粉碎的含金(Au)矿石,得到Na[Au(CN)2](二氰合金酸钠)溶液,再用锌还原Na[ Au(CN)2]生成金。“浸取”反应的氧化剂是 ,消耗的锌与生成的金的物质的量之比为 。
(5)工业利用NaCN制备蓝色染料的流程如下:
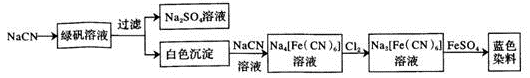
通入Cl2时发生反应的离子方程式为_ _,该蓝色染料的化学式为 。
(6)常温下HCN的电离常数Ka=6.2×10-10,浓度均为0.5mol/L的NaCN和HCN的混合溶液显 (填“酸”、“碱”或“中”)性,通过计算说明其原因 。
-
硫和钙的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)基态Ca原子中,核外电子占据最高能层的符号是________,该能层为次外层时最多可以容纳的电子数为_________。元素Ca和S相比,第一电离能较大的是______(填元素符号)。
(2)钙元素的焰色反应呈砖红色,其中红色对应的辐射与钾元素的焰色反应对应颜色的辐射波长,较短的是_______(填元素符号)。
(3)H2S和H2O分子构型都为V形,中心原子的杂化形式都是______,但H2O分子键角大于H2S分子,原因是________________________________________________________。
(4)钙元素和锰元素属于同一周期,且核外最外层电子构型相同,但金属钙的熔点、沸点等都比金属锰低,原因是______________________________________。
(5)Ca、Mn、Mg的氧化物和硫化物都是NaCl型结构的离子晶体,其中阴离子采用面心立方最密堆积方式,X射线衍射实验测得它们的晶胞参数如下表:
| 氧化物晶体 | MgO | MnO | CaO |
| a/nm | 0.421 | 0.444 | 0.480 |
| 硫化物晶体 | MgS | MnS | CaS |
| a/nm | 0.520 | 0.520 | 0.568 |
由表可知:r(S2-)_______r(O2-)(填“>”或“<”),r(Mg2+)、r(Ca2+)、r(Mn2+)由大到小的的顺序是____________________________,r(S2- )为_____nm,r(Ca2+)为_____nm。











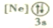 B.
B.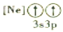 C.
C.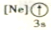 D.
D.





