下图是某工厂对海水资源综合利用的示意图,下列说法错误的是
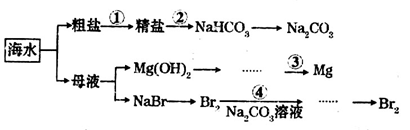
A.第①步中除去粗盐中的,依次加入的物质可以是
溶液、
溶液和盐酸
B.第②步发生的化学反应为:
C.第③步工业上电解熔融的Mg(OH)2冶炼金属Mg
D.第④步用Na2CO3溶液吸收Br2过程中,既有溴元素被氧化也有溴元素被还原
高三化学选择题中等难度题
下图是某工厂对海水资源综合利用的示意图,下列说法错误的是

A.第①步中除去粗盐中的,依次加入的物质可以是
溶液、
溶液和盐酸
B.第②步发生的化学反应为:
C.第③步工业上电解熔融的Mg(OH)2冶炼金属Mg
D.第④步用Na2CO3溶液吸收Br2过程中,既有溴元素被氧化也有溴元素被还原
高三化学选择题中等难度题
下图是某工厂对海水资源综合利用的示意图,下列说法错误的是

A.第①步中除去粗盐中的,依次加入的物质可以是
溶液、
溶液和盐酸
B.第②步发生的化学反应为:
C.第③步工业上电解熔融的Mg(OH)2冶炼金属Mg
D.第④步用Na2CO3溶液吸收Br2过程中,既有溴元素被氧化也有溴元素被还原
高三化学选择题中等难度题查看答案及解析
海水中蕴含丰富的资源,对海水进行综合利用,可制备一系列物质(见下图),下列说法正确的是
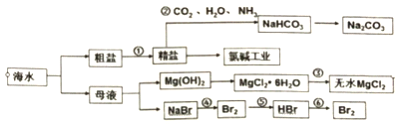
A. 步骤①中,除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→盐酸→过滤
B. 步骤②中反应利用的原理是:相同条件下NaHCO3的溶解度比NaCl小
C. 步骤③可将MgCl2·6H2O晶体在空气中直接加热脱水
D. 步骤④、⑤、⑥溴元素均被氧化
高三化学选择题困难题查看答案及解析
海水中蕴藏着丰富的资源,海水综合利用的示意图如下,下列说法正确的是( )
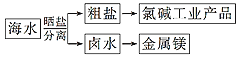
①通过氯碱工业可生产的产品有NaOH、NaClO、盐酸等
②除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤→盐酸
③可将MgCl2·6H2O晶体在空气中直接加热脱水得到较纯净的无水MgCl2
④电解MgCl2溶液可制取金属镁
A.①③ B.②④ C.③④ D.①②
高三化学单选题简单题查看答案及解析
高三化学解答题中等难度题查看答案及解析
海水中蕴藏着丰富的资源。海水综合利用的示意图如下。
下列说法正确的是
A.通过氯碱工业可生产的产品有NaOH、NaClO、盐酸等
B.将卤水中Mg2+转化为氢氧化镁沉淀通常是向卤水加入氢氧化钠溶液
C.直接加热MgCl2·6H2O可得到较纯净的无水MgCl2
D.在高温下用铝还原MgCl2可制取金属镁
高三化学选择题简单题查看答案及解析
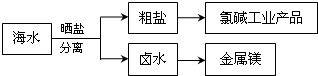
根据如图海水综合利用的工业流程图,判断下列说法正确的是( )

A.除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→Na2CO3溶液→BaCl2溶液→过滤后加盐酸
B.在过程④中SO2被氧化
C.从第③步到第⑤步的目的是为了浓缩
D.从能量转换角度看,氯碱工业中的电解饱和食盐水是一个将化学能转化为电能的过程
高三化学选择题中等难度题查看答案及解析
根据海水综合利用的工业流程图,判断下列说法不正确的是( )
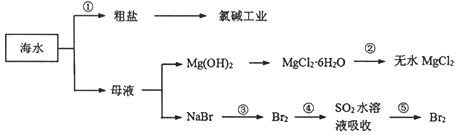
A. 除去粗盐中杂质(Mg2+、SO42-、Ca2+),加入的药品顺序为:NaOH溶液→BaCl2溶液→Na2CO3溶液→过滤后加盐酸
B. 在过程②中将MgCl2·6H2O灼烧即可制得无水MgCl2
C. 从能量转换角度看,氯碱工业电解饱和食盐水是一个将电能转化为化学能的过程
D. 从第④步到第⑤步的目的是富集Br2
高三化学单选题中等难度题查看答案及解析
海水是一种丰富的资源,工业上从海水中可提取许多种物质,广泛应用于生活、生产、科技等方面。下图是某工厂对海水资源进行综合利用的示意图。
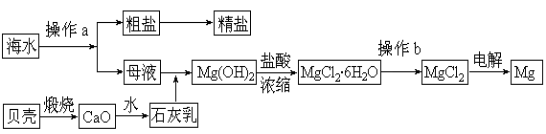
回答下列问题:
(1)流程图中操作a的名称为 。
(2)工业上从海水中提取的NaCl,可用来制取纯碱,其简要过程如下:向饱和食盐水中先通入气体A,后通入气体B,充分反应后过滤得到晶体C和滤液D,将晶体C灼烧即可制得纯碱。
①已知气体A、B是CO2或NH3,则气体A应是 (填化学式)。
②灼烧晶体C的反应方程式为 。
③滤液D中主要含有NH4Cl、NaHCO3等物质,工业上是向滤液D中通入NH3,并加入细小食盐颗粒,冷却后,可析出不含有NaHCO3的副产品NH4Cl晶体,则通入NH3的作用是 。
(3)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
① 若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是: 。
② 通过操作b获得无水MgCl2是在 氛围中进行,若直接在空气中加热,则会生成Mg(OH)Cl,写出有关反应的化学方程式: 。
高三化学填空题极难题查看答案及解析
高三化学选择题中等难度题查看答案及解析
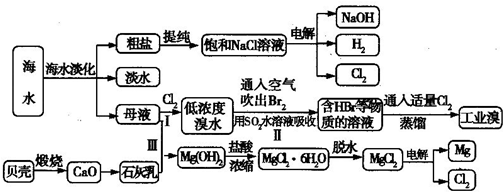
海水是巨大的资源宝库,人类可以从海水中提取各种化工产品。下图是某工厂对海水综合利用的示意图:
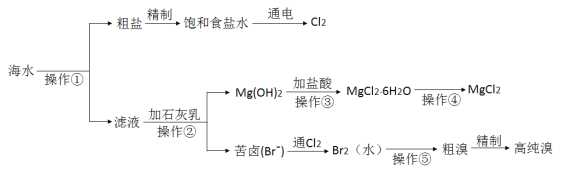
完成下列填空:
(1)写出电解饱和食盐水的化学方程式_____________,检验氯气生成的方法是_________。
(2)液氯储存在钢瓶中,钢瓶上应贴的标签为_________________(选填编号)。
a.自燃品 b.爆炸品 c.有毒品 d.易燃品
(3)Mg(OH)2加入盐酸充分反应后,操作③ 是从MgCl2溶液中获得MgCl26H2O晶体,此处需要进行的实验操作依次为____________________________。
(4)操作④是加热MgCl26H2O获得MgCl2,简述其实验操作及其原因________________。
(5)操作⑤是向溶液中鼓入__________,即可将溴单质从溶液中分离出来,此方法的成功应用是基于溴单质有____________性。
(6)粗溴的精制过程是先将粗溴用SO2水溶液吸收,将其转变成Br¯,再通Cl2,最后蒸馏得到高纯溴。用SO2水溶液吸收Br2的吸收率可达95%,有关反应的离子方程式为_________。由此反应可知,除环境保护外,在工业生产中应解决的主要问题是________________________。
高三化学工业流程困难题查看答案及解析