-
下列说法正确的是
A.0.1mol/L醋酸溶液加水稀释,电离平衡正移,电离平衡常数增大
B.0.1mol/L醋酸溶液中加入锌粒,电离平衡正移,c(H+)增大
C.0.1mol/L醋酸钠溶液中加入醋酸钠固体,水解平衡正移,c(OH-)增大
D.在AgCl饱和溶液中加入AgCl固体,沉淀溶解平衡正移,c(Ag+)增大
高二化学选择题中等难度题查看答案及解析
-
25℃时,甲为0.1mol/L的醋酸溶液,乙为0.5mol/L的醋酸溶液。下列说法正确的是
A. 溶液的导电能力:甲=乙 B. 醋酸的电离转化率:甲 >乙
C. 对水的电离的抑制程度:甲 >乙 D. c(CH3COO-):甲>乙
高二化学单选题中等难度题查看答案及解析
-
室温下,甲溶液中水电离出的H+浓度为10-12 mol•L-1,乙溶液中水电离出的H+浓度为10-2 mol•L-1,下列说法中正确的是( )
A.甲、乙两溶液的pH不可能相同
B.甲、乙两种溶液中加入Al粉都会产生H2
C.HCO3- 不可能在甲、乙两溶液中大量共存
D.甲不可能是盐溶液,乙不可能是酸或碱溶液高二化学选择题中等难度题查看答案及解析
-
常温下,向20 mL 0.1 mol·L−1的HA溶液中逐滴加入0.1mol·L−1的NaOH溶液,溶液中水所电离的c水(H+)随加入NaOH溶液体积的变化如图所示,下列说法正确的是
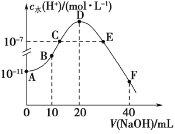
A.HA的电离常数Ka约为1×10−5
B.B点的溶液中粒子浓度满足关系:c(HA)>c(Na+)>c(A−)
C.C、E两点因为对水的电离的抑制作用和促进作用相同,所以溶液均呈中性
D.F点的溶液呈碱性,粒子浓度满足关系c(OH−)=c(HA)+c(A−)+c(H+)
高二化学单选题中等难度题查看答案及解析
-
在相同温度下,0.01mol/L的NaOH溶液和0.01mol/L的盐酸相比较,下列说法正确的是( )
A.两溶液的pH之和等于14
B.由水电离出的c(H+)都是1.0×10-12mol/L
C.由水电离出的c(OH-)相等
D.若将0.01mol/L的盐酸换成同浓度的醋酸,对水的电离的影响不变
高二化学单选题简单题查看答案及解析
-
常温下,甲溶液中水电离出的H+浓度为10-12 mol/L,乙溶液中水电离出的H+浓度为
10-2mol/L,下列说法正确的是
A.甲、乙两溶液的pH不可能相同
B.甲、乙两种溶液中加入Al粉都一定会产生H2
C.HCO3-不可能在甲、乙两溶液中大量共存
D.甲不可能是盐溶液,乙不可能是酸或碱溶液
高二化学选择题中等难度题查看答案及解析
-
常温时,0.01 mol·L-1某一元弱酸的电离常数Ka=10-6,则下列说法正确的是
A.上述弱酸溶液的pH=4
B.加入NaOH溶液后,弱酸的电离平衡向右移动,K值增大
C.加入等体积0.01 mol·L-1 NaOH溶液后,所得溶液的pH=7
D.加入等体积0.01 mol·L-1 NaOH溶液后,所得溶液的pH<7
高二化学选择题中等难度题查看答案及解析
-
下列说法正确的是( )
A.50℃时,水在0.1mol/L盐酸中与在0.1mol/LNaOH溶液中的电离程度相同
B.pH等于7的溶液一定呈中性
C.水的离子积表示在水溶液中由水电离出的H+和OH-浓度符合Kw=c(H+)·c(OH-)
D.将0.06mol·L-1氢氧化钡溶液与0.1mol·L-1盐酸溶液等体积混合,该混合溶液的pH等于13(忽略混合过程中溶液体积变化)
高二化学单选题中等难度题查看答案及解析
-
现有常温下的四份溶液:①0.01mol/LCH3COOH ②0.01mol/LHCl ③pH=12的氨水 ④pH=12的 NaOH溶液下列说法正确的是
A.。①中水电离程度最小,③中水电离程度最大
B.将②③混合,若pH=7,则消耗溶液的体积:②﹥③
C.将四份溶液稀释相同倍数后,溶液的pH:③﹥④,②﹥①
D.将①、④混合,若有c(CH3COO-)﹥c(H+),则混合液一定呈碱性
高二化学选择题简单题查看答案及解析
-
现有常温下的四份溶液:①0.01mol/LCH3COOH ②0.01mol/LHCl ③pH=12的氨水 ④pH=12的 NaOH溶液下列说法正确的是
A.①中水电离程度最小,③中水电离程度最大
B.将②③混合,若pH=7,则消耗溶液的体积:②﹥③
C.将四份溶液稀释相同倍数后,溶液的pH:③﹥④,②﹥①
D.将①、④混合,若有c(CH3COO-)﹥c(H+),则混合液一定呈碱性
高二化学选择题简单题查看答案及解析