-
牙釉质的主要成分羟基磷灰石[Ca10(PO4)6(OH)2]在水中能极少溶解Ca10(PO4)6(OH)2(s)⇌10Ca2+(aq)+6PO43-(aq)+2OH-(aq),已知25℃时Ksp[Ca10(PO4)6(OH)2]=2.35×10-59,Ksp[Ca10(PO4)6F2]=7.1×10-61,Ksp[CaCO3]=5×10-9,Ksp[CaF2]=4×10-11,下列说法不正确是( )
A.口腔内残留食物会发酵使口腔呈酸性,所以饭后、睡前应该要漱口
B.饮用水中氟元素含量较低的地区使用含氟牙膏可有效防止龋齿
C.25℃时饱和CaCO3溶液和饱和CaF2溶液相比,后者c(Ca2+)较大
D.25℃时,在CaCO3悬浊液中加入NaF溶液后,CaCO3不可能转化为CaF2高三化学选择题中等难度题查看答案及解析
-
牙釉质的主要成分羟基磷灰石[Ca10(PO4)6(OH)2]在水中能极少溶解Ca10(PO4)6(OH)2(s)
10Ca2+(aq)+6PO43-(aq)+2OH-(aq),已知25℃时Ksp[Ca10(PO4)6(OH)2]=2.35
10-59, Ksp[Ca10(PO4)6F2]=7.1
10-61,Ksp[CaCO3]=5
10-9,Ksp[CaF2]=4
10-11,下列说法不正确是( )
A.口腔内残留食物会发酵使口腔呈酸性,所以饭后、睡前应该要漱口
B.饮用水中氟元素含量较低的地区使用含氟牙膏可有效防止龋齿
C.25℃时饱和CaCO3溶液和饱和CaF2溶液相比,后者c(Ca2+)较大
D.25℃时,在CaCO3悬浊液中加入NaF溶液后,CaCO3不可能转化为CaF2
高三化学选择题中等难度题查看答案及解析
-
碱式磷酸钙Ca10(PO4)6(OH)2]又名羟基磷酸钙,工业上叫羟基磷酸钙,工业上叫羟基磷灰石或羟磷灰石,是人的牙齿中比较坚硬的物质(排第二),也是骨骼的主要组成成分·在水中有微弱的溶解,这是牙齿损坏的主要原因。氟磷酸钙也称氟磷灰石,它的化学式为Ca10(PO4)6F2,是牙表面牙釉的主要成分。回答下列问题
(1)基态钙原子的价层电子接布式为__。基态磷原子的未成对电子数为____
(2)碱式磷酸钙中含氧酸根离子中的中心原子的杂化类型是___________,含氧酸根离子的空间构型为_______
(3)氢氟酸溶液中存在:2HF
H2F2,H2F2为一元酸,则氢氟酸溶液中含氟阴离子是____,(填离子符号)。氢氟酸中存在H2F2的原因是__.与H2F+互为等电子体的分子是__(写出一个即可)。
(4)O、F、P的电负性由小到大的顺序为_________
(5)NH3和PH3的构型相似,NH3的键角略大于PH。从原子结构角度解释其原因:_______
(6)CaF2晶胞如图所示。位于体内的粒子的配位数为______
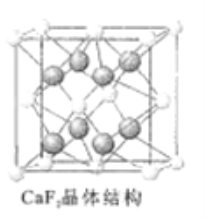
已知:氟化钙晶体密度为ρg/cm3,NA代表阿伏加德罗常数的值。氟化钙品体中Ca2+和F-之间最近核间距(d)为_________________pm(只要求列出CaF2晶体结构计算式即可)。
高三化学综合题中等难度题查看答案及解析
-
碱式磷酸钙[Ca10(PO4)6(OH)2],工业上叫羟基磷灰石或羟磷灰石,是人的牙齿中比较坚硬的物质,在水中有微弱的溶解,这是牙齿损坏的主要原因。氟磷酸钙也称氟磷灰石,它的化学式为Ca10(PO4)6F2,是牙表面牙釉的主要成分。
回答下列问题:
(1)基态钙原子的价层电子排布式为____________。基态磷原子的未成对电子数为______________。
(2)碱式磷酸钙中含氧酸根离子的中心原子杂化类型是______________________,含氧酸根离子的空间构型为______________;
(3)氢氟酸溶液中存在:2HF
H2F2,H2F2为一元酸,则氢氟酸溶液中含氟阴离子是______________(填离子符号)。氢氟酸中存在H2F2的原因是______________________________________________。与H2F+互为等电子体的分子是________________(写出一个即可)。
(4)O、F、P的电负性由小到大的顺序为______________。
(5)NH3和PH3的构型相似,NH3的键角略大于PH3 ,从原子结构角度解释其原因:________________。
(6)CaF2晶胞如图所示。位于体内的粒子的配位数为______________。

已知:氟化钙晶体密度为ρg·cm-3,NA代表阿伏加德罗常数的值。
氟化钙晶体中Ca2+和F-之间最近核间距(d)为______________pm(只要求列出计算式即可)。
高三化学综合题困难题查看答案及解析
-
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛。
(1)氯元素同族的下一周期元素的原子结构示意图为_______,碘是______(填颜色)固体物质。(2)牙齿的损坏实际上是牙釉质羟基磷灰石[Ca5(PO4)3OH]溶解的结果,糖沾附在牙齿上,在酶的作用下产生酸性物质,易造成龋齿。使用含氟牙膏会保护牙齿,因为氟离子会跟羟基磷灰石[Ca5(PO4)3OH]发生反应生成氟磷灰石,氟磷灰石比羟基磷灰石更能抵抗酸的侵蚀氟,用离子方程式表示这一过程_________________________________________。此外氟离子还能抑制口腔细菌产生酸,含氟牙膏已经普遍使用。
(3)碘被称为“智力元素”,碘酸钾(KIO3)是国家规定的食盐加碘剂,它的晶体为白色,可溶于水。碘酸钾在酸性介质中与碘化钾生成单质碘。写出该反应的离子方程式_________________。
(4)①电解装置如图所示,电解槽内装有KI及淀粉溶液,中间用阴离子交换膜隔开。在一定的电压下通电,发现左侧溶液变蓝色,一段时间后,蓝色逐渐变浅。
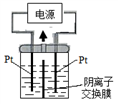
已知:3I2+6OH—==IO3—+5I—+3H2O
下列说法正确的是(____)
A.右侧发生的电极方程式:2H2O+2e—==H2↑+2OH—
B.电解结束时,右侧溶液中含有IO3—
C.电解槽内发生反应的总化学方程式KI+3H2O==KIO3+3H2↑(条件通电)
D.如果用阳离子交换膜代替阴离子交换膜,电解槽内发生的总化学方程式会改变
②电解完毕,从电解液中得到碘酸钾晶体的实验过程如下:

步骤⑤的操作名称____________________
(5)已知:I2+2
=
+2I-。溶度积常数Ksp(CuCl)=1.7×10-7 Ksp( CuI)=1.3×10-12用“间接碘量法”测定含有CuCl2•2H2O晶体的试样(不含能与I―发生反应的氧化性杂质)的纯度,过程如下:取a g试样溶于水,加入过量KI固体,充分反应,生成白色沉淀。用c mol/L Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液b mL。
①可选用___________作滴定指示剂,滴定终点的现象是_________________。
②CuCl2溶液与KI反应的离子方程式为______________________________。
③该试样中CuCl2•2H2O的质量百分数为___________________________。
高三化学简答题困难题查看答案及解析
-
(12分)羟基磷灰石(化学式为Ca10(PO4)6(OH)2,简称HA)是一种重要的生物材料。用磷酸与氢氧化钙制备HA的流程如下:

(1)配制石灰乳时,用广泛pH试纸测定溶液的pH值,操作方法是________。
(2)步骤②中适宜的加热方法是________。
(3)步骤②、③中必须充分搅拌,其目的是
________。
(4)步骤④中需将生成的白色胶状沉淀过滤,再用蒸馏水洗涤数次,洗涤的目的是________。
(5)实验②中滴入磷酸时,pH随“磷酸的用量与理论量比值”(用K表示)的变化如右图,需要严格控制滴定速率的阶段是________。(用K的范围表示)

(6)氢氧化钙与磷酸中和生成HA的化学方程式是________。
高三化学实验题简单题查看答案及解析
-
(3分)牙齿的损坏实际是牙釉质[Ca5(PO4)3OH]溶解的结果,在口腔中存在如下平衡:Ca5(PO4)3OH
5Ca2+ +3PO43― +OH―当糖附在牙齿上发酵时会产生H+,试运用化学平衡理论说明经常吃糖对牙齿的影响。
高三化学填空题困难题查看答案及解析
-
(1)(广东)由磷灰石[主要成分Ca5(PO4)3F]在高温下制备黄磷(P4)的热化学方程式为:4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)===3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) ΔH
①上述反应中,副产物矿渣可用来________。
②已知相同条件下:
4Ca5(PO4)3F(s)+3SiO2(s)===6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) ΔH1
2Ca3(PO4)2(s)+10C(s)===P4(g)+6CaO(s)+10CO(g) ΔH2
SiO2(s)+CaO(s)===CaSiO3(s) ΔH3
用ΔH1、ΔH2和ΔH3表示ΔH,ΔH=____________。
(2)(江苏)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)===Cu2+(aq)+H2(g) ΔH1=+64.39 kJ·mol-1
②2H2O2(l)===2H2O(l)+O2(g) ΔH2=-196.46 kJ·mol-1
③H2(g)+
O2(g)===H2O(l) ΔH3=-285.84 kJ·mol-1
在H2SO4溶液中,Cu与H2O2反应生成Cu2+和H2O的热化学方程式为______。
高三化学填空题中等难度题查看答案及解析
-
(1)由磷灰石[主要成分Ca5(PO4)3F]在高温下制备黄磷(P4)的热化学方程式为:4Ca5(PO4)3F(s)+21SiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) ΔH
①上述反应中,副产物矿渣可用来________。
②已知相同条件下:
4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) ΔH1
2Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g) ΔH2
SiO2(s)+CaO(s)=CaSiO3(s) ΔH3
用ΔH1、ΔH2和ΔH3表示ΔH,ΔH=____________。
(2)(江苏)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜。已知:
①Cu(s)+2H+(aq)=Cu2+(aq)+H2(g)ΔH1=+64.39 kJ·mol-1
②2H2O2(l)=2H2O(l)+O2(g)ΔH2=-196.46 kJ·mol-1
③H2(g)+
O2(g)=H2O(l)ΔH3=-285.84 kJ·mol-1
在H2SO4溶液中,Cu与H2O2反应生成Cu2+和H2O的热化学方程式为_________________________________________________________________。
高三化学填空题中等难度题查看答案及解析
-
磷单质及其化合物的有广泛应用.
(1)由磷灰石[主要成分Ca5(PO4)3F]在高温下制备黄磷(P4)的热化学方程式为:
4Ca5(PO4)3F(s)+2lSiO2(s)+30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g)△H
①上述反应中,副产物矿渣可用来______.
②已知相同条件下:
4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g)△H1
2Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g)△H2
SiO2(s)+CaO(s)=CaSiO3(s)△H3
用△H1、△H2和△H3表示△H,△H=______
(2)三聚磷酸可视为三个磷酸分子(磷酸结构式见右图)之间脱去两个分子产物,其结构式为______.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为______
(3)次磷酸钠(NaH2PO2)可用于化学镀镍.
①NaH2PO2中P元素的化合价为______.
②化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a)______Ni2++______ H2PO2-+______→______Ni+______ H2PO3 -+______
(b)6H2PO2-+2H+=2P+4H2PO3-+3H2↑
请在答题卡上写出并配平反应式(a).
③利用②中反应可在塑料镀件表面沉积镍-磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀.请从以下方面比较化学镀与电镀.
方法上的不同点:______;原理上的相同点:______;化学镀的优点:______.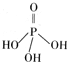
高三化学解答题中等难度题查看答案及解析