-
下列共价化合物中,共价键的键能最大的是( )
A.HCl B.HF C.HBr D.HI
高二化学选择题中等难度题查看答案及解析
-
下列共价化合物中,共价键的键能最大的是
A.HCl B.HF C.HBr D.HI
高二化学选择题简单题查看答案及解析
-
下列共价化合物中,共价键的键能最大的是
A、HCl B、HF C、HBr D、HI
高二化学选择题中等难度题查看答案及解析
-
下列共价化合物中,共价键的键能最大的是
A.HCl B.HF C.HBr D.HI
高二化学选择题简单题查看答案及解析
-
下列共价化合物中,共价键的键能最大的是
A.HCl B.HF C.HBr D.HI
【答案】B
【解析】
四物质分子均为卤代氢分子,结构相似,一般来讲,键长越短,键能越大;而键长由原子半径决定,所以四分子中F原子的半径最小,键长最短,键能最大,B项正确;答案选B。
考点:考查键能大小判断
【题型】选择题
【适用】容易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】下列粒子不属于等电子体的是
A.CH4和NH3 B.N2和CO
C.HCl和H2O D NH2-和H3O+
【答案】C
【解析】
A、CH4是10电子,NH3是10电子,属于等电子体,A项错误;B、N2是14电子,CO是14电子,属于等电子体,B项错误;C 、HCl是18电子,H2O是10电子,不属于等电子体,C项正确;D、NH2-是10电子,H3O+是10电子,属于等电子体,D项错误;答案选C。
考点:考查等电子体判断
【题型】选择题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】关于σ键和π键的比较,下列说法不正确的是
A.σ键是轴对称的,π键是镜像对称的
B.σ键是“头碰头”式重叠,π键是“肩并肩”式重叠
C.σ键不能断裂,π键容易断裂
D.H原子只能形成σ键,O原子可以形成σ键和π键
【答案】B
【解析】
A、σ键是轴对称的,π键是镜像对称的,A项正确;B、σ键是“头碰头”式重叠,π键是“肩并肩”式重叠,B项正确;C、σ键也能断裂,C项错误;D、H原子只能形成σ键,O原子可以形成σ键和π键,D项正确;答案选B。
考点:考查σ键和π键的比较
【题型】选择题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】某有机物的结构式如下:
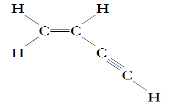
则分子中有________个σ键,________个π键。
【答案】7 3
【解析】
由结构简式可得有5个单键,1个双键,1个三键,故有7个σ键,3个π键。
考点:考查化学键判断
【题型】填空题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】以下列出的是一些原子的2p能级和3d能级中电子排布的情况。试判断,哪些违反了泡利不相容原理,哪些违反了洪特规则。
(1)
(2)
(3)
(4)
(5)
(6)
违反泡利不相容原理的有 ,违反洪特规则的有 。
【答案】(1);(2)、(4)、(5):
【解析】
在一个原子轨道里,最多只能容纳2个电子,而且它们的自旋状态相反,称为泡利不相容原理,所以违反泡利不相容原理的有(1);当电子排布在同一个能级的不同轨道时,基态原子中的电子总是单独优先占据一个轨道,而且自旋状态相同,称为洪特规则,所以违反洪特规则的有(2)、(4)、(5)。
考点:考查考查轨道表达式的一个正误判断
【题型】填空题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】下表为元素周期表的一部分,期中的编号代表对应的元素
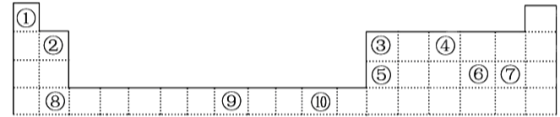
请回答下列问题:
(1)表中属于ds区的元素是________(填编号)。
(2)写出元素⑨的高价离子的电子排布式_____________________________。
(3)某元素的最外层电子排布式为nsnnpn+1,该元素原子的核外共有________种不同运动状态的电子。该元素在周期表中的位置是上表中相对应的 (填编号).
(4)⑥、⑦分别①形成的化合物稳定性较强的为 (化学式表示)
【答案】(1)⑩(2)1s22s22p63s23p63d5(3)7 ④ NH3分子间存在氢键(4)HCl:
【解析】
(1)元素周期表中位于ds区的元素是第一、二副族元素,所以⑩位于ds区。
(2)⑨是Fe元素,最高价离子是Fe3+,核外有23个电子,排布式为1s22s22p63s23p63d5。(3)s轨道最多只能排2个电子,所以n=2,最外层电子排布式为nsnnpn+1,则该元素的最外层是2s22p3,该元素是N元素,核外有7个电子,就有7种不同的运动状态;是上表中的④。
(4)⑥、⑦分别是S、Cl元素,①是H元素,Cl的非金属性比S强,所以HCl比较稳定。
考点:考查元素推断
【题型】填空题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】某元素的原子序数为29,试问:
(1) 它有__________个电子层
(2)有__________个能级。
(3)它的价电子排布式是__________。
(4)它属于第__________周期第__________族。
(5)它有__________个未成对电子。
【答案】 (1)29(2)4 7(3)3d104s1 (4)四 ⅠB(5)1
【解析】
根据核外电子排布原理,该元素的核外电子排布式应为1s22s22p63s23p63s104s1,共有29个电子,故为Cu元素。从核外电子排布式中可以得出n=4,有四个电子层,所以为第四周期元素,外围电子排布式为3d104s1,所以在第ⅠB族。外围电子的电子排布图为
,所以有1个未成对电子。
考点:考查核外电子排布原理
【题型】填空题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。其中J为0族元素。
X
Y
Z
R
W
J
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1)R原子的电子排布图为__________。
(2)在化合物YZ2中Y的化合价为__________;Y2-与Na+的半径大小为__________。
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是__________;X与Y的第一电离能:X__________Y(填“<”、“>”或“=”),其理由是_________________________________________。
【答案】(1)
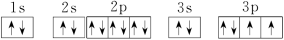 (2)+2 O2->Na+(3)F>O>N > N原子的p轨道为半充满,能量低较稳定,难失电子
(2)+2 O2->Na+(3)F>O>N > N原子的p轨道为半充满,能量低较稳定,难失电子【解析】
根据表格和J为0族元素可知:X为N,Y为O,Z为F,R为S,W为Br,J为Xe。
(1),R为S,电子排布图为
 。
。(2) 化合物YZ2是OF2,其中F为-1价,故O为+2价;O2-与Na+,核外电子排布相同,故O2->Na+。
(3)N、O、F属于同一周期元素,故电负性由大到小的顺序是F>O>N;N原子的p轨道为半充满,能量低较稳定,难失电子,故的第一电离能:N>O。
考点:考查元素及其性质推断
【题型】填空题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】下表中的数据是破坏1 mol化学键所消耗的能量。
物质
Cl2
Br2
I2
H2
HF
HCl
HBr
HI
能量(kJ)
243
193
151
436
565
431
363
297
根据上述数据回答(1)~(4)题。
(1)下列物质本身具有的能量最低的是( )
A.H2 B.Cl2
C.Br2 D.I2
(2)下列氢化物中,最稳定的是( )
A.HF B.HCl
C.HBr D.HI
(3)X2+H2===2HX(X代表F、Cl、Br)的反应是吸热反应还是放热反应:________。
(4)相同条件下,X2(X代表F、Cl、Br)分别与氢气反应,当消耗等物质的量的氢气时,放出或吸收的热量最多的是________。
高二化学填空题简单题查看答案及解析
-
I. 现有一组物质的熔点(℃)数据,据此回答下列问题:
HF:-83
HCl:-115
HBr:-89
HI:-51
(1)HF熔点反常是由于______________。这组物质中共价键的键能最大的是_____。
II.按要求回答下列问题。
(2)CS2气化时克服的粒子间作用是__________,1mol CS2中含有___mol σ键,含有___mol π键。
(3)HCHO分子中C原子轨道的杂化类型为______。
高二化学综合题中等难度题查看答案及解析
-
下列元素或化合物的性质变化顺序不正确的是( )
A.第一电离能:Cl>S>P>Si
B.共价键的极性:HF>HCl>HBr>HI
C.晶格能:NaF>NaCl>NaBr>NaI
D.热稳定性:MgCO3>CaCO3>SrCO3>BaCO3
高二化学多选题中等难度题查看答案及解析
-
下列叙述中正确的是
A.冰融化时水分子中共价键发生断裂
B.H2O2、PCl5都是含有极性键的非极性分子
C.HF、HCl、HBr、HI的酸性依次增强
D.H2O是一种非常稳定的化合物,这是由于氢键所致
高二化学选择题中等难度题查看答案及解析
-
下列物质性质的变化规律,与共价键的键能大小有关的是
A. F2、Cl2、Br2、I2 的熔点、沸点逐渐开高 B. HCl、HBr、HI、HF 的沸点逐渐开高
C. 金刚石的硬度、熔点、沸点都高于晶体硅 D. NaF、NaCl、NaBr、NaI的熔点依次降低
高二化学单选题中等难度题查看答案及解析
-
下列物质性质的变化规律,与共价键的键能大小有关的是 ( )
A. F2、Cl2、Br2、I2的熔点、沸点逐渐升高
B. HF、HCl、HBr、HI的热稳定性依次减弱
C. 乙醇可以与水任意比互溶
D. NaF、NaCl、NaBr、NaI的熔点依次降低
高二化学单选题简单题查看答案及解析