-
(10分)称取三份锌,分别放入三支试管中,在试管甲里加入PH=3的盐酸50ml,在试管乙里加入PH=3的醋酸50ml,在试管丙里加入PH=3的醋酸50ml及少量铜粉,塞上导管塞子,定时测定生成H2的体积。若反应终了时,生成的H2一样多,且锌没有剩余。
(1)用“>”、“=”或“<”回答以下问题:
①参加反应的锌的质量由多到少的顺序为:________。
②反应完毕时,所需反应时间由多到少的顺序为:________。
(2)简答:
①反应所需时间最长的一种酸的原因是:________。
②乙、丙反应所需时间是否相等?答:________。其原因是:________。
高二化学填空题中等难度题查看答案及解析
-
称取2份一定质量的锌,分别盛在2支试管中,按下列要求另加物质后,塞上带导管的塞子,定时测定生成氢气的体积。
A试管中加入pH=3的盐酸50mL; B试管中加入pH=3的醋酸50mL。
若反应终了时生成的氢气一样多,且没有剩余的锌。那么
(1)开始时反应速率的大小为A__________B。(填“<”、“>”或“=”)
(2)2支试管中参加反应的锌的质量A__________B。(填“<”、“>”或“=”)
(3)反应终了所需时间A__________B。(填“<”、“>”或“=”)
高二化学填空题中等难度题查看答案及解析
-
下列实验操作规范且能达到目的的是
目的
操作
A.
取20.00 mL盐酸
在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶
B.
测定醋酸钠溶液pH
用玻璃棒蘸取溶液,点在湿润的pH试纸上
C.
配制浓度为0.010mol/L的高锰酸钾溶液
称取高锰酸钾固体0.158 g,放入100 mL容量瓶中,加水溶解并稀释至刻度
D.
清洗碘升华实验所用试管
先用酒精清洗,再用水清洗
A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析
-
称取三份锌粉,分别盛于甲、乙、丙三支试管中。甲中加入50mLc(H+)=0.1mol/L的盐酸,乙中加入50mL c(H+)=0.1mol/L的醋酸,丙加入50mLc(H+)=0.1mol/L的醋酸及少量的胆矾粉末。若反应终了,生成氢气的体积一样多,且没有剩余的锌,则下列说法不正确的是
A. 开始时反应速率的大小:甲=乙=丙 B. 反应终了时,所需时间的大小:甲>乙>丙
C. 反应过程中,甲、乙速率相同 D. 三支试管中参加反应的锌的质量:甲=乙<丙
高二化学单选题中等难度题查看答案及解析
-
以下有关溶液(均在常温下)的结论正确的是
A.pH=1的盐酸与pH=5的盐酸等体积混合后pH=3
B.0.1 mol/L醋酸溶液100 mL与0.2 mol/L氨水50 mL混合后能恰好完全中和
C.pH>7的溶液中不可能存在CH3COOH分子
D.等浓度等体积的KOH溶液和CH3COOH溶液混合后:c(CH3COO-)=c(K+)
高二化学选择题中等难度题查看答案及解析
-
以下有关溶液(均在常温下)的结论正确的是:
A.pH=1的盐酸与pH=5的盐酸等体积混合后pH=3
B.0.1 mol/L醋酸溶液100 mL与0.2 mol/L氨水50 mL混合后能恰好完全中和
C.pH>7的溶液中不可能存在CH3COOH分子
D.等浓度等体积的KOH溶液和CH3COOH溶液混合后:c (CH3COO-)=c (K)+
高二化学选择题中等难度题查看答案及解析
-
常温下,用pH传感器进行数字化实验,分别向两个盛50 mL0.100mol/L盐酸的烧杯中匀速滴加50mL去离子水、50 mL 0.100 mol/L 醋酸铵溶液,滴加过程进行磁力搅拌,测得溶液pH随时间变化如图所示。已知常温下醋酸铵溶液pH=7,下列说法错误的是
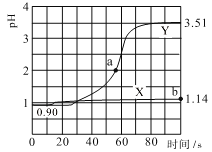
A.曲线X表示盐酸中加醋酸铵溶液稀释的pH变化
B.曲线Y的pH变化主要是因为CH3COO-与H+结合成了弱电解质
C.a点对应的溶液中c(Cl-)+c(CH3COO-)+c(CH3COOH)-c(NH4+)=0.01mol/L
D.b点对应的溶液中水电离的c(H+)=10-12.86 mol/L
高二化学多选题中等难度题查看答案及解析
-
在大试管里加入3mL乙醇、2mL冰醋酸,再缓缓加入2mL浓硫酸,边加边振荡,在另一支试管中加入饱和碳酸钠溶液,试回答下列问题:
(1)酯化反应(定义):__.反应现象:__反应化学方程式:__;
(2)在酯化反应中,乙酸的分子结构发生什么变化_________?
(3)酯化反应在常温下反应极慢,一般15年才能达到平衡,怎样能使反应加快呢_________?
(4)酯化反应中,浓硫酸起什么作用_________?
(5)为什么用来吸收反应生成物的试管里要装饱和碳酸钠溶液_________?不用饱和碳酸钠溶液而改用水来吸收酯化反应的生成物,会有什么不同的结果_________?
(6)为什么出气导管口不能插入碳酸钠液面下_________?
高二化学实验题简单题查看答案及解析
-
常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如右图所示。下列说法不正确的是

A. 图中表示醋酸溶液中pH变化曲线的是B
B. 设盐酸和醋酸中加入的Zn质量分别为m1、m2,则m1<m2
C. pH=2时盐酸和醋酸的物质的量前者小
D. pH=4时两溶液c(Zn2+)相等
高二化学单选题中等难度题查看答案及解析
-
对室温下100 mL pH=2的醋酸和盐酸两种溶液分别采取下列措施,有关叙述正确的是
A.加水稀释至溶液体积为200 mL,醋酸溶液的pH变为4
B.温度都
升高20 ℃后,两溶液的pH不再相等
C.加水稀释至溶液体积为200 mL后,醋酸的电离度减小,电离平衡常数也减小
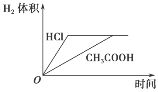
D.加
足量的锌充分反应后,两溶液中产生的氢气体积可用上图表示
高二化学选择题中等难度题查看答案及解析