-
固氮有三种方式:生物固氮、工业合成氨和放电条件下氮气与氧气化合.全世界工业合成氮肥中的氮只占固氮总量的20%,其余绝大多数是通过生物固氮进行的,最常见的是豆科植物根部的根瘤菌,能将大气中游离态的氮经固氮酶的作用生成氮的化合物,以利于植物利用.
(1)根瘤菌与豆科植物的关系在生物学上称为______;
(2)根瘤菌之所以有固氮作用,是因为它有独特的固氮酶,而最根本原因是它含有独特的______;
(3)日本科学家把固氮基因转移到水稻根际微生物中,通过指导合成固氮所需的______进而引起固氮作用.更为理想的是直接将固氮基因转移到稻、麦等粮食及经济作物的细胞中,让植物本身直接固氮,这样可以免施氮肥.如果这种愿望实现的话说,那么固氮基因中遗传信息表达途径为______;
(4)这种生物固氮与工业合成氨比较,它是在______条件下进行的,从而节省了大量的器材、设备和能源;
(5)俗话说“雷雨发庄稼”,因为电闪雷鸣的雨天,氮气在空气中发生一系列的反应,产生了植物可利用的含氮化合物,写出有关的三个反应方程式______、______、______.高三化学解答题中等难度题查看答案及解析
-
运用化学反应原理研究部分单质及其化合物的反应有重要意义。
(1)氨是氮循环过程中的重要物质,是氮肥工业的重要原料。氨的合成目前普遍使用的人工固氮方法:N2(g)+3H2(g)
2NH3(g)。请回答:
①已知:H-H键能为436kJ/mol,N N键能为945kJ/mol,N一H键能为391kJ/mol.由键能计算消耗1molN2时的△H=_________。若在恒温、恒压条件下向上述平衡体系中通入氦气,平衡_______移动(填“向左”、“向右”或“不”);
②如图中:当温度由T1变化到T2时,KA______KB(填“>”、“<”或“=”)。
(2)氨气溶于水得到氨水。NO2可用氨水吸收生成NH4NO3,25℃时,将amolNH4NO3溶于水,溶液显酸性,原因是___________(用离子方程式表示),向该溶液滴加bL氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将__________(填“正向”、“不”或“逆向”)移动,所滴加氨水的浓度为________mol/L(用含a、b的代数式表示),(NH3·H2O的电离平衡常数取Kb=2×10-5mol/L)
(3)硫酸生产中,SO2催化氧化生成SO3:SO2(g)+1/2O2(g)
SO3(g)△H<0,是工业上生产硫酸的关键步骤。
①在某温度时,该反应的平衡常数K=0.75,若在此温度下,向100L的恒容密闭容器中,充入3mol SO2、4mol O2和4mol SO3,则反应开始时正反应速率________逆反应速率(填“<”、“>”或“=”)。
②在①中的反应达到平衡后,改变下列条件,能使SO2(g)平衡浓度比原来减小的是________。
a.保持温度和容器体积不变,充入1.0mol SO3(g)
b.保持温度和容器内压强不变,充入2.0mol He
c.降低温度
d.在其他条件不变时,减小容器的容积
③由硫酸可制得硫酸盐.在一定温度下,向K2SO4溶液中滴加Na2CO3溶液和BaCl2溶液,当两种 沉淀共存时,
=_________。
[已知该温度时,Ksp(BaSO4)=1.3×10-10,Ksp(BaCO3)=5.2×10-9]
高三化学填空题极难题查看答案及解析
-
氨气是一种重要的化工原料,氨态氮肥是常用的肥料。
工业合成氨的化学方程式:N2 + 3H2
2NH3 +92.4KJ
(1)它是氮的固定的一种,属于_____________( 选填“大气固氮”、“生物固氮” “人工固氮”);若升高温度,该平衡向____________方向移动(选填“正反应”或“逆反应”)。
(2)该反应达到平衡状态的标志是______________。(选填编号)
a.压强不变 b.v正(H2)= v正(NH3) c.c (N2)不变 d.c(NH3)= c(N2)
(3)欲使NH3产率增大,可采取的措施有_____________、____________。若容器容积为2L,开始加入的N2为0.1mol,20s后测得NH3的物质的量为0.08mol,则N2的平均反应速率为_________________________________________mol/(L∙S)。
(4)如右图所示,将集有氨气的试管倒置于水槽中,观察到试管内液面上升,溶液变为红色,解释发生该现象的原因____________________________________。
(5)(NH4)2SO4是常用的氮肥,长期施用时会使土壤酸化板结,
用离子方程式表示原因___________________________________
检验(NH4)2SO4含NH4+的方法是_______________________________。
___________________________________________________.
高三化学填空题中等难度题查看答案及解析
-
下列属于自然固氮的是
A.N2和O2在雷电作用下生成NO B.某金属化合物将氮气转化为化合态氮
C.在一定条件下使N2、H2合成NH3 D.NO生成NO2
高三化学单选题简单题查看答案及解析
-
氮的单质及其化合物在生活和生产中有很重要的用途。
(1)氨是合成硝酸、铵盐和氮肥的基本原料。在一定条件下用氮气和氢气合成氨气,然后再用氨氧化法制取硝酸。在整个生产过程中,氮气的利用率为85%。写出氨氧化法制取硝酸的反应式____________现有0.2t液态氮,能生产出浓度为40%的硝酸______________千克。
(2)向27.2 g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5 L,固体物质完全反应,生成NO和Cu(NO3)2。在所得溶液中加入1.0 mol·L-1的NaOH溶液1.0 L,此时溶液呈中性。金属离子已完全沉淀,沉淀质量为39.2 g。
①Cu与Cu2O的物质的量之比?____________
②硝酸的物质的量浓度?___________
(3)将30mLNO和O2混合气体通入过量NaOH溶液中,充分反应后,溶液中只含两种溶质(不考虑水解),且剩余气体体积为2mL。求原混合气体中NO和O2体积比?______________
高三化学综合题中等难度题查看答案及解析
-
将大气中的氮气活化合成氨是维持地球上生命所必需的转化过程,最近我国成功研制出高效电催化固氮催化剂Mo2N,它的研制成功能有效提高氮肥生产效率。
回答下列问题:
(1)钼(Mo)位于第五周期,与铬同副族,则Mo的价电子排布式为______________。
(2)基态氮原子核外电子空间运动状态有____种,氮元素所在周期中第一电离能最大的前三种元素依次是____(按由大到小的顺序写)。
(3)氮元素能形成一系列的化合物,如NH3、HN3(结构式为
)、H2NCH2COOH等。NH3的分子构型为________,HN3结构式中间两个氮原子的杂化轨道类型为________,1个HN3分子中含______个π键;H2NCH2COOH(熔点为182 ℃)、CH3CH2COOH(熔点为−22 ℃)的相对分子质量几乎相同,但熔点相差很大,从物质结构的角度分析,导致该现象的主要原因是______。
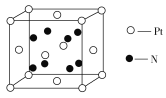
(4)氮与铂元素形成的某种化合物晶胞如图所示,则该化合物的化学式为______,若该晶胞的边长为d pm,则晶体的密度为____ g/cm3。
高三化学综合题中等难度题查看答案及解析
-
氮的固定意义重大,氮肥的使用大面积提高了粮食产量。人工固氮最有效的方法是合成氦,一种工业合成氨的简易流程如图所示(净化、后期处理等流程未列出):
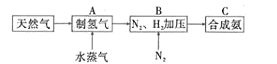
回答下列问题:
Ⅰ.步骤A制氢气的原理之一是CH4(g)+2H2O(g)⇌CO2(g)+4H2(g) ∆H=a kJ/mol
(1)已知:H2、CH4的燃烧热分别为285.8kJ/mol、890.31k/mol;H2O(g)⇌H2O(l) ∆H=-44kJ/mol则a=____kJ/mol。
(2)在密闭容器中,既能加快反应速率,又一定能提高平衡体系中H2体积分数的措施是_____(填序号)。
a.加入催化剂 b.升高温度 c.降低压强 d.增大c(H2O)
Ⅱ.步骤B完成了原料气准备后,通过步骤C合成氨,其原理为N2(g)+3H2(g)
2NH3(g) ∆H=-92.4kJ/mol。
(3)若T℃下,向一个容积为2L的真空密闭容器中(有催化剂)通入lmol N2、3mol H2,1分钟后达到化学平衡状态,测得容器内的压强是开始时的0.8倍。则:
①下列叙述可说明该反应已经达到化学平衡状态的是______(填序号)。
a.3v(H2)正=2v(NH3)逆 b.混合气体的平均相对分子质量不再发生改变
c.混合气体的密度不再发生改变 d. 1个N≡N键断裂的同时有3个H—H键生成
②t分钟内v(H2)=_______。
③T℃下该反应的K=___________(列出计算式即可)。
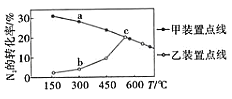
④一定条件下,向体积相同的甲(含催化剂)、乙两个容器中分别充入等物质的量的N2和等物质的量的H2进行合成氨反应,均反应1小时、测得N2的转化率随温度变化如图所示,a、b、c三点中达到化学平衡状态的点有_________,乙装置中N2转化率随着温度的升高先升后降的原因可能是______。
(4)我国科学家成功研制出一种高效电催化固氮催化剂Mo2N,其固氮原理如图所示,该装置中,阴极上的电极反应式为______。
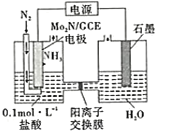
高三化学综合题困难题查看答案及解析
-
下列关于自然界中氮循环的说法错误的是
A. 氮肥均含有NH4+
B. 雷电作用固氮中氮元素被氧化
C. 碳、氢、氧三种元素参与了自然界中氮循环
D. 合成氨工业的产品可用于侯氏制碱法制备纯碱
高三化学单选题中等难度题查看答案及解析
-
下列关于自然界中氮循环的说法错误的是
A.氮肥均含有NH4+
B.雷电作用固氮中氮元素被氧化
C.碳、氢、氧三种元素参与了自然界中氮循环
D.合成氨工业的产品可用于侯氏制碱法制备纯碱
高三化学单选题简单题查看答案及解析
-
自然界中氮的循环涉及到地球上生物圈的方方面面.人类进入工业化社会以后,化学合成氮肥的数量迅速上升,对氮的循环和环境影响很大.下图是工业合成氮肥的转化关系:
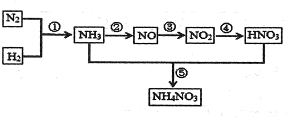
回答下列问题:
(1)反应①的条件是______,反应④的化学方程式为______,反应⑤所得产物的溶液中离子浓度由大到小得顾序为______.
(2)实验室制取NH3的一种方法是在生石灰中滴加浓氨水,其原因是______.
(3)硝酸厂的尾气含有氮的氧化物,直接排放将污染空气.目前科学家探索利用燃料气体中的CH4等将氮的氧化物还原为N2和H2O,反应原理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
CH4(g)+4NO2(g)=2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1
则CH4直接将NO2还原为N2的热化学方程式为______.
(4)下图表示某温度时,反应N2O4(g)2NO2(g)在前1l0s内的反应进
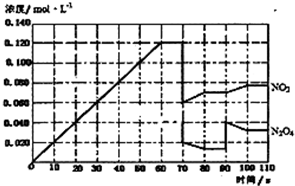
①此反应的平衡常数表达式K=______.
②反应进行到70s时,改变的条件可能是______(填字母),反应进行到90s时,改变的条件可能是______(填字母)
A.加入催化剂 B.扩大容器体积 C.升高温度 D.增大N2O4的浓度
③请在图中画出反应物N2O4在0~70秒时的浓度变化曲线.高三化学解答题中等难度题查看答案及解析