-
磷酸(H3PO4)、亚磷酸(H3PO3)和次磷酸(H3PO2)都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。下列推断正确的是( )
A.磷酸与氢氧化钠反应能生成2种盐
B.NaH2PO4、NaH2PO3、NaH2PO2都是酸式盐
C.H3PO4、H3PO3、H3PO2都是含氧酸
D.H3PO3是三元酸,又是还原性酸
高三化学选择题中等难度题查看答案及解析
-
磷酸(H3PO4)、亚磷酸(H3PO3)和次磷酸(H3PO2)都是重要的化工产品。已知:1mol磷酸、亚磷酸、次磷酸最多消耗NaOH的物质的量依次为3mol、2mol、1mol。下列推断正确的是
A.磷酸与氢氧化钠反应能生成2种盐
B.NaH2PO4、NaH2PO3、NaH2PO2都是酸式盐
C.H3PO4、H3PO3、H3PO2都是含氧酸
D.H3PO3是三元酸,又是还原性酸
高三化学选择题简单题查看答案及解析
-
亚磷酸(H3PO3,二元中强酸)及其盐在工农业生产中有着重要作用。
已知:25℃时,亚磷酸(H3PO3)的Ka1=5×10-2,Ka2=2.5×10-7
(1)亚磷酸(H3PO3)具有强还原性,可被阴离子氧化为磷酸。则该反应的离子方程式为______________________________________。
(2)试从电离平衡移动的角度解释Ka1、Ka2差异原因_____________。
(3)在稀溶液中H3PO3(aq)
H2PO3-(aq)+H+(aq) △H=akJ/mol
H2PO3-(aq)
HPO32-(aq)+H+(aq) △H=bkJ/mol
H+(aq)+ OH-(aq)=H2O(l) △H=ckJ/mol
H3PO3(aq)+ 2NaOH(aq)
Na2HPO3(aq)+2H2O(l) △H=___________kJ/mol
(4)亚磷酸氧钠可使碘水褪色,.25℃时,Na2HPO3水解反应的Kb=_____________,若向Na2HPO3溶液中加入少量的I2,则溶液中
将 ______________ (填“增大”、“减小”或“不变”)。
(5)电解Na2HPO3溶液也可得到亚磷酸,装置示意图如下:
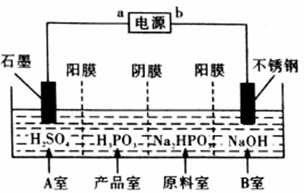
①a为电源_____极(填“正”或“负”)产品室中反应的离子方程式为__________________________。
②得到0.1mol亚磷酸的同时,理论上B室可制得NaOH质量为___________g。
高三化学简答题困难题查看答案及解析
-
磷及其化合物在生产、生活中有重要的用途。回答下列问题:
(1)已知磷酸(
 )分子中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2) 却不能与D2O发生氢交换。则H3PO2是(填“一元”“二元”或“三元”)酸,其分子的结构式为________(填字母)。
)分子中的三个氢原子都可以与重水分子(D2O)中的D原子发生氢交换。又知次磷酸(H3PO2)也可与D2O进行氢交换,但次磷酸钠(NaH2PO2) 却不能与D2O发生氢交换。则H3PO2是(填“一元”“二元”或“三元”)酸,其分子的结构式为________(填字母)。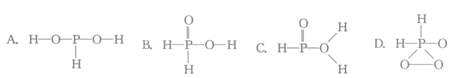
(2)H3PO2具有较强的还原性,可以通过电解的方法制备。“四室电渗析法”工作原理如图所示(阳离子交换膜和阴离子交换膜分别只允许阳离子、阴离子通过)。

①阳极的电极反应式为_________。
②II 膜为___________(填“阴离子交换膜”或“阳离子交换膜”)。
③早期采用“三室电渗析法”制备H3PO2,将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与产品室之间的交换膜,从而合并阳极室与产品室,其缺点是产品中混有______杂质。
高三化学填空题困难题查看答案及解析
-
次磷酸(H3PO2一元弱酸)和氟硼酸(HBF4)均可用于植物杀菌。常温时,有1mol∙L-1的H3PO2溶液和1mol∙L-1的HBF4溶液,两者起始时的体积均为V0,分别向两溶液中加水,稀释后溶液的体积均为V,两溶液的pH变化曲线如图所示。下列说法错误的是

A.常温下,NaBF4溶液的pH=7
B.常温下,H3PO2的电离平衡常数约为1.1
10-2
C.NaH2PO2 溶液中:c(Na+) =c( H2PO2- ) +c( HPO22-) +c(PO23-) +c( H3PO2)
D.常温下,在0≤pH≤4时,HBF4溶液满足
高三化学单选题困难题查看答案及解析
-
次磷酸(H3PO2一元弱酸)和氟硼酸(HBF4)均可用于植物杀菌。常温时,有1mol∙L-1的H3PO2溶液和1mol∙L-1的HBF4溶液,两者起始时的体积均为V0,分别向两溶液中加水,稀释后溶液的体积均为V,两溶液的pH变化曲线如图所示。下列说法错误的是
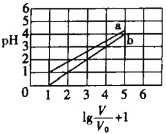
A.常温下,NaBF4溶液的pH=7
B.常温下,H3PO2的电离平衡常数约为1.1
10-2
C.NaH2PO2 溶液中:c(Na+) =c( H2PO2- ) +c( HPO22-) +c(PO23-) +c( H3PO2)
D.常温下,在0≤pH≤4时,HBF4溶液满足
高三化学单选题困难题查看答案及解析
-
已知H3PO2(次磷酸)是一种精细磷化工产品,要求密封阴凉保存。工业制备原理如下:
(I)2P4+3Ba(OH)2+6H2O===3Ba(H2PO2)2+2PH3↑
(II)Ba(H2PO2)2+H2SO4===BaSO4↓+2H3PO2
下列推断不正确的是( )
A.反应I是氧化还原反应,反应II是非氧化还原反应
B.H3PO2具有强还原性,高温时在空气可能被氧化成磷酸
C.在反应I中氧化剂与还原剂的质量之比为1∶1
D.在标准状况下生成2.24 L PH3,上述反应转移0.3 mol电子
高三化学选择题中等难度题查看答案及解析
-
次磷酸(H3PO2)是一种精细磷化工产品,有强还原性。已知:①2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+2PH3↑,②H3PO2+NaOH(足量)=NaH2PO2+H2O。下列推断不正确的是
A. H3PO2的结构式为
B. H3PO2具有强还原性,在空气中可能被氧化成磷酸
C. NaH2PO2是酸式盐
D. 每消耗1mol P4,反应①中转移6mol电子
高三化学多选题中等难度题查看答案及解析
-
一元中强酸次磷酸(H3PO2)是一种精细化工产品,下列说法正确的是( )
A.次磷酸的电离方程式为H3PO2
3H++PO23-
B.次磷酸中P的化合价为+1
C.NaH2PO2是酸式盐
D.NaH2PO2溶液显弱酸性
高三化学选择题简单题查看答案及解析
-
磷有多种化合物,次磷酸(H3PO2)和次磷酸钠(NaH2PO2)常为化工生产中的还原剂。完成下列填空:
(1)H3PO2是一元中强酸,写出其电离方程式:_______;请将NaH2PO2溶液中的各离子按浓度由大到小的顺序排列:__________。
(2)室温下0.1mol/L的NaH2PO2溶液和0.1mol/L的Na2CO3溶液,pH更大的是_______,其原因是__________。
(3)化学镀银,可利用H3PO2把溶液中的Ag+还原为银的反应,已知该反应中还原剂与氧化剂的物质的量之比为1:4,则氧化产物是_______(填化学式)。
(4)工业上可用白磷(P4)与Ba(OH)2溶液反应生成PH3和Ba(H2PO2)2。写出并配平该反应的化学方程式________,若反应中转移电子6NA,用去还原剂_____mol。再向Ba(H2PO2)2溶液中加入盐酸制备H3PO2,有人说应该用硫酸代替盐酸,请说明用硫酸代替盐酸的优点:_______。
(5)下图是利用电解原理制备H3PO2的示意图(阳离子交换膜和阴离子交换膜分别只允许阳、阴离子通过;已知电极反应为:

阳极 4OH--4e→O2↑+ H2O
阴极 2H+ + 2e→H2↑):
分析在阳极室得到H3PO2原因:_______。
高三化学综合题困难题查看答案及解析