-
钾是—种活泼的金属,工业上通常用金属钠和氯化钾在高温下反应制取。该反应为:Na(l)+KCl(l) NaCl(l)+K(g)一Q
NaCl(l)+K(g)一Q
| 压强(kPa) | 13.33 | 53.32 | 101.3 |
| K的沸点(℃) | 590 | 710 | 770 |
| Na的沸点(℃) | 700 | 830 | 890 |
| KCl的沸点(℃) | | | 1437 |
| NaCl的沸点(℃) | | | 1465 |
该反应的平衡常数可表示为:K=C(K),各物质的沸点与压强的关系见上表。
(1)在常压下金属钾转变为气态从反应混合物中分离的最低温度约为________,而反应的最高温度应低于________。
(2)在制取钾的过程中,为了提高原料的转化率可以采取的措施是____________。
(3)常压下,当反应温度升高900℃时,该反应的平衡常数可表示为:K=______
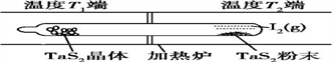
(4)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应:TaS2(s)+2I2(g) TaI4(g)+S2(g) ΔH>0 (Ⅰ)如图所示,在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净TaS2晶体,则温度T1____T2(填“>”“<”或“=”)。上述反应体系中循环使用的物质是____。
TaI4(g)+S2(g) ΔH>0 (Ⅰ)如图所示,在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净TaS2晶体,则温度T1____T2(填“>”“<”或“=”)。上述反应体系中循环使用的物质是____。
-
下列说法错误的是
A. 电解NaCl溶液和电解熔融的NaC1均可制备金属钠
B. 电解熔融氯化镁制金属镁
C. 氧化铁与一氧化碳高温反应炼铁
D. 工业上常用氢气在氯气中燃烧的方法制取盐酸
-
下列有关金属冶炼的说法正确的是
A. 工业上常用电解NaCl水溶液可制取金属钠
B. 工业上常用电解MgO熔融可制取金属镁
C. 工业上常用CO高温条件下还原Fe2O3可制取Fe
D. 工业上常用金属钠和TiCl4溶液反应制取金属Ti
-
工业上,常用Mg还原法制取金属Ti,反应如下:2Mg+TiCl4 2MgCl2+Ti。①该反应属于置换反应;②该反应属于氧化还原反应;③该反应表明Mg比Ti活泼;④Ti被誉为“21世纪的金属”,在航天工业上有广泛用途。以上说法正确的是( )
2MgCl2+Ti。①该反应属于置换反应;②该反应属于氧化还原反应;③该反应表明Mg比Ti活泼;④Ti被誉为“21世纪的金属”,在航天工业上有广泛用途。以上说法正确的是( )
A.只有①② B.只有③④ C.只有①②③ D.全部
-
工业上生产Na、Ca、Mg都用电解熔融的氯化物,但K不能用电解熔融态的方法得到,因金属钾易溶于熔融态的KCl而有危险,很难制得K,且降低电流效率。现生产钾是用金属钠和KCl在850℃反应制取,有关的反应式为:KCl+Na=NaCl+K↑下列说法错误的是
A.该反应850℃的选择是基于熔沸点的考虑
B.该反应不能在空气中进行
C.该反应属于置换反应的类型
D.该反应表明钠比钾的活动性强
-
下列事实中,不能用勒夏特列原理解释的是
A.冰镇的啤酒打开后泛起泡沫
B.对N2+3H2 2NH3的反应,使用铁触媒可加快合成氨反应的速率
2NH3的反应,使用铁触媒可加快合成氨反应的速率
C.工业制取金属钾Na(l)+KCl(l) NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来
NaCl(l)+K(g)选取适宜的温度,使K成蒸汽从反应混合物中分离出来
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
-
下列有关金属的工业制法中,正确的是
A.制钛:用金属钠置换氯化钛(TiCl4)溶液中的钛
B.炼铁:用焦炭和空气反应产生的CO在高温下还原铁矿石中的铁
C.制钠:用海水为原料制得精盐,再电解纯净的NaCl溶液
D.炼铜:用黄铜矿(主要成分为CuFeS2)直接电解精炼得到纯度为99.9%的铜
-
在熔融状态下,Na与KCl存在可逆反应:Na+KCl NaCl+K,通过调整温度,可利用金属Na来制取K。
NaCl+K,通过调整温度,可利用金属Na来制取K。
| 物质 | K | Na | KCl | NaCl |
| 熔点(℃) | 63.6 | 97.8 | 770 | 801 |
| 沸点(℃) | 774 | 883 | 1 500 | 1 413 |
根据上表的熔点和沸点,确定由Na与KCl反应制取K的合适温度为( )
A.770℃ B.801℃
C.850℃ D.770℃~801℃
-
下列叙述正确的是
A.工业上用电解熔融氯化钠的方法制取钠
B.钠加入氯化镁的饱和溶液中可以制取金属镁
C.电解冶炼铝的原料是氯化铝
D.碳在高温下能还原氧化镁中的镁
-
下列说法正确的是( )
A. 元素周期表有7个周期、18个族
B. 天然气是一种清洁的化石燃料
C. 工业上常用电解NaCl水溶液的方法制取金属钠
D. 淀粉和纤维素互为同分异构体
NaCl(l)+K(g)一Q
TaI4(g)+S2(g) ΔH>0 (Ⅰ)如图所示,在石英真空管中进行,先在温度为T2的一端放入未提纯的TaS2粉末和少量I2(g),一段时间后,在温度为T1的一端得到了纯净TaS2晶体,则温度T1____T2(填“>”“<”或“=”)。上述反应体系中循环使用的物质是____。
