-
文献报道:利用氯化氢氧化反应一脱水耦合工艺,可用有机氯化工艺的副产品氯化氢为原料制备氯气,实现氯的循环利用,原理为4HCl(g)+O2(g) 2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化率影响的曲线如图.
2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化率影响的曲线如图.
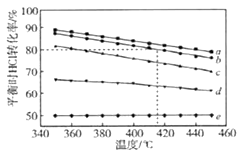
请回答下列问题:
(1)可以判断该反应已经达到化学平衡的是__. (填字母).
A.密闭容器中总压强不变 B.密闭容器中混合气体的密度不变
C.v(HCl)=2v(Cl2) D.密闭容器中氯气的体积分数不变
(2)d曲线对应的投料比是__(填比值,从题干中选择,下同).有机工业需要含O2量低的氧气和氯化氢混合气体,可控制n(HCl):n(O2)=_______制备.
(3)该反应的平衡常数表达式为________.
(4)若按b曲线对应的投料比进行反应,且温度为415℃,反应达到平衡时Cl2的体积分数为_______.
-
氯气是一种清洁、高效新能源, 也是重要的化工原料。
(1)通过热化学循环在较低温度下由硫化氢分解制备氢气的反应系统原理为:
SO2(g)+I2(s)+2H2O(l)=2HI(aq)+H2SO4(aq) ∆H1=-151kJ∙mol-1
2HI(aq)=H2(g)+I2(s) ∆H2=+110kJ∙mol-1
H2S(g)+H2SO4(aq)=S(s)+SO2(g)+2H2O(l) ∆H3=+61kJ∙mol-1
(热化学硫碘循环硫化氢分解联产氢气、硫磺系统)
通过计算可知,该系统制氢的热化学方程式为___________。
(2)工业上利用CO和H2合成清洁能源CH3OH,其反应为CO(g)+2H2(g)⇌CH3OH(g)ΔH= -116 kJ·mol-1。如图表示CO的平衡转化率(α)随温度和压强变化的示意图:
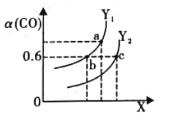
①X 表示的是______ (填“温度”或“压强”) ,理由是_________;Y1______Y2 (填“<”、“ >”或“=”)
②在2L恒容密闭容器中充入2 mol CO 和4 mol H2,一定条件下经过10 min 达到平衡状态c 点处。在该条件下,从开始至达到平衡状态v(CH3OH) =______ mol∙L-1∙min -1,平衡常数K=________(填最简分数)。平衡常数Ka、Kb、Kc的大小关系是______
③下列措施既能增大反应速率又能提高反应物转化率的是______ (填字母)。
A. 使用催化剂 B. 及时分离CH3OH C.升高温度 D.增大压强
(3) 已知燃料电池的比能最与单位质量燃料物质失去的电子数成正比。理论上H2、CH4、CH3OH的碱性电池的比能量由大到小的顺序为_________。
-
氯化铜、氯化亚铜是重要的化工原料,广泛地用作有机合成催化剂。
I.实验室中以粗铜(含杂质Fe)为原料制备铜的氯化物。现用左图所示的实验仪器及药品来制备纯净、干燥的氯气并与粗铜反应(铁架台、铁夹、酒精灯已省略)。按要求回答下列问题:
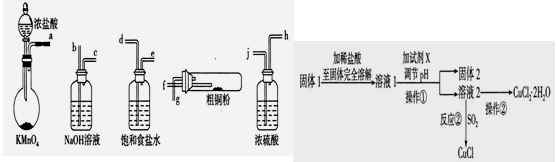
(1)按气流方向连接各仪器接口顺序是:a→ 、 → 、 → 、 → 。
(2)写出加热时硬质试管中主要发生反应的化学方程式 。
II.若将上述实验制得的固体产物按如上右图的流程操作,请回答下列问题:
(3)检验溶液2中是否含有杂质离子的试剂是 。
(4)溶液l可加试剂X用于调节pH以除去杂质,X可选用下列试剂中的(填序号) 。
a.NaOH b.NH3·H2O C.CuO d.CuSO4 e.Cu2(OH)2CO3
(5)反应②是向溶液2中通入一定量的SO2,加热一段时间后生成CuCl白色沉淀。写出制
备CuCl的离子方程式
-
以SO2为原料,通过下列工艺可制备化工原料H2SO4和清洁能源H2。下列说法中不正确的是

A.该生产工艺中Br2被循环利用
B.在电解过程中,电解槽阴极附近溶液的pH变大
C.原电池中负极发生的反应为SO2+2H2O-2e-=SO42-+4H+
D.该工艺总反应的化学方程式表示为SO2+Br2+2H20=2HBr+H2SO4
-
以硫铁矿(主要成分为 )为原料制备氯化铁晶体(
)为原料制备氯化铁晶体( )的工艺流程如下所示:
)的工艺流程如下所示:
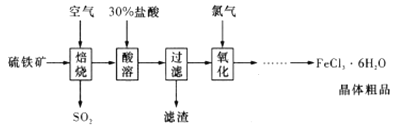
下列说法不正确的是
A. “酸溶”过程中使用的酸也可以是硝酸
B. 为防止污染,“焙烧”过程中产生的 应回收利用
应回收利用
C. 通入氯气的目的是氧化
D. 用 制取无水
制取无水 时,需要在氯化氢气流中加热
时,需要在氯化氢气流中加热
-
甲烷是一种重要的基础化工原料,不仅可制备多种重要有机产品,还可用于环境保护。请回答下列问题:
(1)用甲烷催化还原氮的氧化物可消除氮氧化物的污染。已知:

反应过程(2)是__反应(填“放热”或“吸热”),甲烷还原NO2生成H2O(g)、N2和CO2时的热化学方程式是__。
(2)工厂利用甲烷与氯气的反应原理制取氯甲烷,为妥善处理氯甲烷生产企业的副产物CCl4,以减少其对臭氧层的破坏。化学家研究在催化条件下,通过下列反应:CCl4(g)+H2(g) CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
CHCl3(g)+HCl(g),使CCl4转化为重要的化工原料氯仿(CHCl3)(不考虑副反应)。在固定容积为2L的密闭容器中,该反应达到平衡后,测得如下数据:
| 实验 序号 | 温度℃ | 初始n(CCl4)( mol) | 初始n(H2)( mol) | 平衡时n(CHCl3)( mol) |
| 1 | 110 | 0.8 | 1.2 | |
| 2 | 110 | 2 | 2 | 1 |
| 3 | 100 | 1 | 1 | 0.6 |
①此反应在110℃时平衡常数为___。
②实验l中,CCl4的转化率为__。
③判断该反应的正反应是__(填“放热”或“吸热”),理由是__。
④为提高实验3中CCl4的转化率,可采取的措施是__。
a.使用高效催化剂
b.向容器中再投入1molCCl4和1molH2
c.温度升高到200℃
d.向容器中再投入1molHCl
e.向容器中再投入1molH2
-
(13分)无水AlCl3易升华,可用作有机合成的催化剂等。工业上由铝土矿(A12O3、Fe2O3)为原料制备无水AlCl3的工艺流程如下。
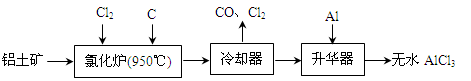
(1)氯化炉中Al2O3、C12和C反应的化学方程式为 。
(2)用Na2SO3溶液可除去冷却器排出尾气中的Cl2,此反应的离子方程式为 ,在标准状况下,吸收112L Cl2需要 molNa2SO3。
(3)工业上另一种由铝灰为原料制备无水AlCl3工艺中,最后一步是由AlCl3·6H2O脱去结晶水制备无水AlCl3,实现这一步的操作方法是在 (填试剂)中加热。
(4)工业上铝土矿经提纯后可冶炼铝,写出在950-970℃和冰晶石作用下进行电解制铝反应的化学方程式 。
-
现代工业常以氯化钠、二氧化碳和氨气为原料制备纯碱,部分工艺流程如下:
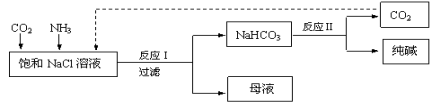
有关说法错误的是
A.反应Ⅰ原理为CO2 + NH3 + NaCl + H2O =NaHCO3↓ + NH4Cl
B.向饱和NaCl溶液中先通入足量的CO2,再通入足量的NH3
C.反应Ⅰ生成的沉淀,经过过滤、洗涤、煅烧可得到纯碱
D.CO2的结构式为O=C=O,其中碳氧原子均满足8电子稳定结构
-
SO2通过下列工艺流程可制备化工原料H2SO4和清洁能源H2
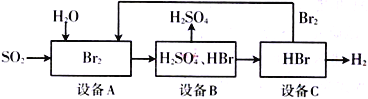
下列说法中不正确的是
A. 设备A中的溴水褪色,体现了SO2的还原性
B. 该生产工艺的优点:Br2可以循环利用,并获得清洁能源H2
C. 该工艺流程的总反应方程式为:SO2+Br2+2H2O=H2SO4+2HBr
D. 设备C中是否残余H2SO4,可在C的样品溶液中加入BaCl2溶液,观察是否有沉淀
-
Ⅰ.苯是一种重要的化工原料,其产品在我们的生活中无处不在。
(1)一定条件下,利用如图所示装置可实现有机物苯(C6H6)到环己烷(C6H12)的转化。
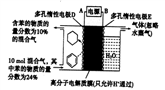
生成目标产物的电极反应式为__________;装置图右侧导出的气体是__________。
(2)已知苯和乙烯可以在催化剂存在的条件下发生加成反应。以苯和乙烯为原料可合成聚苯 乙烯,请设计合成路线(无机试剂及溶剂任选)。合成路线流程图示例如下:
H2C=CH2 CH3CH2Br
CH3CH2Br CH3CH2OH
CH3CH2OH
_________________________________________________________________________
II.丙烯是三大合成材料的基本原料,用于制丙烯腈、环氧丙烷、丙酮、甘油等。下图是以丙烯为原料合成甘油最重要的生产方法。
CH2=CHCH3  C3H5Cl
C3H5Cl  C3H6OCl2
C3H6OCl2 

 甘油
甘油
(3)①的反应类型是:____________
(4)产物C3H6OCl2有两种,选择一种写出反应③的化学方程式:____________
2Cl2(g)+2H2O(g).将HC1和O2分别以5种物质的量比:①1:1 ②2:1 ③4:1 ④6:1 ⑤8:1,向五个容积可变的容器中投料时,反应温度对HCl平衡转化率影响的曲线如图.










 CH3CH2OH
CH3CH2OH