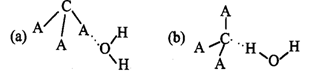-
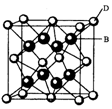
(10分)有A、B、C、D、E、F六种元素。A是宇宙中最丰富的元素;B是周期表中电负性数值最大的元素;C的基态原子中2p轨道有三个未成对的单电子;F原子核外电子数是B与C核外电子数之和;D是主族元素,且与副族元素E同周期;E能分别形成红色(或砖红色)的E2O和黑色的EO两种氧化物;D与B可形成离子化合物,其晶胞结构如右图所示。请回答下列问题。
(1)E元素原子基态时的外围电子排布式为________。
(2)A2F分子中F原子的杂化类型是________,F的气态氧化物FO3分子的键角为。
(3)CA3极易溶于水,其原因是________,试判断CA3溶于水后,形成CA3·H2O的最合理结构为________(选填字母)。
(4)从晶胞结构图中可以看出,D跟B形成的离子化合物的电子式为;
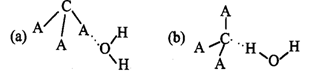
该离子化合物晶体的密度为ρ(g·cm-3)。,则晶胞的体积是(只要求列出算式)。
-
有A、B、C、D、E、F六种元素.A是宇宙中最丰富的元素;B是周期表中电负性数值最大的元素;C的基态原子中2p轨道有三个未成对的单电子;F原子核外电子数是B与C核外电子数之和;D是主族元素,且与副族元素E同周期;E能分别形成红色(或砖红色)的E2O和黑色的EO两种氧化物;D与B可形成离子化合物,其晶胞结构如右图1所示.请回答下列问题.
(1)E元素原子基态时的外围电子排布式为______.
(2)A2F分子中F原子的杂化类型是______,F的气态氧化物FO3分子的键角为______.
(3)CA3极易溶于水,其原因是______,试判断CA3溶于水后,形成CA3•H2O的最合理结构为______(选填字母).
(4)从晶胞结构图1中可以看出,D跟B形成的离子化合物的电子式为______;该离子化合物晶体的密度为ρ.,则晶胞的体积是______(只要求列出算式).
(5)BF3和过量NaF作用可生成NaBF4,BF4-的立体构型为______;
(6)在与石墨结构相似的六方氮化硼晶体中,层内B原子与N原子之间的化学键为______,层间作用力为______.

-
下列有关电负性的说法错误的是
A. 电负性是人为规定的一个相对数值,不是绝对标准
B. 元素电负性的大小反映了元素原子对键合电子吸引能力的大小
C. 一般来说,周期表从左到右,元素的电负性逐渐变大
D. 元素电负性数值越大,其第一电离能越高
-
(10分)1932年美国化学家鲍林首先提出了电负性的概念。电负性(用X表示)也是元素的一种重要性质,下表给出的是原子序数小于20的16种元素的电负性数值:
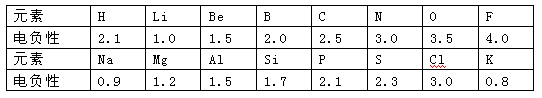
请仔细分析,回答下列有关问题:
①预测周期表中电负性最大的元素应为_____;估计钙元素的电负性的取值范围:________< X <________。
②根据表中的所给数据分析,同主族内的不同元素X的值变化的规律是________
________; 简述元素电负性X的大小与元素金属性、非金属性之间的关系________。
③经验规律告诉我们:当形成化学键的两原子相应元素的电负性差值大于1.7时,所形成的一般为离子键;当小于1.7时,一般为共价键。试推断AlBr3中形成的化学键的类型为________。
-
下列说法正确的是
A. 第一电离能的周期性递变规律是原子半径、化合价、电子排布周期性变化的结果
B. 通常元素的第一电离能为正值,第二电离能为负值
C. 电负性是相对的,所以没有单位
D. 分析元素电负性数值可以看出,金属元素得到电负性较大,非金属元素得到电负性较小
-
在元素周期表中的某些元素之间存在着特殊的“对角线关系”,下列有关说法不正确的是(
A.氢氧化铍是两性氢氧化物
B.B,Si的电负性数值相似
C.Li和Mg的原子半径相近,且核外电子排布相近
D.铍与盐酸或氢氧化钠溶液反应均能产生气体
-
(5分) A、B、C为1~20号元素且原子序数逐渐增大, B和C的单质都能与水剧烈反应,B为电负性数值最大的元素。B单质与水反应产生A单质,0.25molC单质跟水反应时,在标准状况下放出5.6LH2,此时C转化成具有氩原子核外电子层结构的离子。问:
(1)A、B、C各是什么元素?
(2)写出B、C元素所形成的化合物的化学式,并用电子式表示形成过程。
-
已知A、B、C、D、E为元素周期表中前四周期元素,且原子序数依次增大。A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素;E元素位于元素周期表的第11列。
试回答下列有关的问题:
(1)写出基态D原子的外围电子排布式:__________________,E元素位于元素周期表__________________。
(2)A、B、C三种元素的第一电离能最大的是_________(用元素符号表示)。这三种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是______________________________ (写化学式)。
(3)D可形成化合物[D(H2O)6](NO3)3 。①[D(H2O)6](NO3)3中配位体的VSEPR模型名称是__________________。该化合物中阴离子的中心原子的轨道杂化类型为_________。
②1 个 [D(H2O)6]3+ 中含有的σ键数目为_________个。
(4)已知B、C两种元素形成的化合物通常有两种。这两种化合物中________(填化学式)为非极性分子,另一种化合物的电子式为_________。
(5)E+离子能与SCN-离子形成ESCN沉淀。SCN-离子对应的酸有硫氰酸(H―S―C≡N)和异硫氰酸(H―N=C=S),这两种酸沸点更高的是______________(填名称),原因是________________________。
(6)由A、C两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如下图所示为A、C形成化合物的晶胞结构图以及晶胞的截面图,晶胞中距离一个A+最近的A+有_______个,距离一个A+最近的C-围成的图形是______________(写名称)。若晶体密度为ρ g·cm-3,阿伏加德罗常数的值用NA表示,则A+的半径为_________cm(用含NA与ρ的式子表达)。
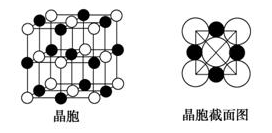
-
已知A、B、C、D、E为元素周期表中前四周期元素,且原子序数依次增大。A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素;E元素位于元素周期表的第11列。试回答下列有关的问题:
(1)写出基态D原子的外围电子排布式:______,E元素位于元素周期表______。
(2)A、B、C三种元素的第一电离能最大的是______ 用元素符号表示
用元素符号表示 。这三种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是______
。这三种元素最高价氧化物的水化物形成的溶液,物质的量浓度相同时,pH由大到小的顺序是______  写化学式
写化学式 。
。
(3)D可形成化合物 。
。
 中配位体的VSEPR模型名称是_____________。该化合物中阴离子的中心原子的轨道杂化类型为_____________。
中配位体的VSEPR模型名称是_____________。该化合物中阴离子的中心原子的轨道杂化类型为_____________。
 个
个 中含有的
中含有的 键数目为______个。
键数目为______个。
(4)已知B、C两种元素形成的化合物通常有两种。这两种化合物中_____________ 填化学式
填化学式 为非极性分子,另一种化合物的电子式为_____________。
为非极性分子,另一种化合物的电子式为_____________。
(5) 离子能与
离子能与 离子形成ESCN沉淀。
离子形成ESCN沉淀。 离子对应的酸有硫氰酸
离子对应的酸有硫氰酸 和异硫氰酸
和异硫氰酸 ,这两种酸沸点更高的是______(填名称),原因是__________。
,这两种酸沸点更高的是______(填名称),原因是__________。
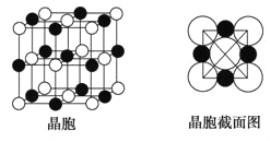
(6)由A、C两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如图所示为A、C形成化合物的晶胞结构图以及晶胞的截面图,晶胞中距离一个 最近的
最近的 有______个,距离一个
有______个,距离一个 最近的
最近的 围成的图形是_____________
围成的图形是_____________ 写名称
写名称 。若晶体密度为
。若晶体密度为
 ,阿伏加德罗常数的值用
,阿伏加德罗常数的值用 表示,则
表示,则 的半径为____________________
的半径为____________________ 用含
用含 与
与 的式子表达
的式子表达 。
。
-
已知:A、B、C、D四种元素,原子序数依次增大。A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素。试回答下列有关的问题:
(1)写出D元素价电子的电子排布式:______________。
(2)D可形成化合物[D(H2O)6](NO3)3 。
①[D(H2O)6](NO3)3中阴离子的立体构型是_____________。NO3-中心原子的轨道杂化类型为__________。
②在[D(H2O)6] 3+中D3+与H2O之间形成的化学键称为______,1 mol [D(H2O)6] 3+ 中含有的σ键有________mol。
(3)已知B、C两种元素形成的化合物通常有两种。这两种化合物中________(填化学式)为非极性分子。另一种物质的电子式为_____________。
(4)由A、C两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如下图所示为A、C形成化合物的晶胞结构图以及晶胞的剖面图:

晶胞中距离一个A+最近的C-有________个,这些C-围成的图形是______________,若晶体密度为ρ g·cm-3,阿伏加德罗常数的值用NA表示,则A+的离子半径为________cm(用含NA与ρ的式子表达)。