-
(10分) 以黄铜矿(主要成份为CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要流程如下:
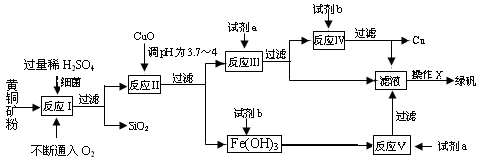
已知:①4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O;
②部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表:
| 沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 6.7 | 3.7 | 9.6 |
(1)试剂a是___________,试剂b是_____________。
(2)操作X应为蒸发浓缩、________________、________________。
(3)反应Ⅱ中加CuO调pH为3.7~4的目的是________
________。
(4)反应Ⅴ的离子方程式为___________________________。
-
(14分)以黄铜矿(主要成份为CuFeS2,含少量杂质SiO2等)为原料,进行生物炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要流程如下:
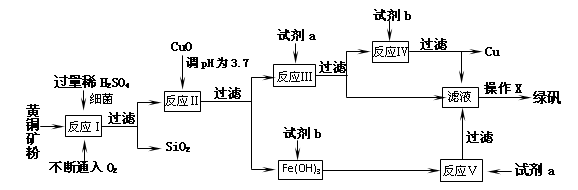

② 部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如下表
| 沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 6.7 | 3.7 | 9.6 |
(1)试剂a是________,试剂b是________(填化学式)。
(2)操作X流程依次为蒸发浓缩、________、过滤、洗涤干燥。
(3)反应Ⅱ中加CuO调pH为3.7的目的是________;
(4)反应Ⅴ的离子方程式为________。
(5)反应①中,每生成1mol Fe2(SO4)3,转移电子的物质的量为mol;
(6)过滤操作中,要用到的玻璃仪器有________、________和漏斗。
-
以黄铜矿(主要成分为CuFeS2,含少量杂质SiO2等)为原料进行炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要流程如下:
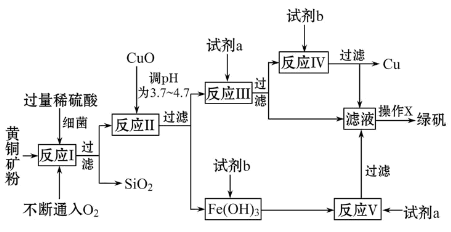
已知:① 4CuFeS2+2H2SO4+17O2=4CuSO4+2Fe2(SO4)3+2H2O
②部分阳离子以氢氧化物形式开始沉淀和完全沉淀时溶液的pH如表
| 沉淀物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 4.7 | 2.7 | 7.6 |
| 完全沉淀pH | 6.7 | 3.7 | 9.6 |
(1)试剂a是__________,试剂b是__________。
(2)操作X应为蒸发浓缩、__________、__________。
(3)反应Ⅱ中加CuO调pH为__________,目的是使Fe3+形成Fe(OH)3沉淀,防止生成Cu(OH)2沉淀。
(4)反应Ⅴ的离子方程式为:__________________________________________。
-
工业上常以铜铁矿(主要成分为CuO和Fe3O4,还含少量SiO2等杂质)为原料,冶炼铜,同时得到副产品绿矾(FeSO4·7H2O)。其主要流程如下
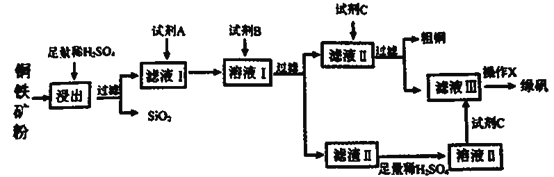
已知:滤渣II的主要成分为Fe(OH)3。请回答下列问题:
(1)如何提高黄铜矿的浸出率___________、___________?(至少答两种方法)
(2)试剂A为___________,其反应的离子方程式为_____________。
(3)试剂B不可能是
A.NH3·H2O B.CuO C.NaOH D.Cu2(OH)2CO3
(4)溶液II中溶质的成分为_______________。
(5)操作X的步骤是________________________。
-
有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)氧化成硫酸盐。运用该原理生产铜和绿矾(FeSO4·7H2O)的流程如下:
回答下列问题:
(1)已知:
| Fe2+ | Cu2+ | Fe3+ |
| 开始转化成氢氧化物沉淀时的pH | 7.6 | 4.7 | 2.7 |
| 完全转化成氢氧化物沉淀时的pH | 9.6 | 6.7 | 3.7 |
(1)加入CuO将溶液的pH调节到约为4,结合平衡移动原理解释该操作的原因________。
(2)写出能实现反应Ⅲ的化学方程式________。
(3)试剂b为________。
(4)欲从滤液中获得绿矾晶体,操作Ⅰ应为浓缩、、 。
(5)反应Ⅰ的化学方程式________。
-
以黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)为原料炼铜的方法有不同的冶炼方法。火法炼铜:将辉铜矿(Cu2S)在空气中高温焙烧即可得到铜和一种还原性的气体。近年来,湿法炼铜有了新进展,科学家发现有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿氧化成硫酸盐。某工厂运用该原理生产铜和绿矾(FeSO4•7H2O)的工艺如下:
回答下列问题:
(1)火法炼铜发生的化学方程式:_________________________;
(2)湿发炼铜工艺流程中,为了提高酸浸时的进取率,本流程可采取的措施是________,试剂X为__________,其作用是_____________。
(3)试剂a为______________,试剂b为______________;
(4)配平反应1的化学方程式:____CuFeS2+___H2SO4+____O2=____CuSO4+____Fe2(SO4)3+____H2O
(5)已知:常温下Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=2.6×10-39。加入过量的试剂X调节pH=4时,可使溶液中的Fe3+转化为Fe(OH)3沉淀,则溶液中的c(Fe3+)=___________。若要此时不出现Cu(OH)2沉淀,则溶液中的Cu2+浓度最大不超过_________________。
-
工业上,以钛铁矿(主要含FeTiO3,还含有Fe2O3 和Al2O3、SiO2等杂质)为原料制备二氧化钛并得到副产品绿矾(FeSO4·7H2O)的工艺流程如下图所示。
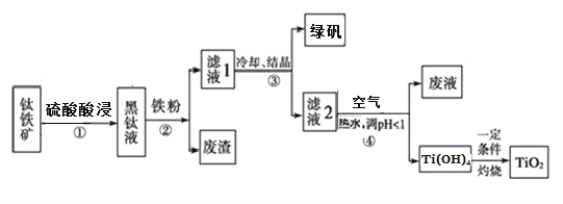
已知:TiO2+在一定条件下会发生水解。
回答下列问题:
(1)要提高酸浸时钛矿石的溶解速率,可行的措施是(写一条即可)_______________。黑钛液中生成的主要阳离子有TiO2+和Fe2+,步骤①主要反应的化学方程式是_________。
(2)步骤②中,加入铁粉的主要作用是_____,同时也会将部分TiO2+还原为Ti3+。
(3)向滤液2中通入空气的目的是______(用离子方程式表示)。
(4)请结合化学用语用化学平衡理论解释步骤④中加入热水稀释将TiO2+转化为Ti(OH)4 的原因:_________________。
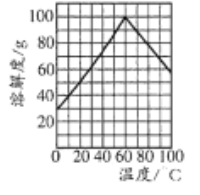
(5)副产品绿矾中含有杂质[Al2(SO4)3]。要将副产品进一步提纯,请结合右图的绿矾溶解度曲线完成提纯过程:将副产品溶于稀硫酸中,充分搅拌后,用NaOH溶液调节反应液的pH约为5,过滤沉淀后得到FeSO4溶液,______,过滤,用冰水洗涤,低温干燥,得到FeSO4·7H20晶体。
(6)用氧化还原滴定法测定制备得到的产品中TiO2的质量分数:在一定条件下,将一定量的产品溶解并将TiO2还原为Ti3+,再以KSCN溶液作为指示剂,用硫酸铁铵[NH4Fe(SO4)2]标准溶液滴定Ti3+至全部生成Ti4+。
①滴定终点的现象是_______________。
②滴定分析时,称取TiO2试样0.2 g,消耗0.1 mol/L NH4Fe(SO4)2标准溶液24.00mL,则TiO2的质量分数为_______________。
-
以黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)为原料炼铜的方法分为高温炼铜和湿法炼铜两种。近年来,湿法炼铜有了新进展,科学家发现有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿氧化成硫酸盐:4CuFeS2+2H2SO4+17O2 4CuSO4+2Fe2(SO4)3+2H2O。某工厂运用该原理生产铜和绿矾的工艺如下:
4CuSO4+2Fe2(SO4)3+2H2O。某工厂运用该原理生产铜和绿矾的工艺如下:
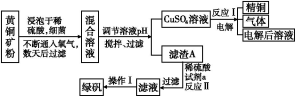
回答下列问题:
(1)下列物质中可以用于上述流程中调节溶液pH的是 (填序号)。
A.Cu;B.Cu2(OH)2CO3;C.H2SO4;D.Fe;E.CuO
(2)滤渣A的主要成分为 (写化学式)。
(3)写出反应Ⅰ的化学方程式: 。
(4)试剂a为 。
(5)欲从溶液中获得绿矾晶体,分离操作Ⅰ应为 (写操作名称)。
(6)生产过程中,除了试剂a、H2O可以循环使用外,还可循环使用的物质有 (写化学式)。
-
以黄铜矿(主要成分是CuFeS2,含少量杂质SiO2)为原料炼铜的方法分为高温炼铜和湿法炼铜两种。近年来,湿法炼铜有了新进展,科学家发现有一种细菌在酸性水溶液、氧气存在下,可以将黄铜矿氧化成硫酸盐,某工厂运用该原理生产铜和绿矾(FeSO4的晶体,含结晶水)。
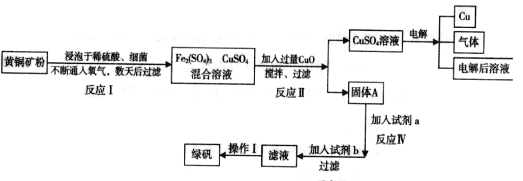
回答下列问题:
(1)写出反应Ⅰ的化学反应方程式:__________________________;
(2)反应II中CuO的作用是_________________________;
(3)写出加入试剂b发生的反应离子方程式_________________________________________;
(4)欲从溶液中获得绿矾晶体,分离操作I应为___________________________;
(5)生产过程中,可循环使用的物质有__________________(写化学式)。
-
(15分)黄铜矿是工业炼铜的主要原料,其主要成分为CuFeS2,现有一种天然黄铜矿(含少量SiO2),为了测定该黄铜矿的纯度,某同学设计了如下实验:
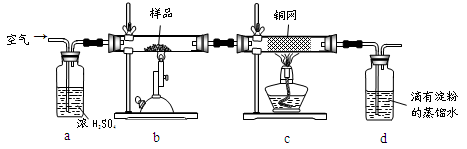
现称取研细的黄铜矿样品1.150g,在空气存在下进行煅烧,生成Cu、Fe3O4和SO2气体,实验后取d中溶液的 置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
置于锥形瓶中,用0.05mol/L标准碘溶液进行滴定,消耗标准溶液20.00ml。请回答下列问题:
(1)称量样品所用的仪器为_____(填“托盘天平”或“电子天平”),将样品研细后再反应,其目的是_______ 。
(2)装置a和c的作用分别是____和____(填标号)。
A除去SO2气体 B除去空气中的水蒸气 C有利于气体混合
D有利于观察空气流速 E除去反应后多余的氧气
(3)上述反应结束后,仍需通一段时间的空气,其目的是___________。
(4)通过计算可知,该黄铜矿的纯度为________。
(5)若用右图装置替代上述实验装置d,同样可以达到实验目的的是____(填序号)。
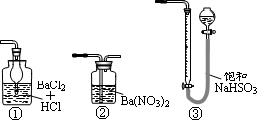
(6)若将原装置d中的试液改为Ba(OH)2,测得的黄铜矿纯度误差为+1%,假设实验操作均正确,可能的原因主要有_____________________________________________。










