-
有A、B、C、D、E五种元素。其相关信息如下:
| 元素 | 相关信息 |
| A | A元素的一种原子没有中子,只有一个质子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道有三个未成对电子 |
| D | D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子 |
| E | E能形成砖红色(红色)的E2O和EO两种氧化物 |
回答下列问题。
(1)写出E元素原子基态时M层的电子排布式 。
(2)C元素单质分子中含有δ和π键的键数之比为 。
(3)解释在水中的溶解度C7H15OH比乙醇低的原因是: 。
(4)A、C、E三种元素可形成:E(CA3)42+配离子,其中存在的化学键类型有 (填序号)。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若 E(CA3)42+具有对称的空间构型.且当 E(CA3)42+中的两个CA3分子被两个Cl取代时.能得到两种不同结构的产物,则 E(CA3)42+的空间构型为 (填序号)。
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(5)三硫化四磷是黄绿色针状结晶,其结构如图所示。
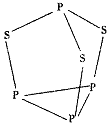
三硫化四磷分子中P原子采取____杂化,与PO3-互为等电子体的化合物分子的化学式为________。用NA表示阿伏加德罗常数的数值,0.1mol三硫化四磷分子中含有的孤电子对数为_________。
-
A、B、C、D是原子序数依次增大的四种短周期主族元素,其相关信息如下表所示
| 元素代号 | 元素相关信息 |
| A | 原子核内无中子,核外只有1个电子 |
| B | 其单质是空气中含量最多的气体 |
| C | 最外层电子数是电子层数的3倍 |
| D | 短周期中原子半径最大的元素 |
试回答下列问题:
(1)写出下列元素名称:A________, C________
(2)B在元素周期表中的位置:第____周期,第_____族。
(3)B、C两种元素的气态氢化物的稳定性强弱为:_____>______(填化学式)。
(4)A、C、D三种元素可以形成离子化合物,该化合物的电子式为_____________。
(5)写出C与D形成的淡黄色化合物的用途(填一种即可)___________________。
-
有A、B、C、D、E五种元素.其相关信息如下:
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有一个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道有三个未成对电子 |
| D | D为主族元素,且与E同周期,其最外层上有两个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和EO两种氧化物 |
请回答下列问题.
(1) B是________(填元素符号), D的简化电子排布式________________
(2) 若[E(CA3)4]2+具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl﹣取代时,能得到两种不同结构的产物,则[E(CA3)4]2+的空间构型为______ (填序号);
a.平面正方形 b.正四面体 c.三角锥型 d.V型
(3)元素E所在的周期,未成对电子数最多的元素是______(填元素符号)
-
X、Y、Z、W、R是前三周期常见元素,T位于第四周期,其相关信息如下表:
| 元素 | 相关信息 |
| X | 宇宙中最丰富的元素 |
| Y | 其单质是空气中最主要的成分 |
| Z | 地壳中含量最高的元素 |
| W | 其原子质量数为23,中子数为12 |
| R | 其最高价氧化物对应的水化物既能与强酸反应,也能与强碱反应 |
| T | 其单质在空气中放置表面会变绿,其常见氧化物有两种,为黑色和砖红色 |
(1)Y、Z、W、R四种元素的原子半径从大到小的顺序是___________(用元素符号表示)。
(2)YX3的电子式为;X 与Z形成一种18e-的分子,其结构式为_____________。
与Z形成一种18e-的分子,其结构式为_____________。
(3)A是人体必需的常量元素,与W同主族,位于第四周期,其原子序数为___________
(4)R在元素周期表中的位置为___________。
(5)T单质可与Y最高价氧化物对应水化物的稀溶液发生反应,该反应的离子方程式为__________。
-
(11分)现有A、B、C、D、E、F、G七种位于周期表前四周期元素,其原子序数依次增大,相关信息如下表所示:
| 元素 | 性质 |
| A | 一种核素的原子核内不含中子 |
| B | 原子核外电子有6种不同运动状态 |
| C | 最高价氧化物的水化物与其氢化物可发生非氧化还原反应 |
| D | 单质之一为淡蓝色气体,可阻挡对人体有害的紫外线 |
| E | 在地壳中的含量位居第三 |
| F | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
| G | 该元素的一种氧化物M可用作油漆颜料,与E的单质反应可应用于焊接钢轨 |
根据以上信息,回答下列问题:
(1)画出元素C的基态原子核外电子排布图: ;G元素位于周期表的 区;
B、C、D三种元素的第一电离能由大到小顺序为: (用元素符号表示)。
(2)化合物BA2D2蒸气293 K时,理论测算密度为2.0g·L-1,实际密度为2.5 g·L-1的原因是 。
(3)FD2中F原子的杂化类型为 ;分子空间构型为 ;FD2易溶于水的原因可能是: (填入序号)。①FD2与水极性相同 ②FD2可以与水反应
(4)有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为:
-
(11分)现有A、B、C、D、E、F六种位于周期表前四周期元素,其原子序数依次增大,相关信息如下表所示:
| 元素 | 性质 |
| A | 一种核素的原子核内不含中子 |
| B | 原子核外电子有6种不同运动状态 |
| C | 最高价氧化物的水化物与其氢化物可发生非氧化还原反应 |
| D | 单质之一为淡蓝色气体,可阻挡对人体有害的紫外线 |
| E | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
| F | 该元素的一种氧化物M可用作油漆颜料,与某单质反应可应用于焊接钢轨 |
根据以上信息,回答下列问题:
(1)画出元素C的基态价电子排布图: ;F元素位于周期表的__ 区;B、C、D三种元素的第一电离能由大到小顺序为: (用元素符号表示)。
(2)化合物BA2D2蒸气293 K时,理论测算密度为2.0g·L-1,实际密度为2.5 g·L-1的原因是 。
(3)ED2中F原子的杂化类型为 ; ED2易溶于水的原因可能是: (填入序号)。
①ED2与水极性相同
②ED2可以与水反应
(4)有人推测化合物CA5的存在,该化合物中含有化学键的可能类型为: 。
-
现有A、B、C、D、E、F六种位于周期表前四周期的元素,其原子序数依次增大,相关信息如下表所示:
| 元素 | 性质 |
| A | 一种核素的原子核内不含中子 |
| B | 原子核外电子有6种不同运动状态 |
| C | 最高价氧化物的水化物与其氢化物可生成盐 |
| D | 单质之一为淡蓝色气体,可阻挡对人体有害的紫外线 |
| E | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
| F | 该元素的一种氧化物可用作油漆颜料,与某单质反应可应用于焊接钢轨 |
根据以上信息,回答下列问题:
(1)F元素位于周期表的____区(填s、p、d、ds或f),B、C、D三种元素的第一电离能由大到小顺序为______________________(用元素符号表示)。
(2)ED2中E原子的杂化类型为__________________;ED2易溶于水的原因可能是___________(填序号)。
①ED2与水极性相同 ②ED2可以与水反应 ③ED2可以与水形成氢键
(3)F元素的一种氯化物常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断该氯化物晶体为________晶体。
(4)F的单质晶体在不同温度下有两种堆积方式(晶胞结构如图所示),面心立方晶胞和体心立方晶胞中实际含有的F原子个数之比为________,其中体心立方晶胞空间利用率为___________(设F原子半径是r,列出含r的计算表达式,不需化简)。
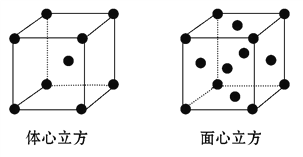
-
现有A、B、C、D、E、F六种位于周期表前四周期的元素,其原子序数依次增大,相关信息如下表所示:
| 元素 | 性质 |
| A | 一种核素的原子核内不含中子 |
| B | 原子核外电子有6种不同运动状态 |
| C | 最高价氧化物的水化物与其氢化物可生成盐 |
| D | 单质之一为淡蓝色气体,可阻挡对人体有害的紫外线 |
| E | 周期表中位于短周期,基态原子M层成对电子数是未成对电子数的2倍 |
| F | 该元素的一种氧化物可用作油漆颜料,与某单质反应可应用于焊接钢轨 |
根据以上信息,回答下列问题:
(1)F元素位于周期表的____区(填s、p、d、ds或f),B、C、D三种元素的第一电离能由大到小顺序为______________________(用元素符号表示)。
(2)ED2中E原子的杂化类型为__________________;ED2易溶于水的原因可能是___________(填序号)。
①ED2与水极性相同 ②ED2可以与水反应 ③ED2可以与水形成氢键
(3)F元素的一种氯化物常温下为固体,熔点282℃,沸点315℃,在300℃以上易升华,易溶于水,也易溶于乙醚、丙酮等有机溶剂,据此判断该氯化物晶体为________晶体。
(4)F的单质晶体在不同温度下有两种堆积方式(晶胞结构如图所示),面心立方晶胞和体心立方晶胞中实际含有的F原子个数之比为________,其中体心立方晶胞空间利用率为___________(设F原子半径是r,列出含r的计算表达式,不需化简)。
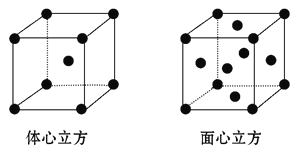
-
(3分)有 A、B、C三种短周期元素。A+只含有一个质子没有中子;B的正、负化合价绝对值相等,在同族元素中其氢化物最稳定;C的原子核内质子数是B的最外层电子数的3.5倍。试推断这三种元素分别是:A____________,B____________,C________。(用元素符号表示)
-
A、B、C、D、E五种常见元素的基本信息如下所示:A元素的一种原子的原子核内没有中子,B是所有元素中电负性最大的元素,C的基态原子2p轨道中有三个未成对电子,D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子,E能形成红色(或砖红色)的E2O和黑色的EO 两种氧化物。请回答下列问题:
(1)写出E元素原子基态时的电子排布式:______________。
(2)C元素的第一电离能比氧元素的第一电离能__________(填“大”或“小”)。
(3)与D元素同周期且未成对电子数最多的元素是__________。
(4)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有___(填字母)。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若[E(CA3)4]2+配离子具有对称的空间构型,且当[E(CA3)4]2+中的两个CA3被两个Cl-取代时,能得到两种不同结构的产物,则[E(CA3)4 ]2+的空间构型为__________(填字母)。
a.平面正方形 b.正四面体形 c.三角锥形 d.V形


