-
原电池的发明是化学对人类的一项重大贡献。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入稀硫酸中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为_________________。
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,若将该反应原理设计成原电池,请写出原电池的正极反应______________________________。
(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示,测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。
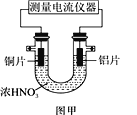

t1s前,原电池的负极是铝片,正极的电极反应式为________,溶液中的H+向______(填“正”或“负”)极移动。t1s后,外电路中电子流动方向发生改变,其原因是_________________。
-
原电池的发明是化学对人类的一项重大贡献。
(1)一种新型燃料电池,它以多孔铂板为两个电极插入稀硫酸中,然后分别向两极通入氢气和氧气而获得电能。通入氢气的电极反应式为________________________。放电一段时间后,负极附近溶液的pH________(填“升高”“降低”或“不变”)。
(2)电子工业上常利用FeCl3溶液腐蚀铜板制作印刷电路,其反应的化学方程式为________________________。请把该反应设计成一个原电池,在方框内面出原电池装置图(要求:标明电极材料和电解质溶液)。_______

(3)常温下,将除去表面氧化膜的铝片、铜片插入浓HNO3中组成原电池装置如图甲所示,测得原电池的电流强度(I)随时间(t)的变化如图乙所示,反应过程中有红棕色气体产生。

t1s前,原电池的负极是铝片,正极的电极反应式为____________,溶液中的H+向________(填“正”或“负”)极移动。t1s后,外电路中电子流动方向发生改变,其原因是________________________。
-
高效能电池的研发制约电动汽车的推广。有一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应为:2C2H6+7O2+8KOH===4K2CO3+10H2O,有关此电池的推断中正确的是( )
A.负极反应为:14H2O+7O2+28e-===28OH-
B.放电过程中KOH的物质的量浓度不变
C.每消耗1 mol C2H6,则电路上转移的电子为14 mol
D.放电一段时间后,负极周围的pH升高
-
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通乙烷和氧气,其电极反应式分别为:2C2H6+36OH?–28e?=4CO32?+24H2O,14H2O+7O2+28e?=28OH?。有关此电池的叙述正确的是
A.电解质溶液中的阴离子向正极移动
B.放电一段时间后,KOH的物质的量浓度不变
C.通乙烷的电极为负极
D.参加反应的O2和C2H6的物质的量之比为2:7
-
一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应为:2C2H6+7O2+8KOH = 4K2CO3+10H2O,有关此电池的推断正确的是
A.负极反应为14H2O+7O2+28e- = 28OH-
B.每消耗1 mol C2H6,则电路上转移的电子为14 mol
C.放电一段时间后,负极周围的pH升高
D.放电过程中KOH的物质的量浓度不变
-
一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气,其总反应为:2C2H6+7O2+8KOH=4K2CO3+10H2O。有关此电池的推断正确的是
A.负极反应为:14H2O+7O2+28e—=28OH—
B.放电一段时间后,负极周围的pH升高
C.理论上消耗1mol C2H6,电路上转移的电子为14mol
D.放电过程中,K+向负极移动
-
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通乙烷(C2H6)和氧气,其电极反应式为: C2H6+18OH--14e-=2CO32-+12H2O,
2H2O+O2+4e-=4OH-,有关此电池的推断不正确的是
A.电池工作过程中,溶液的pH值逐渐减小 B.通乙烷的电极为负极
C.正极与负极上参加反应的气体的物质的量之比为2 :7 D.负极发生氧化反应
-
一种新型的燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极通入乙烷和氧气。有关此电池的推断正确的是
A.负极反应为14H2O+7O2+28e-=28OH-
B.放电一段时间后,负极周围的pH升高
C.每消耗1mol C2H6,则电路上转移的电子为14mol
D.放电过程中KOH的物质的量浓度不变
-
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通乙烷(C2H6)和氧气,其电极反应式为:C2H6+18OH——14e-=2CO32—+12H2O,2H2O+O2+4e-=4OH—,有关此电池的推断不正确的是 ( )
A.正极发生还原反应 B.正极与负极上参加反应的气体的物质的量之比为2∶9
C.通乙烷的电极为负极 D.电池工作过程中,溶液的pH逐渐减小
-
一种新型燃料电池,它以多孔镍板为电极插入KOH溶液中,然后分别向两极上通乙烷(C2H6)和氧气,其电极反应式为:C2H6+18OH--14e-=2CO32-+12H2O,2H2O+O2+4e-=4OH-,有关此电池的推断不正确的是( )
A.电池工作过程中,溶液的pH值逐渐减小
B.通乙烷的电极为负极
C.正极与负极上参加反应的气体的物质的量之比为2:7
D.负极发生氧化反应


