
请回答下列问题:
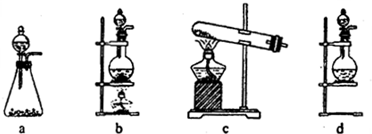
(1)该实验中A部分的装置是______(填写装置的序号)
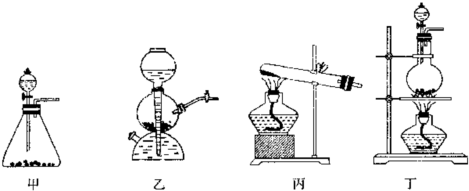
(2)A中发生反应一段时间后,B中的现象是______;整套实验装置存在的明显缺陷是______.
(3)写出D装置中发生反应的离子方程式:______.
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤):______.
高三化学解答题中等难度题


高三化学解答题中等难度题
高三化学解答题中等难度题查看答案及解析


高三化学解答题中等难度题查看答案及解析
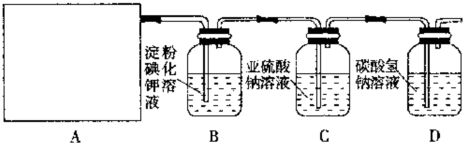
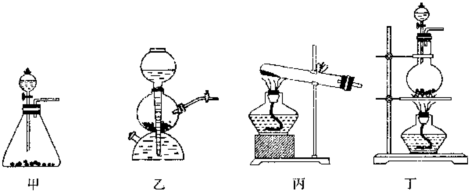
某研究性学习小组同学设计了如下图制取氯气并验证其性质的实验装置。
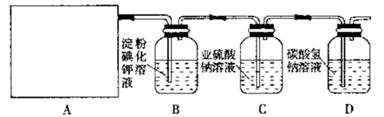
请回答下列问题:
(1)该实验中A部分的装置是________(填写装置的序号)

(2)A中发生反应一段时间后,B中的现象是;
整套实验装置存在的明显缺陷是。
(3)写出D装置中发生反应的离子方程式:________。
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的已被氧化(简述实验步骤):。
高三化学实验题中等难度题查看答案及解析
(10分) 某研究性学习小组同学设计了如下图制取氯气并验证其性质的实验装置。

请回答下列问题:
(1)该实验中A部分的装置是________(填写装置的序号)
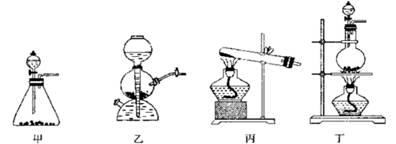
(2)A中发生反应一段时间后,B中的现象是;
整套实验装置存在的明显缺陷是。
(3)写出D装置中发生反应的离子方程式:________。
(4)请你帮该小组同学设计一个实验,证明洗气瓶C中的已被氧化(简述实验步骤):________。
高三化学填空题中等难度题查看答案及解析
(12分) 某研究性学习小组同学设计了如下图制取氯气并验证其性质的实验装置。

请回答下列问题:
(1)该实验中A部分的装置是________(填写装置的序号)
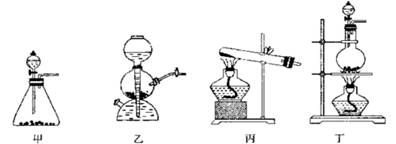
(2)A中发生反应一段时间后,B中的现象是________;
整套实验装置存在的明显缺陷是。
(3)写出D装置中发生反应的离子方程式:________。
(4)写出C装置中发生反应的离子方程式:________。请你帮该小组同学设计一个实验,证明洗气瓶C中的已被氧化(简述实验步骤):________
高三化学实验题简单题查看答案及解析
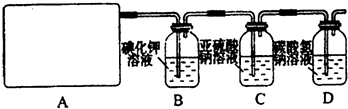
某研究性学习小组为了制取、收集纯净干燥的氯气并探究氯气的性质,他们设计了如图所示的实验装置:
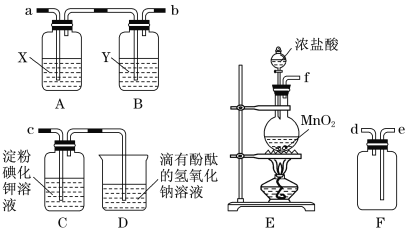
请回答下列问题:
(1)整套实验装置的连接顺序是f接( ) ( )接( )( )接( )(各接口处的字母代号)。_________
(2)E装置中制取氯气的离子方程式是_________________________。
(3)B装置的作用是__________________;A装置中试剂X是________________。
(4)C装置中可观察到的现象是____________。
(5)ClO2和氯气具有相似的性质,用如图装置可以测定某混合气中ClO2 的含量:(其他成分不参与反应)
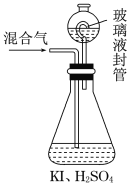
Ⅰ.在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入3 mL稀硫酸;
Ⅱ.在玻璃液封装置中加入水,使液面没过玻璃液封管的管口;
Ⅲ.将一定量的混合气体通入锥形瓶中吸收;
Ⅳ.将玻璃液封装置中的水倒入锥形瓶中;
Ⅴ.用0.100 0 mol·L-1 硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-=2I-+S4O62-),指示剂
显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中:
A. 锥形瓶内ClO2与碘化钾反应的离子方程式为__________________________________。
B. 测得混合气中ClO2的质量为________g。
高三化学实验题中等难度题查看答案及解析
高三化学解答题中等难度题查看答案及解析
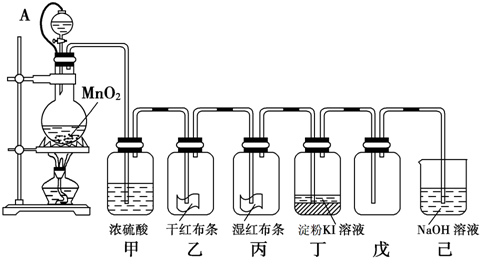
I.某兴趣学习小组设计如图装置制取SO2,研究其性质。

请回答下列问题:
(1)B、C、D分别用于检验SO2 的性质,写出C中反应的离子方程式_______。
(2)实验中观察到D 中有浑浊出现,有同学提出此现象不能证明SO2 具有氧化性,请简述理由________________________。
(3)E装置的作用为______________。
II.某学习小组进一步探究不同浓度的硫酸氧化性不同,设计并完成如下实验:
称取一定量还原铁粉放入一定体积浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。经检验,气体Y 中含有SO2、H2。
(4)溶液X中含有的金属阳离子是(填化学式)_________,简述如何检验该离子______。
(5)为了测定气体Y 中SO2 的含量,将2.24 L( 标准状况)气体Y 通入到200.00mL0.2000mol/L 酸性高锰酸钾溶液中,充分反应后,取出20.00mL溶液转入锥形瓶中进行滴定,消耗0.1000mol/L的KHC2O4标准液10.00mL (高锰酸钾被还原均生成Mn2+ )。
①已知室温下,0.1000mol/L KHC2O4 的溶液中,c(C2O42-) > c(H2C2O4)。滴定操作过程中标准液应用_______(填仪器名称)盛装;滴定终点的现象为____________。
②计算气体Y 中SO2 的物质的量分数为__________。
高三化学实验题中等难度题查看答案及解析
I.某兴趣学习小组设计如图装置制取SO2,研究其性质。

请回答下列问题:
(1)B、C、D分别用于检验SO2 的性质,写出C中反应的离子方程式_______。
(2)实验中观察到D 中有浑浊出现,有同学提出此现象不能证明SO2 具有氧化性,请简述理由________________________。
(3)E装置的作用为______________。
II.某学习小组进一步探究不同浓度的硫酸氧化性不同,设计并完成如下实验:
称取一定量还原铁粉放入一定体积浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y。经检验,气体Y 中含有SO2、H2。
(4)溶液X中含有的金属阳离子是(填化学式)_________,简述如何检验该离子______。
(5)为了测定气体Y 中SO2 的含量,将2.24 L( 标准状况)气体Y 通入到200.00mL0.2000mol/L 酸性高锰酸钾溶液中,充分反应后,取出20.00mL溶液转入锥形瓶中进行滴定,消耗0.1000mol/L的KHC2O4标准液10.00mL (高锰酸钾被还原均生成Mn2+ )。
①已知室温下,0.1000mol/L KHC2O4 的溶液中,c(C2O42-) > c(H2C2O4)。滴定操作过程中标准液应用_______(填仪器名称)盛装;滴定终点的现象为____________。
②计算气体Y 中SO2 的物质的量分数为__________。
高三化学实验题中等难度题查看答案及解析
高三化学解答题中等难度题查看答案及解析