-
X、Y、Z、R、M是原子序数依次增大的五种元素,基态X原子的s电子数比p电子数多3个,Y、Z同周期且相邻,第一电离能:Y>Z,Z、R同主族,M核外电子有29种运动状态,请回答下列问题:
(1)化合物XCl3的中心原子杂化类型为___________;RCl2的立体构型为___________;
(2)H2Z、H2R的沸点分别为100℃、-60.4℃,试解释其原因___________________;
(3)H2RO3的K1和K2分别为1.54×10-2和1.02×10-7,请根据结构与性质的关系解释K1>K2的原因___________________;
(4)Z、M形成的一种化合物晶胞如图所示:
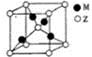
①该化合物的化学式为________________;
②若晶胞参数为apm.列式计算该晶胞的密度ρ=_____________g•cm-3。
-
短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外电子层电子数之比为4:3,Z原子比X原子的核外电子数多4.下列说法正确的是
A. X、Y、Z的第一电离能大小顺序一定是Y>Z>X
B. Y、Z形成的分子的空间构型可能是三角锥形
C. W、X、Y、Z的原子半径大小顺序可能是W>X>Y>Z
D. W、Y、Z氢化物的稳定性一定是Z>Y>W
-
X、Y、Z、W为周期表中前四周期元素,它们的原子序数依次增大。X的基态原子有3个不同的能级,各能级中电子数相等;Y与X同周期,其第一电离能高于同周期与 之相邻的元素;Z的基态原子2p能级上的未成对电子数与X原子相同;W元素原子最外层只有未成对电子,其内层所有轨道全部充满,但并不是第IA族元素。
(1)请写出W原子基态的电子排布式___。
(2)写出X原子价电子的轨道表示式___。
(3)X、Y、Z三种元素第一电离能从大到小的顺序是__ (填元素符号,下同),三种元素的电负性由大到小的顺序是___。
-
A、B、C、D、E五种元素都是前36号元素,原子序数依次增大,其相关信息如下表:
| 元素 | 相关信息 |
| A | A的第一电离能低于同周期左右相邻元素 |
| B | B原子中成对电子数等于未成对电子数的2倍 |
| C | C原子p轨道和s轨道中的电子数相等,与非金属的原子结合时形成共价键 |
| D | D与A、B、C均不同周期,其一个单质分子中只有一个σ键 |
| E | E的原子序数比所处周期中未成对电子数最多的元素大3 |
(1)写出上述一种元素与氢元素形成的X2Y2型非极性分子的结构式:________。
(2)写出E元素的元素符号:________,其价电子排布图为:________。
(3)A与D形成化合物的化学式为________,是________分子(填“极性”或“非极性”)
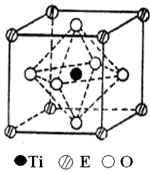
(4)在ETiO3晶胞中(结构如图2所示),1个Ti原子和1个E原子周围距离最近的O原子数目分别为________个、________个.
(5)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3-.N3-的空间构型为________,叠氮化物能与E3+形成配合物,则[E(N3)(NH3)5]SO4中配体是________,E的配位数是________。
-
A、B、C、D、E五种元素都是前36号元素,原子序数依次增大,其相关信息如下表:
| 元素 | 相关信息 |
| A | A的第一电离能低于同周期左右相邻元素 |
| B | B原子中成对电子数等于未成对电子数的2倍 |
| C | C原子p轨道和s轨道中的电子数相等,与非金属的原子结合时形成共价键 |
| D | D与A、B、C均不同周期,其一个单质分子中只有一个σ键 |
| E | E的原子序数比所处周期中未成对电子数最多的元素大3 |
(1)写出上述一种元素与氢元素形成的X2Y2型非极性分子的结构式:_______.
(2)写出E元素的元素符号:______,其价电子排布图为:_______.
(3)A与D形成化合物的化学式为 __,是_______分子(填“极性”或“非极性”)
(4)在ETiO3晶胞中(结构如图所示),1个Ti原子和1个E原子周围距离最近的O原子数目分别为__个、__个.
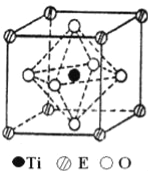
(5)叠氮酸(HN3)是一种弱酸,可部分电离出H+和N3﹣.N3﹣的空间构型为______,叠氮化物能与E3+形成配合物,则[E(N3)(NH3)5]SO4中配体是_____,E的配位数是_____.
-
A、B、C、D、E为前四周期元素,且原子序数依次增大
| A | 第二周期中一种非金属元素,第一电离能大于相邻元素 |
| B | 地壳中含量最多的元素,2P轨道上有二个孤电子 |
| C | 与B同主族 |
| D | 前四周期中金属性最强的元素 |
| E | 前四周期中原子核外孤电子数最多 |
(1)C元素位于第__________________周期__________________族,B元素的核外电子排布式为__________________,E元素的价电子排布图为__________________。
(2)B、C两元素的电负性大小关系为:__________________(用元素符号表示),A、B的最简单气态氢化物的稳定性强弱大小关系为:________________(用氢化物的化学式表示)。
(3)B的氢化物由固体变为气态所需克服的微粒间的作用有__________________。
(4)有A、B、C三种元素及氢元素组成的既含离子键又含共价键且其中元素C显最高价的酸式盐的化学式是__________________。
(5)D2B2的电子式为__________________,与CO2反应生成B的单质的化学方程式为:__________________。
(6)E2O72-具有强氧化性,可与含有C元素的某种还原性离子反应(该离子中C元素显+4价),在酸性条件下该反应的离子方程式为:__________________
-
A、B、C、D、E五种短周期元素,原子序数按A、B、C、D、E依次增大,A元素原子失去1个电子后变为质子,B元素原子的最外层电子数比次外层电子数多2个, C元素原子的最外层电子数是次外层电子数的3倍,D元素原子最外层电子数为1,E元素原子的最高价与负价的绝对值之差为4。试回答:
(1)E元素在元素周期表中的位置是________
(2)由A、C二种元素共同组成的化合物中既含极性键又含非极性键的是________,
只含极性键的是 ________(填化学式)。
(3)D与E可形成化合物,用电子式表示该化合物________
(4)用电子式表示B、C两元素形成稳定化合物的过程________
-
A、B、C、D、E是五种短周期元素。已知:它们的原子序数依次增大,A是元素周期表中原子半径最小的元素;B原子最外层电子数比其次外层电子数多2,C是E的邻族元素;D和E的原子序数之和为30,且D的族序数与周期数相等。甲、乙、丙、丁是它们两两形成的化合物,其中甲分子中含有18个电子。
| 物质组成 | 甲 | 乙 | 丙 | 丁 |
| 化合物中各元素 原子个数比 | A和C 1:1 | B和A 1:4 | D和E 1:3 | B和E 1:4 |
请回答下列问题:
(1)元素E在周期表中的位置为___________________________;
(2)把D的单质放到NaOH溶液中,反应的化学方程式为:_______________________;
(3)用电子式表示甲的形成过程:_________________________;
(4)在密闭容器中充入BC2、BC和乙的混合气体共mg,若加入足量Na2O2,充分振荡并不断用电火花点燃至反应完全,测得固体质量增重mg,则BC2与乙的体积比为________________;
(5)有200mL MgCl2和丙的混合溶液,其中c(Mg2+)= 0.2 mol· L-1,c(Cl-)= 1.3mol·L-1,要使Mg2+全部转化为沉淀分离出来,至少需要4 mol·L-1 NaOH 溶液的体积是:______。
-
A、B、C为原子序数依次增大的同一周期短周期元素,已知A元素的单质既可与盐酸反应,又可与NaOH溶液反应,且均产生氢气;B元素原子次外层电子数比最外层电子数多3,C元素的单质溶于水具有漂白性。
①A元素的元素符号是__________,B的最高价氧化物的化学式为__________;
②B、C两种元素所形成的气态氢化物中最稳定的是__________(用化学式表示);
③写出A、C最高价氧化物对应水化物相互反应的离子方程式__________。
-
(10分)已知A、B、C为同一短周期的三种元素,它们的原子序数依次增大且和为40;A是该周期中(除稀有气体元素外)原子半径最大的元素,B元素的原子核外M层上的电子数比K层上的电子数多1。解答26-30小题:
1.A原子的结构示意图为__________;A元素在周期表中位置为_____________________。
2.写出B的最高价氧化物与A的最高价氧化物对应水化物的溶液之间反应的离子方程式_______________________________________。
3.A和C形成的化合物的电子式为_____________,该化合物的水溶液呈__________性(填“酸”或“碱”)。


