-
(2010•白下区一模)无水硫酸铜(CuSO4)是白色粉末,具有很强的吸水性.吸水后白色粉末转化为蓝色晶体-胆矾(CuSO4•5H2O).
(1)露置在空气中的无水硫酸铜吸收水蒸汽得到胆矾,这一变化过程属于变化(填“物理”或“化学”).
(2)通常状态下,某无色气体可能含有CO2、CO、H2中的一种或几种,依次进行以下实验(假设每步反应均完全进行,且只考虑初中阶段常见的反应):①通过赤热的炭层后,恢复到原状态,气体质量变大;②通过灼热的CuO时,固体变成红色;③通过白色CuSO4粉末时,粉末变成蓝色晶体;④通入澄清石灰水中,石灰水变浑浊.通过以上实验事实可以判定,原混合气体中一定有.
(3)在一定温度下,向一定量的饱和硫酸铜溶液中加入少量无水硫酸铜,一段时间后,观察到白色粉末转变为蓝色晶体,溶液的质量将(选填“增大”、“减小”或“不变”,下同),溶质质量分数将.
(4)某课外研究小组通过下图所示两种不同的途径制取胆矾晶体.
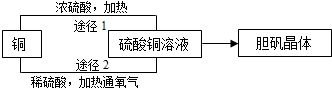
途径1中铜发生反应的化学方程式为“Cu+2H2SO4(浓)≜CuSO4+2H2O+SO2↑”;
途径2中铜发生反应的生成物是硫酸铜和水.
请写出途径2中发生反应的化学方程式:.
与途径1相比,排除安全因素,途径2主要具有两项优点:不污染大气和.
-
无水硫酸铜(CuSO4)是白色粉末,具有很强的吸水性.吸水后白色粉末转化为蓝色晶体-胆矾.
(1)露置在空气中的无水硫酸铜吸收水蒸汽得到胆矾,这一变化过程属于________变化(填“物理”或“化学”).
(2)通常状态下,某无色气体可能含有CO2、CO、H2中的一种或几种,依次进行以下实验(假设每步反应均完全进行,且只考虑初中阶段常见的反应):①通过赤热的炭层后,恢复到原状态,气体质量变大;②通过灼热的CuO时,固体变成红色;③通过白色CuSO4粉末时,粉末变成蓝色晶体;④通入澄清石灰水中,石灰水变浑浊.通过以上实验事实可以判定,原混合气体中一定有________.
(3)在一定温度下,向一定量的饱和硫酸铜溶液中加入少量无水硫酸铜,一段时间后,观察到白色粉末转变为蓝色晶体,溶液的质量将________(选填“增大”、“减小”或“不变”,下同),溶质质量分数将________.
(4)某课外研究小组通过下图所示两种不同的途径制取胆矾晶体.
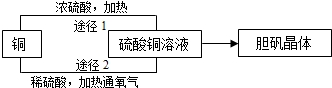
途径1中铜发生反应的化学方程式为“Cu+2H2SO4(浓)≜CuSO4+2H2O+SO2↑”;
途径2中铜发生反应的生成物是硫酸铜和水.
请写出途径2中发生反应的化学方程式:________.
与途径1相比,排除安全因素,途径2主要具有两项优点:不污染大气和________.
-
硫酸铜为白色或灰白色粉末,吸水性很强,吸水后反应生成蓝色的五水合硫酸铜[Cu(H2O)4]SO4·H2O或CuSO4·5H2O],其水溶液因水合铜离子的缘故而呈现出蓝色,故在实验室里无水硫酸铜常被用于检验水的存在。硫酸铜常见的形态为蓝色晶体,即五水合硫酸铜,俗称胆矾或蓝矾,它并不稳定,在加热的条件下,逐渐失去结晶水而变成硫酸铜粉末,给硫酸铜粉末继续加热至650℃高温,可分解为黑色氧化铜、二氧化硫及氧气。
硫酸铜有广泛的应用,如:工业上可用于电镀、定氨催化剂,无水硫酸铜用作脱水剂和气体干燥剂;农业上可与熟石灰混合制农药波尔多液,用于杀菌剂;医疗上可用于检测贫血及作催吐剂。
硫酸铜可以通过不同种方法制得,比如,下面的方法便可以制取硫酸铜。
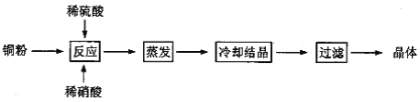
硫酸铜属于重金属盐,有毒,对于人和动物都可因误食一定量而导致死亡,所以用量必须严格控制,若误食,应立即大量食用牛奶、鸡蛋清等富含蛋白质食品,或者使用EDTA钙钠盐解毒。
(1)无水硫酸铜检验水存在的颜色变化是___。
(2)写出一种能制得硫酸铜的化学反应方程式___。
(3)在制备硫酸铜流程中,过滤后的溶液是___硫酸铜溶液(填“饱和”或“不饱和”)
(4)关于硫酸铜说法不正确的是___。
A 五水合硫酸铜的相对分子质量是250。 B 胆矾的化学性质不稳定。
C 无水硫酸铜可作气体干燥剂。 D 硫酸铜的水溶液也称作为波尔多液。
-
无水硫酸铜(CuSO4)是一种白色固体,吸水后可变成蓝色晶体。某气体由H2、CO2、CO、HCl中的一种或几种组成。为探究该气体组成,某化学兴趣小组的同学把该气体依次通过如图所示的试剂(试剂均足量)。观察到的实验现象为:I中澄清石灰水没有变浑浊,Ⅳ中黑色固体变红,V中白色固体变蓝,Ⅵ中澄清石灰水变浑浊。

关于该气体的组成,下列说法正确的是( )
①I中澄清石灰水没有变浑浊,说明原气体中一定不含CO2
②气体通过Ⅱ后,溶液中一定有氯化钠
③Ⅳ中的黑色固体变红,说明原气体中一定含有CO和H2
④V中白色固体变蓝,说明原气体中一定含有H2
⑤原气体中可能含有CO2、HCl
A.①④ B.②③ C.③④ D.④⑤
-
化学小组受英国科学家法拉第《蜡烛的化学史》的启发,对蜡烛的燃烧过程进行了再一次探究。

(查阅资料)
硫酸铜(CuSO4)是一种白色粉末,具有吸水性,吸水后变为蓝色。
(进行实验)

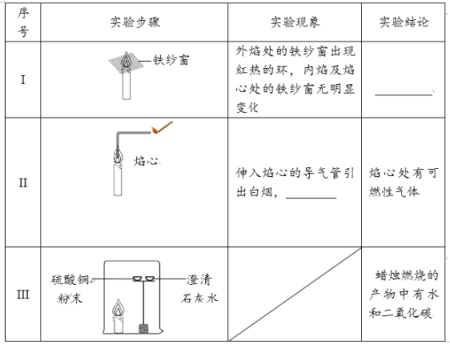
(1)实验I得到的结论是 。
(2)补全实验II的实验现象: 。
(3)实验III中,硫酸铜粉末的作用是 ;得到“蜡烛燃烧的产物中含有二氧化碳”这一结论所对应的实验现象是 。
(4)依据实验III,可以得到的关于蜡烛的元素组成的推论是 。
(反思与评价)
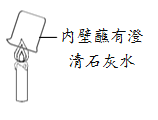
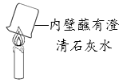
(5)实验III是该小组同学对如右图所示实验的改进。与如图所示实验相比,实验3的优点是 。
-
化学小组受英国科学家法拉第《蜡烛的化学史》的启发,对蜡烛的燃烧过程进行了再一次探究。

【查阅资料】
硫酸铜(CuSO4)是一种白色粉末,具有吸水性,吸水后变为蓝色。
【进行实验】
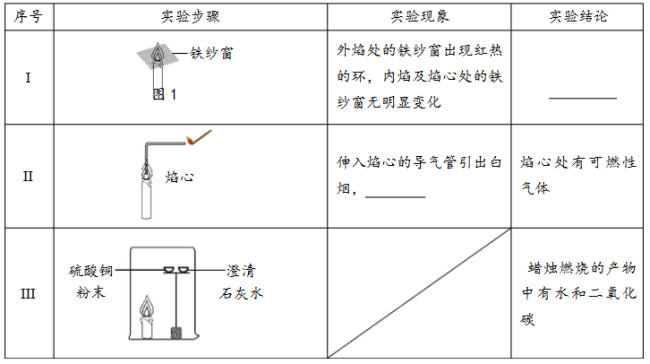
(1)实验I得到的结论是 。
(2)补全实验II的实验现象: 。
(3)实验III中,硫酸铜粉末的作用是 ;得到“蜡烛燃烧的产物中含有二氧化碳”这一结论所对应的实验现象是 。
(4)依据实验III,可以得到的关于蜡烛的元素组成的推论是 。
【反思与评价】
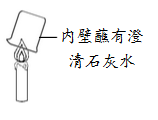
(5)实验III是该小组同学对如右图所示实验的改进。与如图所示实验相比,实验3的优点是 。
-
现在多数家庭使用天然气或液化石油气。液化石油气主要成分是丙烷和丁烷。已知:无水硫酸铜CuSO4遇到水由白色变为蓝色,常用于检验水的存在;浓硫酸具有强吸水性;氢氧化钠溶液能吸收二氧化碳。
(1)写化学式:甲烷CH4、乙烷C2H6、丙烷C3H8、丁烷_____、戊烷C5H12
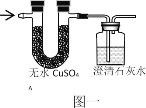
(2)写出丙烷C3H8完全燃烧的化学方程式_____;将丙烷C3H8完全燃烧产物通入“图一”装置,则无水硫酸铜由白色变为____色,澄清石灰水变浑浊的化学反应方程式_____。
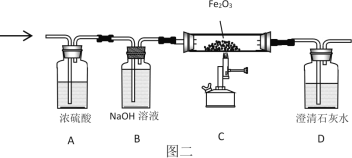
(3)将13.2g丙烷C3H8与38.4g氧气O2充分反应后生成物依次通过“图二”装置;认真阅读下表,回答相关问题:
| 物质 质量 /g | 丙烷C3H8 | 氧气O2 | 装置A | 装置B | X |
| 反应前 | 13.2 | 38.4 | 508.2 | 485.4 | 0 |
| 反应后 | 0 | 0 | 529.8 | 498.6 | a |
①a=_____;求物质X的化学式(写出计算过程)
②写出13.2g丙烷C3H8与38.4g氧气O2充分反应的化学方程式_____。
③装置C中的现象是_____;化学反应方程式是_____。由上可知“图三”装置有一处明显不足_____。
④判断CO2是否被装置B完全吸收的方法:在装置B、C之间增加装有澄清石灰水的洗气瓶,若澄清石灰水_____,则CO2被完全吸收。
⑤若增加氧气的量,则X与H2O的化学计量数之比将_____(填“变大”、“不变”或“变小”)。
-
胆矾是一种蓝色晶体,化学式是CuSO4•5H2O,胆矾受热时易失去结晶水,成为白色的无水CuSO4粉末,无水CuSO4易吸收水份又变成蓝色,在工业上精炼铜、镀铜等都要用胆矾.上述对胆矾的描述中,没有涉及到的是( )
A. 物理性质 B. 用途 C. 制法 D. 化学性质
-
化学小组受英国科学家法拉第《蜡烛的化学史》的启发,对蜡烛的燃烧过程进行了再一次探究。
(查阅资料)
硫酸铜(CuSO4)是一种白色粉末,具有吸水性,吸水后变为蓝色。
(进行实验)
(1)实验I得到的结论是________。
(2)补全实验II的实验现象:________。
(3)实验III中,硫酸铜粉末的作用是________;得到“蜡烛燃烧的产物中含有二氧化碳”这一结论所对应的实验现象是________。
(4)依据实验III,可以得到的关于蜡烛的元素组成中一定含有的元素是________。
(反思与评价)
(5)实验III是该小组同学对如图所示实验的改进。与图所示实验相比,实验3的优点是________
-
阅读下面短文,回答相关问题。
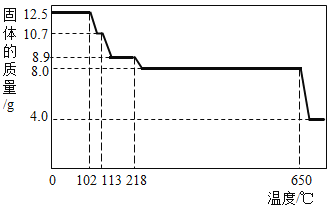
硫酸铜为白色或灰白色粉末,吸水性很强,吸水后反应生成蓝色的五水合硫酸铜[Cu(H2O)4]SO4·H2O或CuSO4·5H2O],其水溶液因水合铜离子的缘故而呈现出蓝色,故在实验室里无水硫酸铜常被用于检验水的存在。硫酸铜常见的形态为蓝色晶体,即五水合硫酸铜,俗称胆矾或蓝矾,它并不稳定,在加热的条件下,逐渐失去结晶水而变成硫酸铜粉末,给硫酸铜粉末继续加热至650℃高温,可分解为黑色氧化铜、二氧化硫及氧气 (如图为胆矾加热过程中固体质量与温度的关系)。
硫酸铜有广泛的应用,如:工业上可用于电镀、定氨催化剂,无水硫酸铜用作脱水剂和气体干燥剂;农业上可与熟石灰混合制农药波尔多液,用于杀菌剂;医疗上可用于检测贫血及作催吐剂。
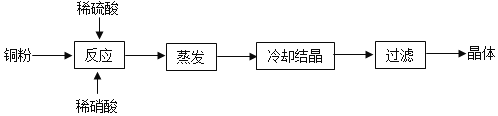
硫酸铜可以通过不同种方法制得,比如,下面的方法便可以制取硫酸铜。
硫酸铜属于重金属盐,有毒,对于人和动物都可因误食一定量而导致死亡,所以用量必须严格控制,若误食,应立即大量食用牛奶、鸡蛋清等富含蛋白质食品,或者使用EDTA钙钠盐解毒。
(1)硫酸铜溶液呈现为蓝色的原因是___。
(2)无水硫酸铜检验水存在的颜色变化是___。
(3)胆矾加热至650℃高温后,发生反应的化学方程式是___。
(4)在制备硫酸铜流程中,过滤后的溶液是___硫酸铜溶液(填“饱和”或“不饱和”)
(5)关于硫酸铜说法正确的是___。
A 五水合硫酸铜的相对分子质量是250
B 胆矾受热至102℃时失去了部分结晶水
C 无水硫酸铜可作气体干燥剂
D 硫酸铜的水溶液也称作为波尔多液















