-
将2molSO2和1molO2混合置于容积为2L的密闭容器中,在800K时,发生如下反应:2SO2(g)+O2(g)⇌2SO3(g)△H<0,当反应从开始进行到5min时,反应达到平衡状态,测得混合气体总物质的量为2.1mol.请回答下列问题:
(1)800K时,该反应的平衡常数为______,在0~5min时间间隔内SO2的反应速率为______.
(2)若在5min时降低温度,在某一时刻重新达到平衡状态,则新平衡混合物中气体的总物质的量______2.1mol(填“>”、“<”或“=”),简述你的判断理由:______.
(3)若相同条件下,向该容器内分别充人xmolSO2、ymolO2和zmolSO3,反应达到平衡时,容器内混合气体总物质的量仍为2.1mol.则:x、y、z必须满足的关系是______.(一个用含x、z的式子表示,一个用含y、z的式子表示)
(4)相同条件下,若在上述容器中,充入0.2mol SO2、0.4mol O2和4.0molSO3三种气体,下列对该反应状态的描述中,正确的是______(填字母序号).
A.处于平衡状态 B.不是平衡状态,反应正向进行 C.不是平衡状态,反应逆向进行.高二化学解答题中等难度题查看答案及解析
-
将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)
2SO3(g) △H<0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1mol.试回答下列问题:
(1)若平衡时,容器体积为aL,写出该反应的平衡常数为:K=__________(用含a的代数式表示)
(2)反应进行到t1时,SO2的体积分数为_______________;
(3)若在t1时充入一定量的氩气(Ar),SO2的物质的量将________(填“增大”、“减小”或“不变”);
(4)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量____2.1mol(填“<”、“>”或“=”),简单说明原因:____________。
(5)若t1达到平衡后,保持容器的体积不再变化。再加入0.2molSO2、0.1molO2和1.8molSO3,此时v逆________v正 (填“<”、“>”或“=”)。
(6)一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g)
2SO3(g)(正反应放热),测得反应的相关数据如下:
容器1
容器2
容器3
反应温度T/K
700
700
800
反应物投入量
2 mol SO2、1 mol O2
4 mol SO3
2 mol SO2、1 mol O2
平衡v正(SO2)/ mol·L-1·s-1
v1
v2
v3
平衡c(SO3)/mol·L-1
c1
c2
c3
平衡体系总压强p/Pa
p1
p2
p3
物质的平衡转化率α
α1(SO2)
α2(SO3)
α3(SO2)
平衡常数K
K1
K2
K3
用“<”、“>”或“=”填入下列横线上:
c2______2c1,v1______v2;K1_____K3,p2____2p3;α1(SO2)_____α3(SO2);α2(SO3)+α3(SO2)_______1
高二化学综合题困难题查看答案及解析
-
将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)
2SO3(g) △H<0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1mol.试回答下列问题:
(1)若平衡时,容器体积为aL,写出该反应的平衡常数为:K=__________(用含a的代数式表示)
(2)反应进行到t1时,SO2的体积分数为_______________;
(3)若在t1时充入一定量的氩气(Ar),SO2的物质的量将________(填“增大”、“减小”或“不变”);
(4)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量____2.1mol(填“<”、“>”或“=”),简单说明原因:____________。
(5)若t1达到平衡后,保持容器的体积不再变化。再加入0.2molSO2、0.1molO2和1.8molSO3,此时v逆________v正 (填“<”、“>”或“=”)。
(6)一定温度下,在三个容积相同的恒容密闭容器中按不同方式投入反应物,发生反应2SO2(g)+O2(g)
2SO3(g)(正反应放热),测得反应的相关数据如下:
容器1
容器2
容器3
反应温度T/K
700
700
800
反应物投入量
2 mol SO2、1 mol O2
4 mol SO3
2 mol SO2、1 mol O2
平衡v正(SO2)/ mol·L-1·s-1
v1
v2
v3
平衡c(SO3)/mol·L-1
c1
c2
c3
平衡体系总压强p/Pa
p1
p2
p3
物质的平衡转化率α
α1(SO2)
α2(SO3)
α3(SO2)
平衡常数K
K1
K2
K3
用“<”、“>”或“=”填入下列横线上:
c2______2c1,v1______v2;K1_____K3,p2____2p3;α1(SO2)_____α3(SO2);α2(SO3)+α3(SO2)_______1
高二化学综合题困难题查看答案及解析
-
将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)
2SO3(g);△H<0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1mol。试回答下列问题:
(1)反应进行到t1时,SO2的体积分数为__;
(2)若在t1时充入一定量的氩气(Ar),SO2的物质的量将__(填“增大”、“减小”或“不变”);
(3)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量_2.1mol(填“<”、“>”或“=”),简单说明原因:__。
(4)若t1达到平衡后,保持容器的体积不再变化。再加入0.2molSO2、0.1molO2和1.8molSO3,此时v逆_v正(填“<”、“>”或“=”)
高二化学填空题中等难度题查看答案及解析
-
将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)
2SO3(g);△H﹤0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1 mol。试回答下列问题:
(1)写出该反应的平衡常数表达式:K = __________;
(2)反应进行到t1时,SO2的体积分数为__________;
(3)若在t1时充入一定量的氩气(Ar),SO2的物质的量将________(填“增大”、“减小”或“不变”);
(4)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量_____2.1mol(填“<”、“>”或“=”),简单说明原因_______________________________;
(5)若其它条件不变,在t1时再加入0.2molSO2、0.1molO2 和1.8molSO3,在图中作出从t0→t1→t2点这段时间内SO2的物质的量变化曲线____________。
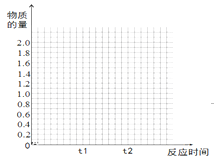
高二化学综合题困难题查看答案及解析
-
将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)
2SO3(g);△H﹤0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1 mol。试回答下列问题:
(1)写出该反应的平衡常数表达式:K =
(2)反应进行到t1时,SO2的体积分数为 ;
(3)若在t1时充入一定量的氩气(Ar),SO2的物质的量将 (填“增大”、“减小”或“不变”);
(4)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量 2.1mol(填“<”、“>”或“=”),简单说明原因 ;
(5) 若其它条件不变,在t1时再加入0.2molSO2、0.1molO2 和1.8molSO3,在图中作出从t0→t1→t2点这段时间内SO2的物质的量变化曲线。
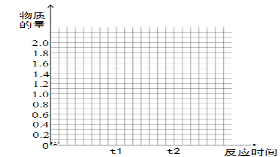
高二化学简答题困难题查看答案及解析
-
将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)
2SO3(g);△H﹤0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1 mol。试回答下列问题:
(1)写出该反应的平衡常数表达式:K =
(2)反应进行到t1时,SO2的体积分数为 ;
(3)若在t1时充入一定量的氩气(Ar),SO2的物质的量将 (填“增大”、“减小”或“不变”);
(4)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量 2.1mol(填“<”、“>”或“=”),简单说明原因 ;
(5)若其它条件不变,在t1时再加入0.2molSO2、0.1molO2 和1.8molSO3,在图中作出从t0→t1→t2点这段时间内SO2的物质的量变化曲线。
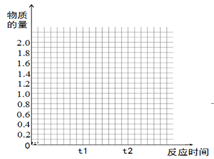
高二化学填空题困难题查看答案及解析
-
Ⅰ.将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)
2SO3(g);△H﹤0,
当反应达到平衡状态,测得混合气体总物质的量为2.1 mol。则平衡时SO2的体积分数为 ;
Ⅱ.某兴趣小组的同学用如图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量),当闭合该装置的电键K时,观察到电流计的指针发生了偏转。当乙池中C极质量减轻10.8 g时,回答下列问题。

(1)甲池中B电极理论上消耗O2的体积(标准状况下) mL。
(2)若丙池中溶液的体积为1000 mL,此时丙池中溶液的pH为 。
高二化学填空题中等难度题查看答案及解析
-
(10分)将2molSO2和1molO2混合置于体积可变,压强恒定的密闭容器中,在一定温度下发生如下反应:2SO2(g)+O2(g)
2SO3(g);△H﹤0,当反应进行到时间t1点时达到平衡状态,测得混合气体总物质的量为2.1 mol。试回答下列问题:
(1)反应进行到t1时,SO2的体积分数为 ;
(2)若在t1时充入一定量的氩气(Ar),SO2的物质的量将 (填“增大”、“减小”或“不变”);
(3)若在t1时升温,重新达到平衡状态,新平衡混合物中气体的总物质的量 2.1mol(填“<”、“>”或“=”),简单说明原因 ;
(4)若其它条件不变,在t1时再加入0.2molSO2、0.1molO2 和1.8molSO3,在图中作出从t0→t1→t2点这段时间内SO2的物质的量变化曲线。
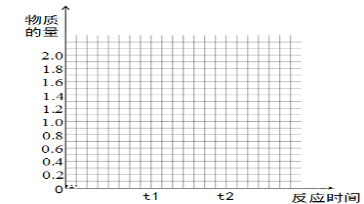
高二化学填空题困难题查看答案及解析
-
将2molSO2 和1molO2充入一容积固定的密闭容器中,在一定条件下发生反应:2SO2(g)+O2(g)
2SO3(g)。下列哪些量不再变化时,不能说明化学反应已达平衡状态( )
A.混合气体的密度 B.混合气体的压强
C.混合气体的总物质的量 D.混合气体的平均相对分子质量
高二化学选择题中等难度题查看答案及解析