下面几种情况,能够形成原电池的是

高二化学选择题中等难度题
下面几种情况,能够形成原电池的是

高二化学选择题中等难度题
下面几种情况,能够形成原电池的是

高二化学选择题简单题查看答案及解析
下面几种情况,能够形成原电池的是( )
A.
B.
C.
D.
高二化学单选题简单题查看答案及解析
下面几种情况,能够形成原电池的是

高二化学选择题中等难度题查看答案及解析
以葡萄糖为燃料可以形成微生物燃料电池(酸性电解质体系中)。关于该电池的叙述正确的是( )
A.该电池能够在高温下工作
B.电池的负极反应为: C6H12O6+6H2O - 24e—= 6CO2↑+24H+
C.放电过程中,H+从正极区向负极区迁移
D.在电池反应中,每消耗1mol氧气,理论上生成标准状况下CO2气体(22.4/6)L
高二化学选择题简单题查看答案及解析
铝及其化合物在生活、生产中有广泛应用。
(1)Al与NaOH溶液能够形成原电池,写出该电池的负极反应式________。Al的原子结构示意图为_______。不能电解A1的氯化物来生产Al,原因是________;
(2)Na3AlF6是冰晶石的主要成分,冰晶石常作工业冶炼铝的助熔剂。工业上用HF、Na2CO3和A1(OH)3制备冰晶石。写出制备冰晶石的化学方程式________。上述反应不能在玻璃容器中反应,其原因是__________(用化学方程式表示)。
(3)明矾[KA1(SO4)2·12H2O]常作净水剂。在明矾溶液中滴加氢氧化钡溶液至Al3+恰好完全沉淀,写出该反应的离子方程式_______________。
(4)铝合金广泛用于建筑材料。等质量的铁、铝、硅组成的同种合金分别与足量盐酸、足量烧碱溶液反应,产生气体体积相等(同温同压)。则该合金中铁、硅的质量之比为________(已知:Si+2NaOH+H2O=Na2SiO3+2H2↑ )
(5)铝氢化钠(NaAlH4)是有机合成的重要还原剂。它的制备方法是将氢化钠和氯化铝在乙醚中反应制备铝氢化钠。
①写出化学方程式_____________;
②在化学上,含包还原剂的还原能力用“有效氢”表示,“有效氢”含义是单位质量的含氢还原剂的还原能力相当于多少克氢气。一般地含氢还原剂的氢被氧化成H2O,“还原能力”用氢失去电子数多少表示。NaAlH4、NaH的“有效氢”之比为___________。
高二化学综合题中等难度题查看答案及解析
下面能够构成原电池及电极反应式正确的是
A.Fe、Cu、浓硝酸溶液,负极反应式为:Fe-2e-==Fe2+
B.Al、Cu、稀硫酸,负极反应式为:Cu-2e-==Cu2+
C.Al、Mg、NaOH溶液,负极反应式为:Al+4OH--3e-==AlO2-+2H2O
D.Zn、Cu、乙醇,负极反应式为:Zn-2e-==Zn2+
高二化学选择题中等难度题查看答案及解析
以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,供LED发光,装置如下图所示。
某实验兴趣小组做完实验后,在读书卡片上记录如下:

(1)在卡片上,记录合理的是(填序号)。
(2)其他条件相同情况下,产生气泡的速率比单一锌片(填“快”或“慢”),如果将锌片换成铁片,电路中的电流方向(填“变”或“不变”)。
(3)如果把硫酸换成硫酸铜溶液,猜测(填“锌片”或“铜片”)变厚,原因是(用电极方程式表示)。实验结束后称得两极质量差12.9g,假设初始时Zn片与Cu片质量相等,则反应中转移的电子的物质的量为mol。
(4)有同学利用原电池原理,将A、B、C、D四种金属设计成下表中装置进行实验用以判断四种金属的活泼性强弱。
| 序号 | 甲 | 乙 | 丙 |
| 装置 |
|
|
|
| 现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据以上现象,判断四种金属活泼性由强到弱的顺序是。
高二化学填空题困难题查看答案及解析
(1)下列各种情况,在其中Fe片腐蚀由快到慢的顺序是 .
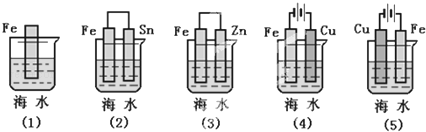
(2)钢铁容易生锈的主要原因是因为钢铁在炼制过程中混有少量的碳杂质,在潮湿的空气中容易形成原电池,发生电化学腐蚀.在空气酸度不大的环境中负极反应式为 ;正极反应式为 .
高二化学填空题中等难度题查看答案及解析
下面关于水解应用的说法错误的是
A.用热水溶解纯碱能够提高去油污的效果
B.配制氯化铁溶液时滴加几滴稀盐酸可以防止氢氧化铁形成
C.硫酸铵和草木灰混合施用到农田可以增强肥效
D.盐碱地(含NaCl、 Na2 CO3)施加适量石膏可以降低土壤的碱性
高二化学选择题中等难度题查看答案及解析
利用碳纳米管能够吸附氢气,设计一种新型二次电池,其装置如图所示。关于该电池的叙述不正确的是( )
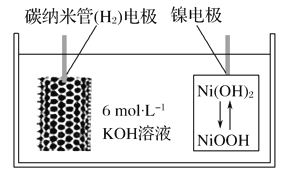
A. 电池放电时K+移向正极
B. 电池放电时负极反应为:H2-2e-+2OH-===2H2O
C. 电池充电时镍电极上NiOOH转化为Ni(OH)2
D. 电池充电时碳纳米管电极与电源的负极相连
高二化学单选题中等难度题查看答案及解析