工业上用粗盐(含Ca2+、Mg2+、等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示,下列有关说法正确的是( )
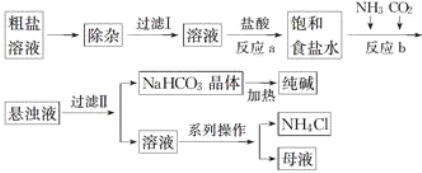
A. 在“侯氏制碱法”中涉及到了氧化还原反应
B. 饱和食盐水中先通入的气体为CO2
C. 流程图中的系列操作中一定需要玻璃棒
D. 工艺中只有碳酸氢钠加热分解产生的CO2可回收循环利用
高二化学单选题中等难度题
工业上用粗盐(含Ca2+、Mg2+、等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示,下列有关说法正确的是( )

A. 在“侯氏制碱法”中涉及到了氧化还原反应
B. 饱和食盐水中先通入的气体为CO2
C. 流程图中的系列操作中一定需要玻璃棒
D. 工艺中只有碳酸氢钠加热分解产生的CO2可回收循环利用
高二化学单选题中等难度题
工业上用粗盐(含Ca2+、Mg2+、等杂质)为主要原料采用“侯氏制碱法”生产纯碱和化肥NH4Cl,工艺流程如下图所示,下列有关说法正确的是( )

A. 在“侯氏制碱法”中涉及到了氧化还原反应
B. 饱和食盐水中先通入的气体为CO2
C. 流程图中的系列操作中一定需要玻璃棒
D. 工艺中只有碳酸氢钠加热分解产生的CO2可回收循环利用
高二化学单选题中等难度题查看答案及解析
(1)海水中有丰富的食盐资源,工业上以粗食盐水(含少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3。流程如下:
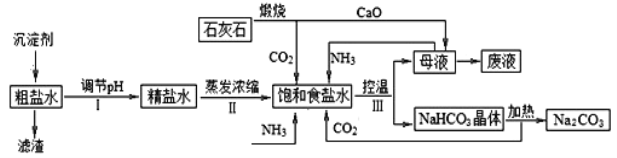
请回答:
①粗盐精制过程中加入的沉淀剂是石灰乳和纯碱,加入顺序是_____。
②上述流程中循环使用的物质是____。
③上图中制得的饱和食盐水还可用于氯碱工业,NaCl 溶液的电解产物可用于生产盐酸、漂白粉、氢氧化钠等产品。工业上电解饱和食盐水的离子方程式为_____。
④氨气可用电解法合成,其原料转化率大幅度提高, 有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图 1 和图 2 所示。
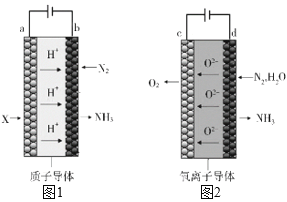
图 1 中,a 电极上通入的X 为_____。图 2 中,d 电极上的电极反应式为_________。
(2)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图 3 所示:

图 3
①金属锂在电极_____(填“A”或“B”)上生成。
②阳极产生两种气体单质,电极反应式是_____。
③某种锂离子二次电池的总反应为:FePO4(s)+Li(s) LiFePO4(s) , 装置如下图所示(a 极材料为金属锂和石墨的复合材料)。下列说法不正确的是_____。
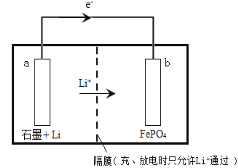
A.图中 e-及 Li+移动方向说明该电池处于放电状态
B.该电池中a 极不能接触水溶液
C.充电时 a 极连接外接电源的正极
D.充电时,b 极电极反应式为:LiFePO4-e-= Li++ FePO
高二化学综合题困难题查看答案及解析
氧化铁黄(化学式为FeOOH)是一种黄色颜料,工业上用废铁为主要原料生产氧化铁黄的一种工艺流程如下:

(1)氧化铁黄中铁元素的化合价为 ,废铁在反应前常用热的纯碱溶液清洗表面油污,其原理是 (写离子方程式)。
(2)氧化过程生成氧化铁黄的化学方程式是 。
(3)上述流程中,检验“洗涤”是否完全的方法是 。
(4)氧化时应控制pH的合理范围是3.5-4.0,pH过小导致氧化铁黄产率较低的可能原因是 。
(5)取1g样品进行纯度测试,将其溶解于足量稀盐酸中,后用一定浓度的过量NaOH溶液沉淀其中的铁元素,得到沉淀的质量为Bg,试用所给数据求出产品的纯度 。
高二化学实验题中等难度题查看答案及解析
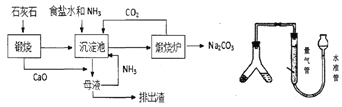
索氏制碱又称氨碱法,其主要生产流程如左下图:

(1)粗盐中常含Ca2+、Mg2+、SO42-等杂质离子,可依次加入NaOH、____、____、盐酸试剂来进行提纯。
(2)用化学方程式表示沉淀池中发生的反应为________________________________。
(3)氨碱法制得的纯碱样品中可能会含有MaCl杂质。现用量气法测定纯碱样品的纯度,(如右上图)如何检查该装置的气密性_________________________________,称取m克样品装入Y型管左侧,量气管中液体应为______________(填字母)。
A.水 B.饱和食盐水 C.饱和碳酸钠溶液 D.饱和碳酸氢钠溶液
(4)若最后测得产生CO2气体的体积为VL(标况下),则样品中纯碱的纯度为_________。若最后读数时,发现水准管液面高于量气管(其他操作都正确),则计算所得纯碱样品的纯度值_____(填“偏大”,“偏小”或“无影响”)。
高二化学填空题中等难度题查看答案及解析
索氏制碱又称氨碱法,其主要生产流程如左下图:
(1)粗盐中常含Ca2+、Mg2+、SO42-等杂质离子,可依次加入NaOH、____、____、盐酸试剂来进行提纯。
(2)用化学方程式表示沉淀池中发生的反应为________________________________。
(3)氨碱法制得的纯碱样品中可能会含有MaCl杂质。现用量气法测定纯碱样品的纯度,(如右上图)如何检查该装置的气密性_________________________________,称取m克样品装入Y型管左侧,量气管中液体应为______________(填字母)。
A.水 B.饱和食盐水 C.饱和碳酸钠溶液 D.饱和碳酸氢钠溶液
(4)若最后测得产生CO2气体的体积为VL(标况下),则样品中纯碱的纯度为_________。若最后读数时,发现水准管液面高于量气管(其他操作都正确),则计算所得纯碱样品的纯度值_____(填“偏大”,“偏小”或“无影响”)。
高二化学填空题中等难度题查看答案及解析
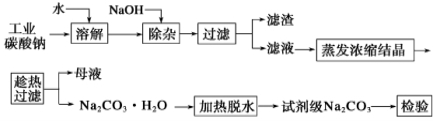
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺流程如下:
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
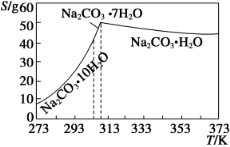
回答下列问题:
(1)滤渣的主要成分为_____________________________。
(2)“趁热过滤”的原因是_________________________。
(3)若在实验室进行“趁热过滤”,可采取的措施是________(写出一种)。
(4)已知:Na2CO3·10H2O (s)===Na2CO3(s)+10H2O(g) ΔH1= +532.36 kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2= +473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式____________。
高二化学填空题简单题查看答案及解析
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺流程如下:
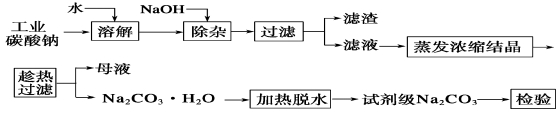
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
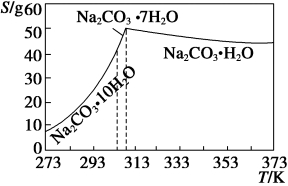
回答下列问题:
(1)滤渣的主要成分为_______________________________。
(2)“趁热过滤”的原因是___________________________。
(3)若在实验室进行“趁热过滤”,可采取的措施是_____(写出一种)。
(4)已知:Na2CO3·10H2O (s)===Na2CO3(s)+10H2O(g) ΔH1= +532.36 kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2= +473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式____________。
高二化学实验题简单题查看答案及解析
(12分)工业上用闪锌矿(主要成分为ZnS,还含有CdS、Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:(已知Cd的金属活动性介于Zn和Fe之间)
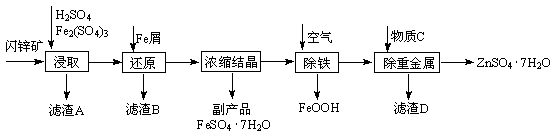
(1)从滤渣A中可获得一种淡黄色非金属单质的副产品,其化学式为 。
(2)浸取时Fe2(SO4)3与ZnS发生反应的化学方程式为 。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为 。
该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是 。
(4)置换法除去重金属离子Cd2+,所用物质C为 。
(5)取28.70 g ZnSO4·7H2O加热至不同温度,剩余固体的质量变化如图所示。
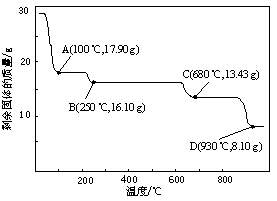
680℃时所得固体的化学式为 。
a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4·H2O
高二化学填空题困难题查看答案及解析
工业上用闪锌矿(主要成分为ZnS,还含有Fe2O3等杂质)为原料生产ZnSO4·7H2O的工艺流程如下:
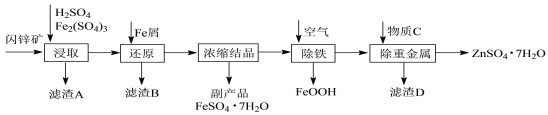
(1)滤渣A经CS2提取后可获得一种淡黄色副产品,其化学式为____。
(2)浸取过程中Fe2(SO4)3的作用是________ (氧化剂或还原剂)。
(3)除铁过程控制溶液的pH在5.4左右,该反应的离子方程式为_________。该过程在空气入口处设计了一个类似淋浴喷头的装置,其目的是________。
(4)置换法除重金属离子所用物质C为___________。
高二化学工业流程中等难度题查看答案及解析
(12分)碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl—和SO等杂质,提纯工艺路线如下:已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示。

回答下列问题:
(1)滤渣的主要成分为 。
(2)“趁热过滤”的原因是 。
(3)若“母液”循环使用,可能出现的问题及其原因是 ________ 。
(4)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g) ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g) ΔH1=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式 ________ 。
高二化学填空题简单题查看答案及解析