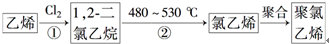-
纯碱(Na2CO3)在生产生活中具有广泛的用途。以下是实验室模拟制碱原理制取Na2CO3的流程图
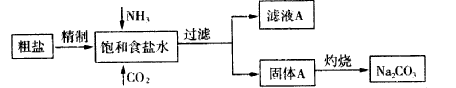
请回答以下问题:
(1)粗盐中含有的杂质离子有Ca2+,Mg2+,SO42-等。粗盐溶解之后,依次加入下列药品:
足量NaOH溶液、 、 除杂,然后过滤,向滤液中加入适量盐酸得到精制食盐水。
(2)向饱和食盐水中通氨气和二氧化碳反应的方程式为: 。
(3)可以区别A固体和Na2CO3固体的方法有 。
A.利用热稳定性不同,加热固体并将生成的气体通入澄清石灰水中,观察是否有浑浊
B.将相同浓度的盐酸逐滴滴入相同浓度的上述固体的溶液中,观察气体产生的速率
C.向相同浓度的两种固体的溶液中滴入酚酞试液,观察溶液颜色的深浅
D.取两种固体配成的溶液,分别加入BaCl2溶液,观察是否有固体生成
E.取两种固体配成的溶液,分别加入Ba(OH)2溶液,观察是否有固体生成
F.取两种固体配成的溶液,分别测量溶液的pH值并比较大小
(4)检验滤液A中含有的阳离子的方法为______________________________。
-
铜及其化合物在生产生活中用途广泛。回答下列问题:
(1)目前,低压甲醇铜基催化剂的主要组分是CuO、ZnO和Al2O3,下列氧原子电子排布图表示的状态中,能量最高的是__(填序号)。
A.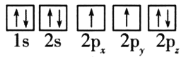 B.
B.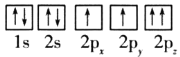
C.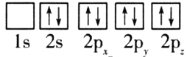 D.
D.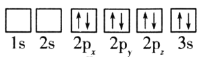
(2)铜离子是人体内多种酶的辅因子,某化合物与Cu+结合形成如图所示的离子。
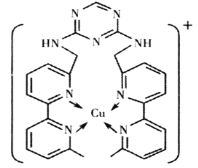
①该离子中含有化学键的类型有___(填序号)。
A.极性键 B.离子键 C.非极性键 D.配位键
②H、N、Cu三种元素的电负性由大到小的顺序是___。H、N、Cu三种元素形成单质其熔点由低到高顺序为___。
(3)某磷青铜晶胞结构如图所示:

①其中原子坐标参数A为(0,0,0);B为(0, ,
, )。则P原子的坐标参数为___。
)。则P原子的坐标参数为___。
②该晶体中距离Cu原子最近的Sn原子有__个,这些Sn原子所呈现的构型为___。
-
碘及其化合物在生产生活中应用广泛。回答下列问题:
(1)单质碘与氟反应可得IF5,实验表明液态IF5具有一定的导电性原因在于IF5的自偶电离(如:2H2O⇌H3O++OH-),IF5的自偶电离方程式为__。
(2)亚硫酸钠和碘酸钾在酸性溶液中的反应是:Na2SO3+KIO3+H2SO4→Na2SO4+K2SO4+I2+H2O(未配平)该反应过程的机理较复杂,一般认为分为以下几步:
①IO3-+SO32-→IO2-+SO42-(慢)
②IO2-+SO32-→IO-+SO42-(快)
③5I-+6H++IO3-→3I2+3H2O(快)
④I2+SO32-+H2O→2I-+SO42-+2H+(快)
根据上述条件推测,此反应的总反应速率由___步反应决定(填序号)。若预先加入淀粉溶液,由题述看必在___离子消耗完时,才会有淀粉变蓝的现象产生。
(3)离子的吸附是重要的研究课题

①已知SO2与I2的反应,速率极快且平衡常数大。溶液中存在如下平衡:I2(aq)+I-(aq)⇌I3-(aq)现将1molSO2缓通入含1molI2的水溶液中至恰好完全反应,溶液中I3-的物质的量n(I3-)时间(t)的变化曲线如图1所示。开始阶段,n(I3-)逐渐增大的原因是___。
②科研小组用新型材料Ag/TiO2对溶液中碘离子进行吸附研究。如图2是不同pH条件下,碘离子吸附效果的变化曲线。据此推断Ag/TiO2材料最适合吸附___(填“酸性”“中性”或“碱性”)溶液中的I-。
③氯化银复合吸附剂也可有效吸附碘离子。氯化银复合吸附剂对碘离子的吸附反应为:I-(aq)+AgCl(s)⇌AgI(s)+Cl-(aq),反应达到平衡后溶液中c(Cl-)=0.10mol•L-1。则溶液中c(I-)=__mol•L-1。[k(AgCl)=2.0×10-10,k(AgI)=8.4×10-17]
(4)Fe3+与I-在溶液中发生反应:2Fe3++2I-⇌2Fe2++I2,该反应的正反应速率和Fe2+与I-的浓度关系为v=k•cm(I-)•cn(Fe3+)(其中k为常数)。T℃时,实验测得c(I-)、c(Fe3+)与反应速率的关系如下表:
| c(I-)/mol·L-1 | c(Fe3+)/mol·L-1 | v/mol·L-1·s-1 |
| ① | 0.20 | 0.80 | 0.032k |
| ② | 0.60 | 0.40 | 0.144k |
| ③ | 0.80 | 0.20 | 0.128k |
在v=k•cm(I-)•cn(Fe3+)中m、n的值为___(填序号)
A.m=1、n=1 B.m=1、n=2 C.m=2、n=2 D.m=2、n=1
-
(12分)过渡金属在生产生活中的应用十分广泛。
Ⅰ.Cr元素形成的氯化铬酰(CrO2Cl2)有重要用途,在有机合成中可作氧化剂或氯化剂,能与许多有机物反应。
Ⅱ.Cu可形成多种配合物,根据下列信息回答问题:
(1)向盛有硫酸铜水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液,请写出先后发生的离子方程式
;
。
深蓝色溶液中配离子的立体构型为 。
(2)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为 。
(3)根据以上实验过程,判断NH3和H2O与Cu2+的配位能力:NH3 H2O(填“>”、“=”或“<”);
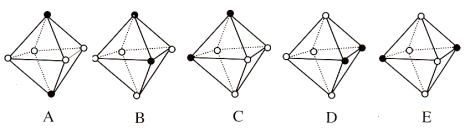
Ⅲ.Ni(CO)6为正八面体结构,其中的镍原子位于正八面体的中心,配位体CO分子则在正八面体的六个顶点上。
(4)若把其中两个CO配位体换成 NH3 得到新的配合物,则以下物质中互为同分异构体的是 。(填字母编号,任填一组。图中黑点为NH3,圆圈为CO,Ni略去)
-
碳及其化合物在能源、材料等方面具有广泛的用途。回答下列问题:
(1)碳酸和草酸均为二元弱酸,其电离分为两步进行,已知其电离常数的有关数据如下表:向Na2CO3溶液中滴加草酸溶液,开始时所发生反应的离子方程式为 。
| H2CO3 | H2C2O4 |
| K1 | 4.2×10-7 | 5.4×10-2 |
| K2 | 5.6×10-11 | 5.4×10-5 |
(2)常温时,C和CO的燃烧热△H分别为-394.0 kJ·mol-1、-283.0 kJ·mol-1,该条件下C转化为CO的热化学方程式为 。
(3)氢气和一氧化碳在一定条件下可合成甲醇,反应如下
2H2(g)+CO(g) CH3OH(g) △H=Q kJ·mol-1。
CH3OH(g) △H=Q kJ·mol-1。
①该反应在不同温度下的化学平衡常数(K)如下表:
| 温度(℃) | 250 | 300 | 350 |
| K(L2·mol-1) | 2.041 | 0.270 | 0.012 |
由此可判断Q 0(填“>”、“=”或“<”)
②一定温度下,将6 mol H2和2mol CO充入到体积为2 L的密闭容器中,10 min时反应达到平衡状态,此时测得c(CO)=0.2 mol·L-1,该温度下的平衡常数K= 。0~10 min内,反应速率v(CH3OH)= 。
③在两个密闭容器中分别都充入20 mol H2和10 mol CO,测得一氧化碳的平衡转化率随温度(T)、压强(p)的变化如下图所示:
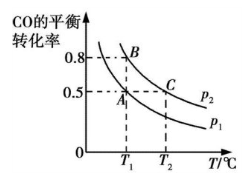
A、B两点压强大小关系:p1 p2(填“>”、“=”或“<”)。若A点对应容器的容积为20 L,则B点对应的容器的容积为 L。
-
电解原理在生产生活中应用广泛,请回答下列问题:
(1)①电解法制备金属铝的化学反应方程式为___。
②为了防止铁器被腐蚀常用电解法在其表面镀铜,此时铁器应与电源__极相连;电解精炼铜时,粗铜应与电源__极相连。
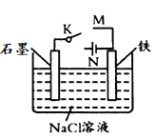
③利用如图装置,可以模拟铁的电化学防护。为减缓铁的腐蚀,开关K应置于__处。
(2)用石墨电极电解100mLH2SO4和CuSO4的混合溶液,通电一段时间后,阴、阳两极分别收集到2.24L和3.36L气体(标况下),溶液想恢复至电解前的状态可加入___。
A.0.2molCuO和0.1molH2O B.0.1molCuCO3
C.0.1molCu(OH)2 D.0.1molCu2(OH)2CO3
(3)汽车尾气排放的CO、NOx等气体是大气污染的主要来源,NOx也是雾霾天气的主要成因之一。利用反应NO2+NH3→N2+H2O(未配平)消除NO2的简易装置如图所示。
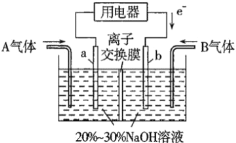
①电极a的电极反应式为___。
②常温下,若用该电池电解0.6L1mol/L的食盐水,当消耗336mLB气体(标况下)时电解池中溶液的pH=__(假设电解过程溶液体积不变)。
-
Na2CO3的制取方法及Na2CO3和NaHCO3综合实验探究
Ⅰ. (1)我国化学家侯德榜改革国外的纯碱生产工艺,其生产流程可简要表示如下:
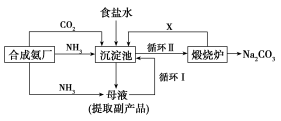
①往饱和食盐水中依次通入足量的NH3、CO2(氨碱法),而不先通CO2再通NH3的原因是_______________________________________________。
②写出沉淀池中反应的化学方程式_______________________________________________。
Ⅱ.某实验小组探究Na2CO3和NaHCO3的性质,发现实验室里盛放两种固体的试剂瓶丢失了标签。于是,他们先对固体A、B进行鉴别,再通过实验进行性质探究。
(2)分别加热固体A、B,发现固体A受热产生的气体能使澄清石灰水变浑浊。A受热分解的化学方程式为_______________________________________________。
(3)称取两种固体各2 g,分别加入两个小烧杯中,再各加10 mL蒸馏水,振荡,测量温度变化;待固体充分溶解,恢复到室温,向所得溶液中各滴入2滴酚酞溶液。
①发现Na2CO3固体完全溶解,而NaHCO3固体有剩余,由此得出结论:_______________________。
②同学们在两烧杯中还观察到以下现象。其中,盛放Na2CO3的烧杯中出现的现象是________(填字母序号)。
a.溶液温度下降
b.溶液温度升高
c.滴入酚酞后呈浅红色
d.滴入酚酞后呈红色
(4)同学们将两种固体分别配制成0.5 mol·L-1的溶液,设计如下方案并对反应现象做出预测:
| 实验方案 | 预测现象 | 预测依据 |
| 操作1:向2 mL Na2CO3溶液中滴加1 mL 0.5 mol·L-1 CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO浓度较大,能与CaCl2发生反应:Ca2++CO===CaCO3↓ (离子方程式) |
| 操作2:向2 mL NaHCO3溶液中滴加1 mL 0.5 mol·L-1 CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO浓度很小,不能与CaCl2反应 |
实施实验后,发现操作2的现象与预测有差异:产生白色沉淀和气体,则该条件下,NaHCO3溶液与CaCl2溶液反应的离子方程式为________________。
-
按要求回答下列问题:
(1)卤代烃在生产生活中具有广泛的应用,如多氯代甲烷常为有机溶剂,其中分子结构为正四面体的是 ,工业上分离这些多氯代物的方法是 。
(2)用系统命名法命名下列有机物

(3)2—甲基—1—丙醇的结构简式为 。
-
卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)有一种多氯代甲烷为常用有机溶剂,其分子结构为正四面体,它是______(写化学式)
(2)聚四氟乙烯稳定、无毒,是不粘锅的涂层,它的结构简式是________________
(3)已知乙二酸俗名草酸,在工业上有广泛的用途,根据下列合成路线填空:

分别写出反应②③的化学反应方程式:________;_____________。
(4)按要求完成下列问题:在 ①苯 ②乙醇 ③甲苯 ④氯乙烷 ⑤ ⑥
⑥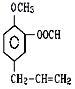 ⑦
⑦ 七种物质中(填编号):
七种物质中(填编号):
①能和金属钠反应放出H2的有________;
②常温下能与溴水化学反应的有________;
③能使酸性KMnO4溶液褪色的有________。
-
卤代烃在生产生活中具有广泛的应用,回答下列问题:
(1)多氯代甲烷常为有机溶剂,其中分子结构为正四面体的是 ,工业上分离这些多氯代物的方法是 。
(2)三氟氯溴乙烷(CF3CHClBr)是一种麻醉剂,写出其所有同分异构体的结构简式 (不考虑立体异构)。
(3)聚氯乙烯是生活中常用的塑料,工业生产聚氯乙烯的一种工艺路线如下:
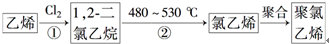
反应①的化学方程式为 ,反应类型为 ;反应②的反应类型为 。

 B.
B.
 D.
D.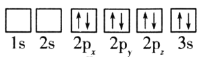










 ⑦
⑦