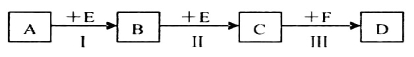-
下图是我们熟悉的元素周期表,请回答下列问题:

(1)在上面元素周期表中画出金属元素与非金属元素的分界线。
(2)在上面元素周期表中全部是金属元素的区域为________(填序号)。
A.A B.B C.C D.D
(3)①写出表示含有8个质子、10个中子的原子的化学符号:________。
②周期表中位于第8纵行的铁元素属于第________族。
③周期表中最活泼的非金属元素位于第________纵行。
④所含元素超过18种的周期是第________、________周期。
(4)根据NaH的存在,有人提议可将氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,又可将氢元素放在周期表中的________族。
-
下图是金字塔式元素周期表的一部分(元素周期表的另一种画法),图上标有第VIA族和几种元素的位置。请回答下列问题:
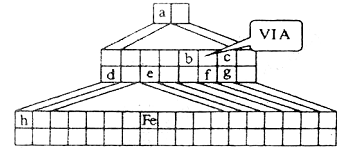
(1)请在上图中描出金属与非金属的分界线,并将铁元素所在族的位置全部涂黑。
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第VIIA族,理由是:氢的最外层电子“饱和缺一”。请用电子式表示LiH:________。
(3)f与c或g均能形成一些化合物,据有关材料f与c能形成化合物fc6,f能与g形成化合物f2g。请回答下面问题:
①甲同学通过分析认为fc6此物质不可在O2中燃烧,原因是________。
通过测定知此物质中的6个c原子在分子结构中化学环境相同,则fc 6分子空间构型为________。
②乙同学通过分析认为f2g2是分子晶体,试写出其结构简式:________;
该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液。试写出该过程的反应方程式:________。
(4)下列叙述正确的是( )
A.h的最高价氧化物对应的水化物是一种强碱。
B.硒化氢的稳定性强于f的氢化物的稳定性。
C.c与h形成化合物的水溶液显中性。
D.离子半径:f>g>h>d
E.f与d形成离子化合物为电解质,故该晶体能导电。
F.a、d、e常见氧化物熔沸点高低比较:e>d>a。
-
(A)

⑴ 在上面元素周期表中画出金属元素与非金属元素的分界线
⑵ 根据NaH的存在,有人提议可把氢元素放在VIIA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的____________族。
⑶ 现有甲、乙两种元素,甲元素原子核外3p亚层上有5个电子,乙元素的焰色反应为黄色。
① 用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
② 甲元素与硫元素相比较,非金属性较强的是______________(填名称),
写出可以验证该结论的一个化学反应方程式___________________________________。
(B)

⑴ 在上面元素周期表中全部是金属元素的区域为___________。
(a)A (b)B (c)C (d)D
⑵ 有人认为形成化合物最多的元素不是IVA族的碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是______________。
⑶ 现有甲、乙两种短周期元素,室温下,甲元素单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
① 用元素符号将甲、乙两元素填写在上面元素周期表中对应的位置。
② 甲、乙两元素相比较,金属性较强的是______________(填名称),
可以验证该结论的实验是_____________________________。
(a)将在空气中放置已久的这两种元素的块状单质分别放入热水中
(b)将这两种元素的单质粉末分别和同浓度的盐酸反应
(c)将这两种元素的单质粉末分别和热水作用,并滴入酚酞溶液
(d)比较这两种元素的气态氢化物的稳定性
-
如图是金字塔式元素周期表的一部分(元素周期表的另一种画法),图上标有第VIA族和几种元素的位置.请回答下列问题:
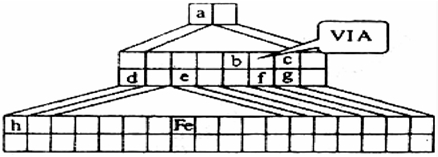
(1)请在上图中描出金属与非金属的分界线,并将铁元素所在族的位置全部涂黑.
(2)自从周期表诞生以来,关于氢元素在周期表中的位置,一直存在纷争,有人主张把它放在第VIIA族,理由是:氢的最外层电子“饱和缺一”.请用电子式表示LiH:______.
(3)f与c或g均能形成一些化合物,据有关材料f与c能形成化合物fC6,f能与g形成化合物f2g.请回答下面问题:
①甲同学通过分析认为fC6此物质不可在O2中燃烧,原因是______.
②乙同学通过分析认为F2g2是分子晶体,试写出其结构简式:______;
该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液.试写出该过程的反应方程式:______.
(4)a和f形成化合物a2f,a2f分子中f原子轨道的杂化类型为______,a2f分子空间构型为______.
(5)下列叙述正确的是______
A.h的最高价氧化物对应的水化物是一种强碱.
B.硒化氢的稳定性强于f的氢化物的稳定性.
C.c与h形成化合物的水溶液显中性.
D.离子半径:f>g>h>d
E.f与d形成离子化合物为电解质,故该晶体能导电.
F.a、d、e常见氧化物熔沸点高低比较:e>d>a.
-
下图为元素周期表的另一种画法——塔式周期表,上面标有部分族及部分元素。请根据周期表中所列的元素回答问题:
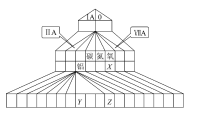
(1)碳、氮、氧三种元素的电负性由小到大的顺序为_____________________。
(2)Y3+的结构示意图为_____________,Z的价电子排布式为_______________。
(3)原子簇是由几个到几百个原子组成的相对独立的物质结构单元,如铝原子簇Al13、Al14。已知原子簇价电子总数为2,8,20,34,40,58……时,原子簇可稳定存在。
①Al13的化学性质与第__________族元素性质相似
②Al14达到稳定时,呈现的化合价为+2,其原因是___________________。
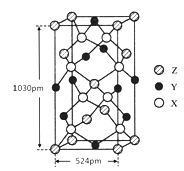
(4)某种化合物由X、Y、Z三种元素组成,其晶胞结构如图所示,则其化学式为____________,该晶胞上下底面为正方形,侧面与底面垂直,根据图中所示的数据列式计算该晶体的密度:ρ=_______g・cm-3(只要求列出计算式)。
-
(16分)
有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y.已知两元素最高价氧化物的水化物均为强酸.根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
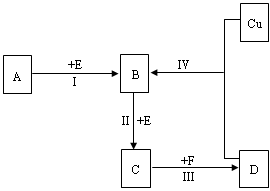
(1)若A、B、C、D均为含X元素的化合物,且A的一个分子中只含有10个电子,则:
①A的分子构型为________。
②反应Ⅰ的化学方程式为________。
③化合物NaX3是合成“达菲”的中间活性物质,NaX3受撞击后生成Na3X和另一种气体单质,请写出该反应的化学方程式________。
(2)若A、B、C、D均为含Y元素的化合物,且A的摩尔质量为120 g·mol ,则:
,则:
①反应Ⅳ的溶液加热蒸干所得的晶体属于________晶体(填“离子”、“分子”、“原子”).
②反应I的化学方程式为________。
③若灼烧6gA产生的B(气态)全部转化为C(气态)时放出9.83 KJ热量,请写第Ⅱ步反应的热化学方程式________。
-
有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸。根据下图转化关系(反应条件及部分产物已略去),回答下列问题:

(1)若A、B、C、D均为含X元素的化合物,且A的一个分子中只含有10个电子,则:
①A分子的空间构型为。
②反应I的化学方程式为________。
③化合物NaX3是合成“达菲”的中间活性物质,NaX3受撞击后生成Na3X和另一种气体单质,请写出该反应的化学方程式________。
(2)若A、B、C、D均为含Y元素的化合物,且A的摩尔质量为120g·mol—1,则:
①将反应IV所得的溶液加热蒸干得到的晶体属于________晶体(填“离子”、“分子”、“原子”)
②反应I的化学方程式为________。
③含Y元素的化合物Na2Yx和次氯酸钠溶液在强碱性环境中能发生反应,产物无沉淀,请写出该反应的离子反应方程式________。
-
有两种位于短周期的相邻周期、相邻主族的非金属元素X、Y,已知两元素最高价氧化物的水化物均为强酸。根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
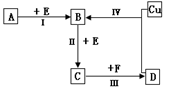
(1)若A、B、C、D均为含X元素的化合物,且A、F的一个分子中都只含有10个电子,则:
①A分子的空间构型为________,F分子的电子式为________。
②反应 I 的化学方程式为________。
③化合物NaX3是合成“达菲”的中间活性物质,也是汽车安全气囊中的主要物质。NaX3受撞击后生成Na3X和另一种气体单质,请写出该反应的化学方程式________。
④ X的氧化物是形成光化学烟雾原因之一,工业上可采用它与其氢化物反应生成无毒害物质而除去,请用方程式表示该反应 ________。
(2)若A、B、C、D均为含Y元素的化合物,其中A由两种元素组成,且A的摩尔质量为120g·mol–1,则:
①将反应IV所得的溶液加热蒸干得到的晶体属于________晶体(填“离子”、“分子”、“原子”)
②反应 I 的化学方程式为________。
③含Y元素的化合物Na2Y和次氯酸钠溶液在强碱性环境中能发生反应,产物无沉淀,请写出该反应的离子反应方程式________。
-
非金属元素在化学中具有重要地位,请回答下列问题:
(1)下图的氮循环是生态系统物质循环的重要部分,人类活动加剧了氮循环中的物质转化。
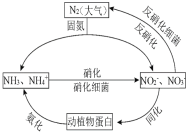
①N在元素周期表中的位置_________, 的立体构型__________。
的立体构型__________。
②反硝化过程中,CH3OH可作为反应的还原剂,1mol还原剂失去6mol电子,被氧化为两种常见离子。请将该反应的离子方程式补充完整:__CH3OH+__
 ___+___+___+___ 。
___+___+___+___ 。
(2)砷及其化合物有重要的用途。
③砷(As)简化的电子排布式___,AsH3的熔沸点比NH3的 ___(填“高”或“低”),原因是____。
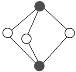
④雌黄(As2S3)在我国古代常用作书写涂改修正液。分子结构如下图,则砷原子的杂化方式为_____。
⑤砷化镓(GaAs)的熔点为1238℃,密度为ρ g·cm-3,其晶胞结构如图所示。
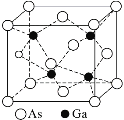
距Ga原子最近且等距的As原子个数为____,GaAs的摩尔质量为M g·mol-1,阿伏加德罗常数值为NA,则该晶胞边长为___pm。
-
(12分)已知两种相邻周期、相邻主族的短周期非金属元素X、Y,其最高价氧化物的水化物均为强酸。根据下图转化关系(反应条件及部分产物已略去),回答下列问题:
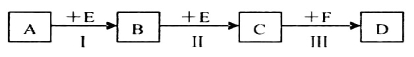
(1)若A、B、C、D均为含X元素的化合物,且A和F的分子均为10电子微粒,则:
①F属于____________(填“离子化合物”或“共价化合物”)。
②反应I的化学方程式为____________________________________________。
③将1.92g铜粉与一定量的D的浓溶液反应,当铜粉完全反应时收集到气体1.12L(标准状况),则反应消耗的D的物质的量为________________mol。
(2)若A、B、C、D均为含Y元素的化合物,其中A由两种元素组成,且A的摩尔质量为34g mol
mol ,则:
,则:
①将铜粉与D的浓溶液反应所得溶液加热蒸干,得到的白色固体物质为_______(填化学式)。
②将少量Na2Y溶液滴加到次氯酸钠溶液中发生反应,无沉淀生成,请写出该反应的离子反应方程式_______________________。在该反应中若有74.5 g NaClO被还原,则转移电子的物质的量为_________mol。