-
(1)基态Ga原子中能量最高的能层符号________ 有______ 种不同能量的电子,Ga元素与同周期相邻元素Zn、Ge相比,第一电离能从大到小的顺序__________,(用元素符号表示)金属Zn晶体采用六方最密堆积,其密置层堆积方式为__________ (ABABAB或ABCABC)区分晶体和非晶体最可靠的科学方法是________________。
(2)磷有三种含氧酸 H3PO2 、 H3PO3 、 H3PO4 其中磷原子均以sp3杂化与相邻原子形成四个α 键,则①H3PO3的结构式是__________;②写出H3PO2 与足量强氧化钠溶液反应的化学方程式_________;③三种酸的强弱顺序为H3PO2 <H3PO3 < H3PO4,其原因是___________;④HNO3 、 HNO2 中心原子的杂化方式分别为__________。
(3)金属铜投入氨水或过氧化氢溶液中均无明显现象,但投入氨水和过氧化氢的混合溶液中,则铜片溶解,溶液呈深蓝色。①写出该反应的离子反应方程式____________________________ ;②已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,原因是_______________。
高二化学综合题困难题查看答案及解析
-
H、C、N、O、V(钒)五种元素形成的某分子结构如图所示,下列说法错误是
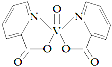
A.N原子核外存在3种不同能量的电子
B.基态V原子的价电子轨道表示式为
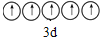
C.基态O原子,电子占据的最高能级符号为2p
D.基态C、N两种原子中,核外存在相同对数自旋方向相反的电子
高二化学单选题中等难度题查看答案及解析
-
(12分)硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)(4分)Ga与B同主族,Ga的基态原子核外电子排布式为 B与同周期相邻两元素第一电离能由大到小的顺序是
(2)硼酸(H3BO3)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
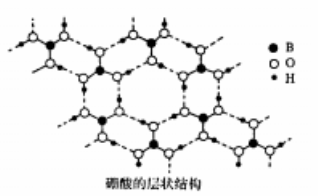
①硼酸中B原子的杂化轨道类型为 。
②硼酸晶体中存在的作用力有范德华力和 。
③加热时,硼酸的溶解度增大,主要原因是 。
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OHˉ 而呈酸性。写出硼酸的电离方程式_ 。
(3)立方氮化硼是一种新型陶瓷材料,结构和形体都类似金刚石,是现时所知的几乎最硬的物质,化学式为BN,则立方氮化硼中B原子的杂化轨道类型为 ;1mol立方氮化硼中B-N的物质的量为 。
高二化学填空题困难题查看答案及解析
-
现有X、Y、Z三种短周期元素,原子序数依次增大,它们原子的最外层电子数之和为20,X、Y是同周期相邻元素,Y、Z是同主族相邻元素.写出它们的元素符号:X______、Y______、Z______.
高二化学解答题中等难度题查看答案及解析
-
X、Y、Z、W为原子序数依次增大的短周期主族元素,已知X、Y为同周期的相邻元素且形成的某种二元化合物能形成光化学烟雾,Z为金属元素且Z原子的L层电子数比其它各层上电子数之和大5,W的最高价氧化物对应水化物和其氢化物均为强酸。下列说法不正确的是
A. X、Y、Z、W原子半径大小:W>Z>Y>X B. 最简单氢化物的稳定性:X<Y
C. WY2能对自来水进行杀菌消毒 D. Z单质在Y单质和W单质中均可燃烧
高二化学单选题中等难度题查看答案及解析
-
X、Y、Z、W四种元素的部分信息如下表所示。
元素
X
Y
Z
W
相关
信息
短周期元素,最高化合价为+7价
基态原子中,电子占据的最高能层符号为L,最高能级上只有两个自旋方向相同的电子
核外电子共有15种运动状态
能与X形成两种常见化合物WX2、WX3,酚遇WX3溶液能发生显色反应
回答下列问题:
(1)W的基态原子电子排布式为___,X、Y、Z三种元素电负性由大到小的顺序为___(用具体的元素符号填写)。
(2)化合物YX4、ZX3、ZX5(气态或液态时)中,中心原子的轨道类型不是sp3杂化的是___ (填化学式,下同),分子构型是正四面体的是___,ZX3属于___(极性分子、非极性分子)。
(3)已知WX3的熔点:306℃,沸点:319℃,则WX3的晶体类型为___。
(4)Z原子的价电子轨道表示式为___。
(5)W元素的单质晶体在不同温度下有两种堆积方式,晶胞分别如图所示。在面心立方晶胞中W原子的配位数为___;若W的原子半径为rcm,阿伏加德罗常数为NA,则其体心立方晶体的密度可表示为___g•cm-3。
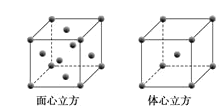
高二化学推断题中等难度题查看答案及解析
-
(14分)A、B、C、D四种元素处于同一周期。在同族元素中,A的气态氢化物沸点最高,B的最高价氧化物对应水化物的酸性在同周期中最强,C的电负性介于A、B之间,D与B相邻。(1)C原子的价电子排布式为___________________
(2)A、B、C三种原子的第一电离能由大到小的顺序是(写元素符号)_____________。
(3)B的单质分子中存在①________个
键;D的最简单气态氢化物分子中的中心原子轨道采用②________杂化。B和D形成一种超硬、耐磨、耐高温的化合物,该化合物属于③_______晶体,其硬度比金刚石
④ ________(填“大”或“小”)。
(4)A的气态氢化物的沸点在同族中最高的原因____________________________________。
高二化学填空题中等难度题查看答案及解析
-
在周期表中相邻的短周期元素X、Y、Z、W,它们的原子序数依次增大。X与Z同主族,并且原子序数之和为20。W原子的最外层电子数比Y多2个。下列叙述正确的是
A.Y的最高价氧化物可与氢氧化钠溶液反应
B.最高价氧化物的水化物酸性 Z>X
C.气态氢化物的稳定性 Z>W
D.原子半径 Z>Y
高二化学选择题简单题查看答案及解析
-
⑴某元素原子的价电子构型为3s23p3,它属于第__ __周期,是__ _ 族,最高正化合价为__ __,元素名称是_ 。
⑵某元素原子的价电子构型为3s2,它是___ ___区元素,元素符号为 _ 。
⑶某元素原子的价电子构型为3d104s2,它属于第 _ 周期,是 _族, _ 区元素,元素符号是 。
高二化学填空题简单题查看答案及解析
-
元素的原子结构决定其性质和在周期表中的位置,下列说法正确的是( )
A. 元素原子的最外层电子数等于元素的最高化合价
B. 多电子原子中,在离核较近的区域内运动的电子能量较高
C. 元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
D. Si、P、S得电子能力和最高价氧化物对应水化物的酸性均依次增强
高二化学选择题中等难度题查看答案及解析