-
某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的探究实验,他们提出下列实验方案——气体分析法。
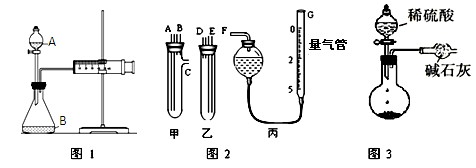
(1)甲同学用图1所示装置,把Xg的混合物与足量稀硫酸反应后,测定产生的CO2气体的体积。实验开始时检查该装置气密性的方法是________。
(2)乙同学用图2代替图1中的发生、收集装置,甲、乙两试管各有两根导管,用橡胶管连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体,则Na2CO3、NaCl的固体混合物和稀硫酸应分别置于 、 仪器中(填仪器编号);
G管可以用化学实验室里的一种常用仪器来替代,你认为这种仪器的名称是 ;仪器甲、乙接口的连接方式如下:A连接________,B连接________,C连接 ;(填写各
接口的编号)
(3)丙同学用图3装置测定CO2的质量,该装置存在明显缺陷,从而导致实验误差,请你分析其中使测定结果可能偏大的主要原因________;
使测定结果可能偏小的主要原因________;
(上述偏大、偏小的原因各写一条)
-
某校化学小组的同学开展测定Na2CO3和NaCl的固体混合物中Na2CO3质量分数的实验,他们提出下列实验方案。
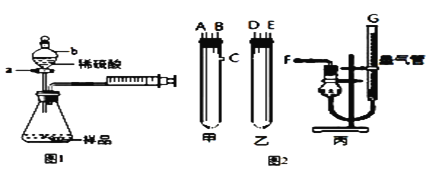
(1)甲同学用图1装置,把m g的混合物样品与足量稀硫酸反应后,测定产生的CO2气体的体积,检查该装置的气密性时,某同学将注射器活塞拉出一定距离,___,说明该装置的气密性好;当锥形瓶内不再产生气泡时立即读数,测定结果 ___(填 “偏大”、“偏小”、“无影响”)。
(2)乙同学用图2装置,Na2CO3、NaCl的固体混合物样品和稀硫酸应分别置于甲和乙中,导管连接方式如下:A连接____,B连接____,C连接_____(填写各接口的字母编号)。
-
某校化学小组的同学开展测定Na2SO3和NaCl的固体混合物中Na2SO3质量分数的探究实验,他们提出下列实验方案:

(1)小明同学用图中的发生、收集装置。甲、乙两试管各有两根导管,连接对应接口后,倒置盛稀硫酸的试管,发生反应,放出气体。则稀硫酸应置于____中(填“甲”或“乙”);G管可以用化学实验室里的一种常用仪器代替,你认为这种仪器的名称是____。仪器甲、乙接口的连接方式如下:A连接___,C连接F;(填写接口的编号)
(2)小李同学用沉淀法测定Na2SO3的质量分数。
操作流程:
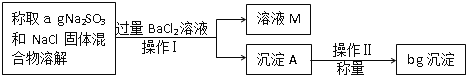
①操作Ⅱ的名称是_______。
②操作Ⅰ之前,为判断所加BaCl2溶液是否过量, 设计如下方案,其中最合理的是___。
A.取少量上层清液,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
B.待浊液澄清后,继续滴加BaCl2,若无沉淀产生则说明BaCl2已过量。
C.待浊液澄清后,继续滴加稀H2SO4,若沉淀产生则说明BaCl2已过量。
③根据以上数据得出Na2SO3的质量分数为_____。
④小丽同学经认真分析,上述实验操作均正确,但发现实验结果与预期相差较大,请你推测可能的原因是______,验证方法__________。
-
化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验,请你参与并完成对有关问题的解答。
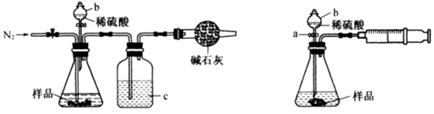
图1 图2
(1)甲同学用图1所示装置测定CO2的质量。实验时稀硫酸是与样品中的________ (填“Na2CO3”或"NaCl”)发生反应。仪器b的名称是________。洗气瓶c中盛装的是浓硫酸,此浓硫酸的作用是________ 。
(2)乙同学用图2所示装置,取一定质量的样品(为m g;已测得)和足量稀硫酸反应进行实验,完成样品中Na2CO3”质量分数的测定。
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的 ________上升,则装置气密性良好。
②在实验完成时,能直接测得的数据是CO2的________ (填“体积’’或“质量’’)。
(3)丙同学用下图所示方法和步骤实验:
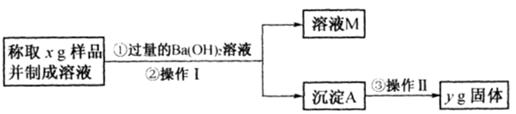
①操作I涉及的实验名称有 ________ 、洗涤;操作Ⅱ涉及的实验名称有干燥、________ 。
②丙测得的样品中Na2CO3质量分数的计算式为________。
(4)标准状况下,将672 mL CO2气通入50 mL1mol/LKOH溶液中,完全反应后,所得溶液中K2CO3和KHCO3的物质的量之比为(设反应前后溶液体积变化忽略不计)________。
-
化学兴趣小组的同学为测定某Na2CO3和NaCl的固体混合物样品中Na2CO3的质量分数进行了以下实验,请你参与并完成对有关问题的解答。

图1 图2
(1)甲同学用图1所示装置测定CO2的质量。实验时稀硫酸是与样品中的________ (填“Na2CO3”或"NaCl”)发生反应。仪器b的名称是________。洗气瓶c中盛装的是浓硫酸,此浓硫酸的作用是________ 。
(2)乙同学用图2所示装置,取一定质量的样品(为m g;已测得)和足量稀硫酸反应进行实验,完成样品中Na2CO3”质量分数的测定。
①实验前,检查该装置气密性的方法是先打开活塞a,由b注入水至其下端玻璃管中形成一段水柱,再将针筒活塞向内推压,若b下端玻璃管中的 ________上升,则装置气密性良好。
②在实验完成时,能直接测得的数据是CO2的________ (填“体积’’或“质量’’)。
(3)丙同学用下图所示方法和步骤实验:
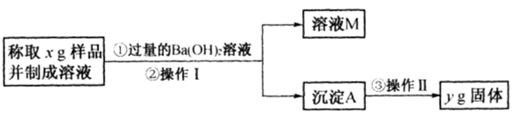
①操作I涉及的实验名称有 ________ 、洗涤;操作Ⅱ涉及的实验名称有干燥、________ 。
②丙测得的样品中Na2CO3质量分数的计算式为________。
(4)标准状况下,将672 mL CO2气通入50 mL1mol/LKOH溶液中,完全反应后,所得溶液中K2CO3和KHCO3的物质的量之比为(设反应前后溶液体积变化忽略不计)________。
-
某化学小组为测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案Ⅰ:铜铝混合物 测定生成气体的体积
测定生成气体的体积
方案Ⅱ:铜铝混合物 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是( )。
A.溶液A和B均可以是盐酸
B.溶液A和B均可以是NaOH溶液
C.溶液A和B均可选用稀硝酸
D.实验室中方案Ⅱ更便于实施
-
某化学学习小组设计以下实验方案:测定某含有NaCl的小苏打样品中 的质量分数。已知:
的质量分数。已知: 受热分解成碳酸钠、二氧化碳和水。
受热分解成碳酸钠、二氧化碳和水。
(方案一)称取一定质量样品,置于仪器A中加热至恒重后,冷却,称量剩余固体质量,计算。
(1)仪器A的名称为___________;A应该放在_________中冷却。恒重操作的目的是________。
(2)本实验从称量空的A仪器开始,完成一次平行实验至少需要称重____次。做平行实验的目的是___________。
(方案二)称取一定质量的样品(样品的质量为m0),置于小烧杯中,加适量水溶解;向小烧杯中加入足量澄清石灰水,过滤,洗涤、干燥,称量沉淀的质量为m1,计算。(已知碳酸钙式量为100, 的式量为84)。
的式量为84)。
(3)反应方程式为_____________,则样品中 的质量分数可以表示为_________。
的质量分数可以表示为_________。
(方案三)往Y形管中注入一定体积和浓度的稀硫酸并放入准确称取的ag样品,连接好注射器(如图),再将Y形管倾斜,使样品与酸液充分反应。
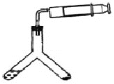
(4)a不能太大,理由是___________,若测定结果偏高,其原因可能是______(选填序号)。
①样品未完全反应
②温度未恒定即记录数据
③少量 溶解在溶液中
溶解在溶液中
(方案四)称取一定质量样品,配成待测溶液,用标准盐酸滴定。
(5)下列叙述正确的是_______(选填序号)。
①用烧杯配制100mL待测溶液
②用酚酞为指示剂
③当滴至待测液变色并能将该颜色保持半分钟即为滴定终点
④盛盐酸的滴定管未润洗会造成实验结果偏高
-
某化学小组在常温下测定一定质量的某铜铝混合物中铜的质量分数,设计了如下实验方案:
方案I:铜铝混合物 测定生成气体的体积
测定生成气体的体积
方案II:铜铝混合物 测定剩余固体的质量
测定剩余固体的质量
下列有关判断中不正确的是( )
A.溶液A和B均可以是盐酸
B.溶液A和B均可以是NaOH溶液
C.溶液A和B均只能是盐酸,不可以是NaOH溶液
D.实验室方案II更便于实施
-
某校化学研究性学习小组设计如下实验方案,测定NaHCO3和Na2CO3混合物中NaHCO3的质量分数。
方案一:按下图装置进行实验。并回答以下问题。

①按图组装仪器并检查装置的气密性。
②实验前称取17.90g样品,从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止, 从导管A处缓缓鼓入一定量的空气。
③实验结束后测得U型管增重 8.80g。
(1)B瓶中装的试剂为______,C装置的作用是__________________________。
(2)从导管A处缓缓鼓入一定量的空气的目的是_______________。
(3)该样品中NaHCO3的质量分数为_____________。
方案二:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量Ba(OH)2溶液。过滤洗涤,干燥沉淀,称量固体质量,进行有关计算。
请回答:实验中判断沉淀是否完全的方法是_____________________________________。
-
(7分)某工业纯碱中含有少量NaCl和NaOH。学生课外活动小组为测定其中Na2CO3的质量分数,采样进行分析。通过集体讨论,选择下列适当装置连接,对设计方案不断完善,成功地完成了测定实验。
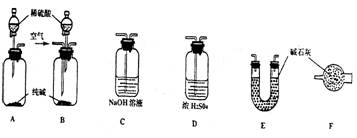
下面是甲、乙、丙、丁、戊五位同学有关设计实验装置的讨论发言。请在空白处填写他们的发言内容:
甲: 将装置A和E连接即可。因为Na2CO3与稀硫酸反应生成的CO2被E中的碱石灰吸收,通过分别测量反应前和反应后E的总质量,可求出Na2CO3的质量分数。
乙: 还应在A和E之间连接装置_____(填序号),其目的是: _________________________
丙:应该用B装置取代A。从B装置的导管口处缓缓鼓入空气,其目的是:
_______________________________________________________________
丁: 由于空气中含有CO2,若直接向B装置鼓入空气会导致实验测定结果__________(填“偏高”、“偏低”或“无影响”)。因此,应将鼓入的空气先通过装置________。
戊: E装置后还应连接装置F,其作用是___________________________________________
学生课外活动小组测定的数据如下:

计算该工业纯碱中Na2CO3的质量分数为: ___________











