-
某位同学在查阅资料时发现含氮化合物有以下性质:
①常温下NO2和N2O4混合存在,在低于0℃的过冷水中只有无色的N2O4液体或晶体存在;
②浓硝酸与铜、银等不活泼金属反应时除生成NO2气体外还有少量NO生成。
该同学在验证了“性质①”后又设计了如下装置验证“性质②”,同时测定某电器元件中铜银合金材料的含铜量。实验步骤如下:
第一步 检验装置的气密性后加入相关药品;
第二步 打开K1,通入氮气一段 时间,关闭K1,打开A中分液漏斗的活塞,向盛有7 g铜银合金粉末的圆底烧瓶中加入13.5 mol·L-1浓硝酸100 mL;
时间,关闭K1,打开A中分液漏斗的活塞,向盛有7 g铜银合金粉末的圆底烧瓶中加入13.5 mol·L-1浓硝酸100 mL;
第三步A中反应结束后……;
第四步打开K1,通入氮气一段时间。
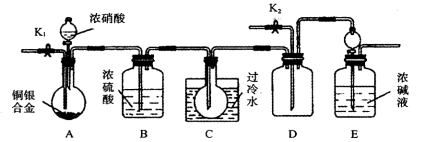
回答下列问题:
(1)实验前、后都需要打开K1,通入氮气一段时间。
“第二步”中通入氮气是为了___________________;
“第四步”中通入氮气是为了____ _______________。
_______________。
(2)“第三步”的目的是验证“性质②”并确保有害气体被完全吸收,请补全实验步骤并写出能证实“性质②”的预期现象:A中反应结束后,__________ _______________。
_______________。
(3)实验结束后,通过测量确定装置A烧瓶中溶液的体积为100 mL,装置C增重3.22 g,装置E增重0.54 g(E中N元素均以NO3-的形式存在),不考虑硝酸的挥发与分解以及空气对试剂的影响,则实验所用铜银合金中铜的质量分数为_________(结果保留3位有效数字),实验后装置A烧瓶内溶液中硝酸的物质的量浓度为_________mol·L-1。
(4)已知存在可逆反应:Ag+FeCl3 AgCl+FeCl2另一位同学提出可通过向盛有铜银合金的容器中加入足量FeCl3溶液的方法快速确定合金的含铜量,计算时所需的数据是铜银合金的质量和____________。
AgCl+FeCl2另一位同学提出可通过向盛有铜银合金的容器中加入足量FeCl3溶液的方法快速确定合金的含铜量,计算时所需的数据是铜银合金的质量和____________。
-
某位同学在查阅资料时发现含氮化合物有以下性质:
①常温下NO2和N2O4混合存在,在低于0℃的过冷水中只有无色的N2O4液体或晶体存在;
②浓硝酸与铜、银等不活泼金属反应时除生成NO2气体外还有少量NO生成。
该同学在验证了“性质①”后又设计了如下装置验证“性质②”,同时测定某电器元件中铜银合金材料的含铜量。实验步骤如下:
第一步 检验装置的气密性后加入相关药品;
第二步 打开K1,通入氮气一段时间,关闭K1,打开A中分液漏斗的活塞,向盛有7 g铜银合金粉末的圆底烧瓶中加入13.5 mol·L-1浓硝酸100 mL;
第三步A中反应结束后……;
第四步打开K1,通入氮气一段时间。
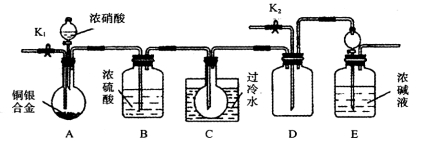
回答下列问题:
(1)实验前、后都需要打开K1,通入氮气一段时间。
“第二步”中通入氮气是为了___________________;
“第四步”中通入氮气是为了___________________。
(2)“第三步”的目的是验证“性质②”并确保有害气体被完全吸收,请补全实验步骤并写出能证实“性质②”的预期现象:A中反应结束后,______________________。
(3)实验结束后,通过测量确定装置A烧瓶中溶液的体积为100 mL,装置C增重3.22 g, 装置E增重0.54 g(E中N元素均以NO3-的形式存在),不考虑硝酸的挥发与分解以及空气对试剂的影响,则实验所用铜银合金中铜的质量分数为_______________(结果保留3位有效数字),实验后装置A烧瓶内溶液中硝酸的物质的量浓度为_______________mol·L-1。
(4)已知存在可逆反应:Ag+FeCl3 AgCl+FeCl2另一位同学提出可通过向盛有铜银合金的容器中加入足量FeCl3溶液的方法快速确定合金的含铜量,计算时所需的数据是铜银合金的质量和______________。
AgCl+FeCl2另一位同学提出可通过向盛有铜银合金的容器中加入足量FeCl3溶液的方法快速确定合金的含铜量,计算时所需的数据是铜银合金的质量和______________。
-
欲用浓硝酸法(测定反应后生成气体的量)测定某铜银合金中铜的质量分数,但资料表明:反应中除了生成NO2气体外还会有少量的NO生成;常温下NO2和N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在。为完成测定并验证确有NO生成,有人设计如下实验:

(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是___。
(2)装置B瓶的作用是___。
(3)A中的反应停止后,打开D中的活塞K2,并通入氧气,若反应确有NO产生,则D中应出现的现象是___;实验发现,通入氧气温度的高低对实验现象有较大影响,则为便于观察应通入___(填“冷”或“热”)的氧气。
(4)为减小测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是___。
(5)实验测得下列数据:所用铜银合金质量:15.0g、浓硝酸:40mL13.5mol/L;实验后A中溶液体积:40mL;H+浓度:1.0mol/L。若设反应中硝酸既无挥发也无分解,则:
①参加反应的硝酸的物质的量为___。
②若已测出反应后E装置的生成物中含氮元素的质量,则为确定合金中铜的质量分数还需要测定的数据是___。
(6)若实验只测定 Cu的质量分数,不验证NO的产生,则在铜银合金中与浓硝酸反应后,只需要简单的实验操作可达到目的,请简述实验过程:___。
-
欲用浓硝酸法(测定反应后生成气体的量)测定某铜银合金中铜的质量分数,但资料表明:
①反应中除生成NO2气体外还会有少量的NO生成;
②常温下NO2和N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在。
为完成测定并验证有NO生成,有人没计如F实验装置:
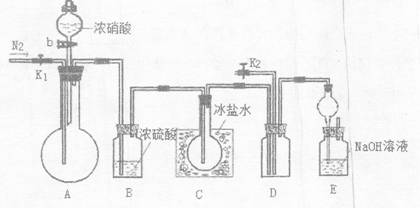
(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是________。
(2)装置中B瓶的作用是。
(3)实验时A中反应停止后,打开D装置导管的活塞K2并通入氧气,若反应确有NO产生,D中的现象是________;实验时发现通入氧气温度的高低对实验有较大的影响,为便于观察应通入____(填“冷”或“热”)的氧气,其原因是:____
(4)若实验只测定Cu的质量分数,不检验NO的产生,则在铜银合金与浓硝酸反应后,只需加入过量的____(填一种物质的化学式,下同)溶液,过滤、洗涤、干燥称量________的质量就可达目的。(已知Cu(OH)2与AgOH类似,也可以溶于过量的氨水而形成溶液。)
-
(14分)欲用浓硝酸法(测定反应后生成气体的量)测定某铜银合金中铜的质量分数。资料表明:①反应中除生成NO2气体外还有少量的NO生成;②常温下N02与N2O4混合存在,在低于0℃时几乎只有无色N2O4液体或晶体存在。为完成测定并验证有NO生成,有人设计下图实验装置。
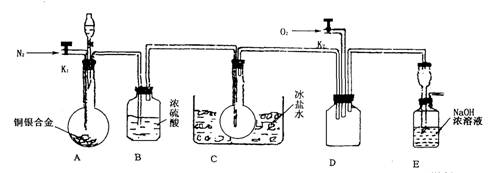
(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是_____________________________________________________________。
(2)装置B瓶的作用是__________________________________________________。
(3)A中反应停止后,打开D中的活塞K2并通人氧气,若反应中确有NO产生,则D中应出现的现象是________________;实验发现,通人氧气温度的高低对实验现象有较大影响,则为了便于观察应通人_______________(填“冷”或“热”)的氧气。
(4)为了减少测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是__________________________________________________________。
(5)实验测得下列数据:所用铜银合金质量为15.0 g,浓硝酸的体积为40 mL,浓度为13.5mol·L-1。实验后:A中溶液体积为40mL,H+浓度为1.0mol·L-1。若设反应中硝酸既无挥发也无分解,则:
①参加反应的硝酸的物质的量为______________;
②若已测出反应后E装置的生成物含氮元素的质量,则为确定合金中铜的质量分数,还需要测定的数据是__________。
(6)实验中只测定铜的质量分数,不验证NO的产生,则在铜银合金与硝酸反应后,只需简单的实验操作就可以达到目的,请简述实验过程________________________。
-
(14分)某研究性学习小组的同学利用下图来验证一定质量的铜银合金完全溶解于浓硝酸时生成的气体除NO2外还含有NO,并测定合金中铜的质量分数,已知常温下NO2和N2O4混合存在,在低于0℃时几乎只有无色的N2O4晶体。
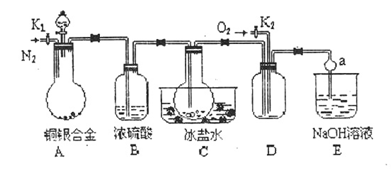
(1)写出A中铜与硝酸反应的一个化学方程式________;
(2)C装置的作用是________;
(3)反应结束后,打开活塞K2,并通入O2,若实验中有NO产生,则在D中可观察到的现象是________;
(4)反应前要先打开活塞K1持续通入一段时间的N2,其理由是________;
(5)利用A装置中反应后的溶液还可确定铜的质量分数,方法是:取出A中反应后的溶液,先向其中加入足量的________溶液,然后再进行________,________,________,________。(填操作名称)
-
某研究性实验小组欲验证浓硝酸在与Cu、Ag合金的反应过程中除生成NO2气体外,还会有少量NO生成、并测定Cu、Ag合金中Cu的质量分数。查阅相关资料表明:“常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在。”为此,他们设计了如下图所示的装置。
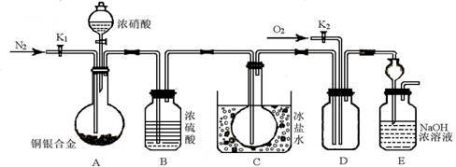
请回答下列问题
(1)写出A中Cu与HNO3反应可能的化学方程式 。
(2)实验开始前先打开A部分的活塞K1,持续通入一段时间的氮气再关闭K1,其目的是 ;装置中B瓶的作用是 。
(3)停止反应后,打开D中的活塞K2并通入O2,若有NO生成,则D中出现的现象是 ;实验发现,通入的O2温度高低对实验现象有较大影响,为便于观察应通入(填“热”或“冷”) 的O2。
(4)为减小实验误差,在A中反应完成和D中出现现象后,还应继续进行的操作是
。
(5)实验测得如下数据:实验前,Cu、Ag合金的质量:15.0g,浓HNO3:40mL 13.5 mol·L1;实验后A溶液:V=40mL c(H+)=1.0 mol·L1。假设反应中HNO3既无挥发也无分解,则:
①参加反应的HNO3的物质的量为 mol。
②若已测出反应后E装置的生成物中含氮元素的质量,则为确定合金中Cu的质量分数还需测定的数据是 。
(6)若已知Cu、Ag合金的质量为m g,且溶解完全。请利用A装置中反应后的溶液进行简单的操作,以确定合金中Cu的质量分数,其实验过程为 。
-
(14分)下图为某实验者设计的验证银圆(银和铜的合金)完全溶解于一定量的浓硝酸后生成NO2气体中含有NO的实验装置图。常温时,NO2与N2O4同时存在;在低于0℃时,几乎只有无色的N2O4的晶体存在。
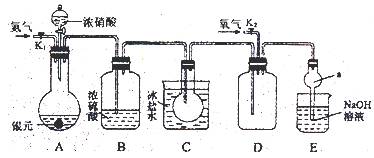
(1)反应前先打开A中的活塞K1,持续通一段时间N2,其理由是________。
(2)若装置中缺B,其后果是________。
(3)反应结束后,打开D中的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是。
(4)C装置的作用是________;E中a仪器所起的作用是________。
(5)已知该银圆的质量为25g,加入75mL 12mol·L—1的浓硝酸。实验结束后,A中烧瓶内溶液中H+的浓度为2mol·L—1(反应中HNO3既无挥发也无分解),溶液体积仍为75mL。
①参加反应的硝酸的物质的量是________。
②为测定该银圆中铜的质量分数,还需进行的主要实验操作是________。
-
(11分)下图为某实验者设计的验证银圆(银和铜的合金)完全溶解于一定量的浓硝酸后生成NO2气体中含有NO的实验装置图。常温时,NO2与N2O4同时存在;在低于0℃时,几乎只有无色的N2O4的晶体存在。
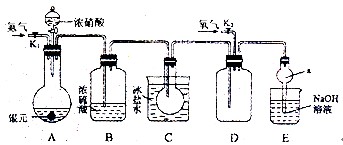
(1)反应前先打开A中的活塞K1,持续通一段时间N2,其理由是________。
(2)若装置中缺B,其后果是。
(3)反应结束后,打开D中的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是________。
(4)C装置的作用是________;E中a仪器所起的作用是________。
(5)已知该银圆的质量为25g,加入75mL 12mol·L—1的浓硝酸。实验结束后,A中烧瓶内溶液中H+的浓度为2mol·L—1(反应中HNO3既无挥发也无分解),溶液体积仍为75mL。
①参加反应的硝酸的物质的量是 。
②为测定该银圆中铜的质量分数,还需进行的主要实验操作是________。
-
(14分)某研究性实验小组欲验证浓硝酸在与Cu、Ag合金的反应过程中除生成NO2气体外,还会有少量NO生成、并测定Cu、Ag合金中Cu的质量分数.查阅相关资料表明:“常温下,NO2与N2O4混合存在,在低于0℃时几乎只有无色的N2O4液体或晶体存在.”为此,他们设计了如图所示的装置.
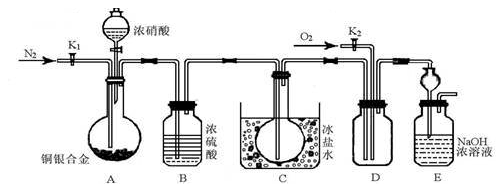
请回答下列问题
(1)写出A中Cu与HNO3反应可能的化学方式 .
(2)实验开始前先打开A部分的活塞K1,持续通入一段时间的氮气再关闭K1,其目的是 ;装置中B瓶的作用是 .
(3)停止反应后,打开D中的活塞K2并通入O2,若有NO生成,则D中出现的现象是 ;实验发现,通入的O2温度高低对实验现象有较大影响,为便于观察应通入(填“热”或“冷”) 的O2.
(4)为减小实验误差,在A中反应完成和D中出现现象后,还应继续进行的操作是 .
(5)实验测得如下数据:实验前,Cu、Ag合金的质量:15.0g,浓HNO3:40mL 13.5mol•L﹣1;实验后A溶液:V=40mL c(H+)=1.0mol•L﹣1.假设反应中HNO3既无挥发也无分解,则:
①参加反应的HNO3的物质的量为 mol.
②若已测出反应后E装置的生成物中含氮元素的质量,则为确定合金中Cu的质量分数还需测定的数据是 .

AgCl+FeCl2另一位同学提出可通过向盛有铜银合金的容器中加入足量FeCl3溶液的方法快速确定合金的含铜量,计算时所需的数据是铜银合金的质量和______________。








