-
测定生成SO3的转化率可以用下图装置,装置中烧瓶内发生的化学反应方程式为:Na2SO3(s)+H2SO4(85%)=Na2SO4+H2O+SO2↑(已知SO3的熔点是16.8oC,沸点是44.8oC)
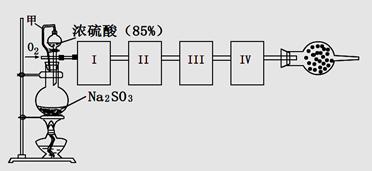
(1)装置中甲管的作用是__________________。
(2)根据实验需要,应该在I、II、III、IV处连接合适的装置,请从下图A?E装置中选择最适合装置并将其序号填至下面的空格中,每个装置不重复使用。
I、 II、III、IV处连接的装置分别是________。
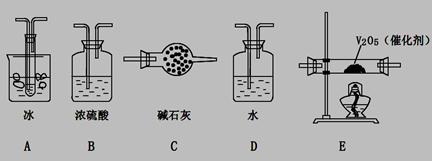
(3)为使SO2有较高的转化率,实验中加热催化剂与滴加浓硫酸的顺序中,应采取的操作是____________ ,若用大火加热烧瓶时,SO2的转化率会____________ (填“升高”、“不变”或“降低”)。
(4)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因(可以不填满)①原因:______ ②原因 :______ ③原因:______
(5)将SO2通入含1mol氯酸的溶液中,可生成一种强酸和一种氧化物,并有6.02×1023个电子转移,则该反应的化学方程式为________
(6)用n mol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置IV增重了 mg,则实验中SO2的转化率为________。(用含m、n的代数式填写)
-
(18分)测定SO2转化成SO3的转化率可以用下图装置,装置中烧瓶内发生的化学反应方程式为:Na2SO3(s)+H2SO4(85%)=Na2SO4+H2O+SO2↑。
(已知SO3的熔点是16.8℃,沸点是44.8℃)
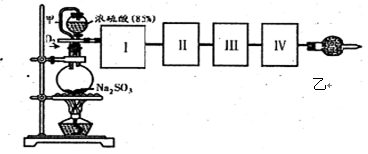
(1)装置中甲管的作用是________;
乙装置的作用是________。
(2)根据实验需要,应该在I、II、Ⅲ、IV处连接合适的装置,请从下图A~E装置中选择最适合装置并将其序号填放下面的空格中。I、Ⅱ、Ⅲ、Ⅳ处连接的装置分别是________、________、________、________。
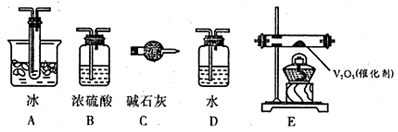
(3)为使SO2有较高的转化率,实验中加热催化剂与滴加浓硫酸的顺序中,应采取的操作是________,若用大火加热烧瓶时,SO2的转化率会________(填“升高”、“不变”或“降低”)。
(4)将SO2通入含1 mol氯酸的溶液中,可生成一种强酸和一种氧化物,并有6.02×1023个电子转移,则该反应的化学方程式为________。
(5)用nmolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅳ增重了mg,则实验中SO2的转化率为________。(用含m、n的代数式填写)
-
测定转化成SO3的转化率可以用如图装置,装置中烧瓶内发生的化学反应方程式为:
Na2SO3(s)+H2SO4(85%)=Na2SO4+H2O+SO2↑(已知S03的熔点是16.8℃,沸点是44.8℃)
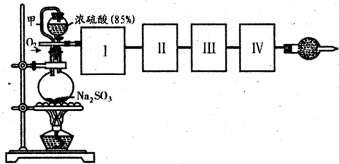
(1)装置中甲管的作用是______.
(2)根据实验需要,应该在I、II、III、IV处连接合适的装置,请从题图A〜E装置中选择最适合装置并将其序号填放下面的空格中.I、II、III、IV处连接的装置分别是______

(3)为使SO2有较高的转化率,实验中加热催化剂与滴加浓硫酸的顺序中,应采取的操作是______,若用大火加热烧瓶时,SO2的转化率会______ (填“升高”、“不变”或“降低”).
(4)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因(可以不填满)①原因:______②原因:______ ③原因:______
(5)将SO2通入含1mol氯酸的溶液中,可生成一种强酸和一种氧化物,并有6.02×1023个电子转移,则该反应的化学方程式为______
(6)用nmolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2-段时间后,测得装置IV增重了 mg,则实验中SO2的转化率为______.(用含m、n的代数式填写)
-
用如图装置可以进行测定SO2转化成SO3的转化率的实验.已知SO3的熔点是16.8℃,沸点是44.8℃.已知发生装置中所涉及反应的化学方程式为:Na2SO3(s)+H2SO4(85%)═Na2SO4+SO2↑+H2O
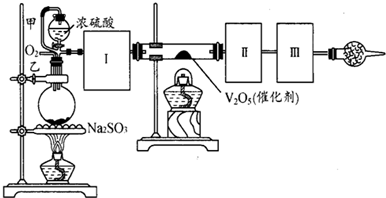
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置.请从图A~E装置中选择最适合装置并将其序号填入下面的空格中.Ⅰ、Ⅱ、Ⅲ处连接的装置分别是________、________、________.
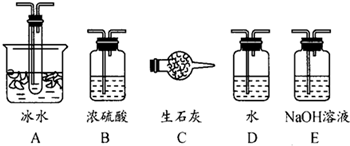
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是________.
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(可以不填满).
①原因________,验证方法________;
②原因________,验证方法________;
③原因________,验证方法________.
(4)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式________.
(5)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为________%(用含a、b的代数式填写)
-
用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是44.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s)+ H2SO4(85%)=Na2SO4+ SO2↑+ H2O
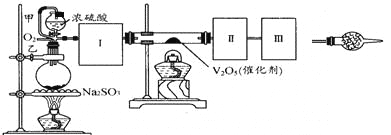
根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合Ⅰ、Ⅱ、Ⅲ处连接的装置分别是____________、_____________、__________。
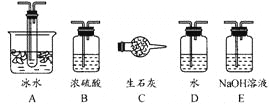
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是_________________。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(写2点)。
①原因____________,验证方法___________________;
②原因____________,验证方法___________________;
(4)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式_______________;
(5)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为__________%(用含a、b的代数式填写)。
-
(13分)用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是16.8℃,沸点是44.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s)+ H2SO4(85%)=Na2SO4 + SO2↑+ H2O
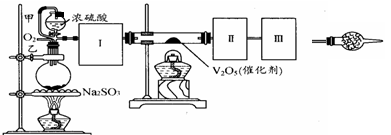
根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~E装置中选择最适合Ⅰ、Ⅱ、Ⅲ处连接的装置分别是、、。
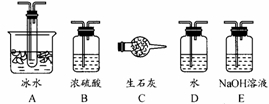
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,首先应采取的操作是________。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法(写2点)。
① 原因,验证方法
② 原因,验证方法
(4)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式________
(5)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为________%(用含a、b的代数式填写)
-
用下图装置可以进行测定SO2转化成SO3的转化率的实验.已知SO3的熔点是 16.8℃,沸点是44.8℃.已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s)+H2SO4(80%) Na2SO4+SO2↑+H2O(注:80%H2SO4具有浓硫酸的特性)
Na2SO4+SO2↑+H2O(注:80%H2SO4具有浓硫酸的特性)

(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置.请从下图A~D装置中选择最合适的装置并将其序号填入下面的空格中.Ⅰ、Ⅱ、Ⅲ处连接的装置分别是______、______、______.
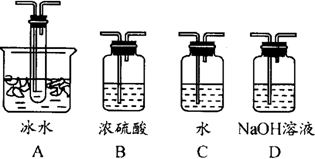
(2)在实验中“加热催化剂”与“滴加浓硫酸”的操作,首先应采取的操作是______.
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法.
①原因______.验证方法______.
②原因______.验证方法______.
(4)将足量SO2通入含1.0mol次氯酸的溶液中,有1.204×1024个电子转移,生成两种强酸,该反应的化学方程式为______.
(5)用25.2gNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间将反应产生的SO2全部排出,测得装置Ⅲ增重了3.2g,则SO2的转化率为______.
-
用下图装置可以进行测定SO2转化成SO3的转化率的实验.已知SO3的熔点是16,8℃,沸点是445.8℃.已知发生装置中所涉及反应的化学方程式为:Na2SO3(s)+H2SO4(98%)═Na2SO4+H2O+SO2↑
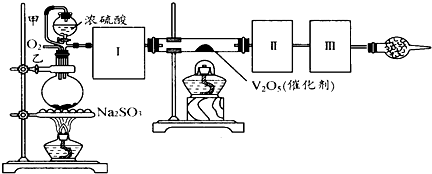
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置.请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中.
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是______、______、______.

(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作是______.
(3)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式______
(4)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为______%(用含a、b的代数式填写)
(5)尾端球形干燥管的作用是______.
-
用下图装置可以进行测定SO2转化成SO3的转化率的实验.已知SO3的熔点是16,8℃,沸点是445.8℃.已知发生装置中所涉及反应的化学方程式为:Na2SO3(s)+H2SO4(98%)═Na2SO4+H2O+SO2↑
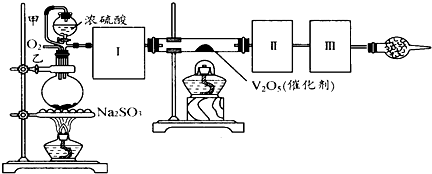
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置.请从下图A~E装置中选择最适合装置并将其序号填入下面的空格中.
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是__________、__________、__________.
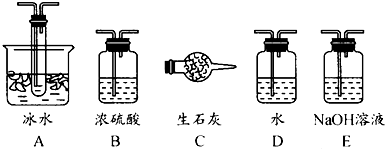
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验中在加热催化剂与滴加浓硫酸的顺序中,应采取的操作是__________________.
(3)将SO2通入含1.5mol氯酸的溶液中,可生成一种强酸和一种氧化物,若有1.5×6.02×1023个电子转移时,该反应的化学方程式______________
(4)用amolNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,测得装置Ⅲ增重了bg,则实验中SO2的转化率为______%(用含a、b的代数式填写)
(5)尾端球形干燥管的作用是__________________.
-
用下图装置可以进行测定SO2转化成SO3的转化率的实验。已知SO3的熔点是 16.8℃,沸点是44.8℃。已知发生装置中所涉及反应的化学方程式为:
Na2SO3(s)+H2SO4(80%)  Na2SO4+SO2↑+H2O
Na2SO4+SO2↑+H2O
【注:80%H2SO4具有浓硫酸的特性】
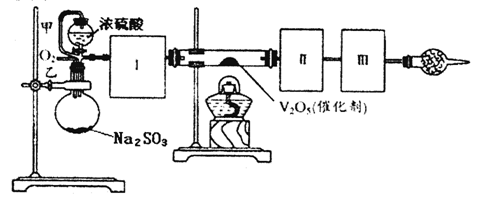
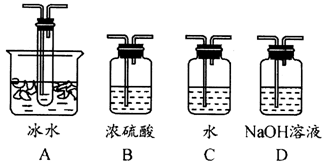
(1)根据实验需要,应该在Ⅰ、Ⅱ、Ⅲ处连接合适的装置。请从下图A~D装置中选择最合适的装置并将其序号填入下面的空格中。
Ⅰ、Ⅱ、Ⅲ处连接的装置分别是___________、_____________、_____________。
(2)在实验中“加热催化剂”与“滴加浓硫酸”的操作,首先应采取的操作是___________。
(3)有一小组在实验中发现,SO2气体产生缓慢,以致后续实验现象不明显,但又不存在气密性问题,请你推测可能的原因并说明相应的验证方法。
①原因__________________________________________________.
验证方法________________________________________________.
②原因__________________________________________________.
验证方法________________________________________________.
(4)将足量SO2通入含1.0mol次氯酸的溶液中,有1.204×1024个电子转移,生成两种强酸,该反应的化学方程式为______________________________。
(5)用25.2gNa2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间将反应产生的SO2全部排出,测得装置Ⅲ增重了3.2g,则SO2的转化率为__________。



















