控制变量法是化学实验的常用方法之一。下图实验探究影响反应速率的因素是

A. 浓度 B. 温度 C. 催化剂 D. 固体质量
高一化学选择题中等难度题
控制变量法是化学实验的常用方法之一。下图实验探究影响反应速率的因素是

A. 浓度 B. 温度 C. 催化剂 D. 固体质量
高一化学选择题中等难度题
控制变量法是化学实验的常用方法之一。下图实验探究影响反应速率的因素是

A. 浓度 B. 温度 C. 催化剂 D. 固体质量
高一化学选择题中等难度题查看答案及解析
某同学设计了探究影响反应速率因素的两组实验,探究的因素是
| 第一组 | 第二组 |
A.浓度 B.压强 C.温度 D.催化剂
高一化学单选题简单题查看答案及解析
在下列影响化学反应速率的因素中,能使化学反应速率加快的方法是( )
①升高温度 ②加入催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末
A. ①②③ B. ①②④ C. ①③④ D. ①②③④
高一化学单选题简单题查看答案及解析
在下列影响化学反应速率的外界因素中,肯定能使化学反应速率加快的方法是:①升高温度 ②加入正催化剂 ③增大反应物浓度 ④将固体块状反应物磨成末⑤增大压强
A.①②③⑤ B.①②④⑤ C.①③④⑤ D.①②③④
高一化学选择题简单题查看答案及解析
某实验小组探究H2O2分解的速率及影响因素,在相同温度下按照下表所示的方案完成实验。

(1)上述实验方案中,探究的变量因素只有催化剂的实验组合是_____和_____。
(2)实验④过程中氧气的生成速率和时间的趋势关系如图所示,判断该反应是反应(填“放热”或“吸热”)______。
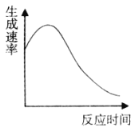
(3)实验⑤:在试管中加入10mL 0.4mol/L H2O2溶液,加入固体催化剂,在一定温度下测得不同时刻生成O2的体积(以折算为标准状况)如下表所示(假设反应过程溶液的体积保持不变):

①反应6min,H2O2分解了_______%。
②0至6min,以H2O2的浓度变化表示的反应速率为υ(H2O2)=________mol▪L-1▪min-1。
高一化学填空题简单题查看答案及解析
影响化学反应速率的因素很多,下列措施不能加快化学反应速率的是
A. 降低温度 B. 升高温度 C. 使用催化剂 D. 增加反应物浓度
高一化学选择题简单题查看答案及解析
某探究小组用盐酸与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HCl浓度为1.00mol/L、2.50mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、40℃,每次实验盐酸的用量为25.00mL,大理石用量为10.00g。
(1)写出盐酸与大理石反应的化学方程式________
(2)请完成以下实验设计表,并把实验中空缺处补充完整:
| 实验 编号 | 温度 (℃) | 大理石 规格 | HCl浓度(mol/L) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.50 | (I)实验①和②探究温度对反应速率的影响; (II)实验①和③探究浓度对反应速率的影响; (III)实验①和④探究______对反应速率的影响 |
| ② | __ | 粗颗粒 | 2.50 | |
| ③ | 25 | 粗颗粒 | ___ | |
| ④ | 25 | 细颗粒 | 2.50 |
(3)实验①中CO2质量随时间变化的关系见下图。计算实验①中70s-90s范围内用HCl表示的平均反应速率 ______(忽略溶液体积变化)
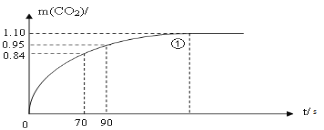
高一化学实验题中等难度题查看答案及解析
某学习小组,用稀HNO3与大理石反应过程中质量减小的方法,探究影响反应速率的因素。所用HNO3浓度为1.00 mol·L-1、2.00 mol·L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为298 K、308 K,每次实验HNO3的用量为25.00 mL、大理石用量为10.00 g。
实验设计如表:
| 编号 | T/K | 大理石规格 | HNO3浓度 |
| ① | 298 | 粗颗粒 | 2.00 mol·L-1 |
| ② | 298 | 粗颗粒 | 1.00 mol·L-1 |
| ③ | 308 | 粗颗粒 | 2.00 mol·L-1 |
| ④ | 298 | 细颗粒 | 2.00 mol·L-1 |
将相应的实验目的填入下列空格中:
(1)实验①和②探究对该反应速率的影响;
(2)实验①和③探究________对该反应速率的影响;
(3)实验①和④探究________对该反应速率的影响
高一化学探究题简单题查看答案及解析
(8分)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00 mol・L-1、2.00 mol・L-1,大理石有细颗粒与粗颗粒两种规格,实验温度为20℃、35℃ ,每次实验HNO3的用量为25.0 mL、大理石用量为10.00 g。
请完成以下实验设计表,并在实验目的一栏中填出对应的实验编号:
| 实验 编号 | T/℃ | 大理石 规格 | HNO3浓度 (mol・L-1) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和 探究温度对该反应速率的影响; (Ⅲ)实验①和 探究大理石规格(粗、细)对该反应速率的影响; |
| ② | ||||
| ③ | 粗颗粒 | 2.00 | ||
| ④ | 25 |
高一化学实验题困难题查看答案及解析
(1)某探究小组用HNO3与大理石反应过程中质量减小的方法,研究影响反应速率的因素。所用HNO3浓度为1.00mol/L、2.00mol/L,大理石有细颗粒和粗颗粒两种规格,实验温度为25℃、35℃,每次实验HNO3的用量为25.0mL.大理石用量为10.00g。
请完成以下实验设计表,并在实验目的一栏中填空:
| 实验编号 | 温度/℃ | 大理石规格 | HNO3浓度(mol/L) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (I)实验①和②探究浓度对反应速率的影响 |
| ② | 25 | 粗颗粒 | _____ | (II)实验①和③探究温度对反应遮率的影响; |
| ③ | _____ | 粗颗粒 | 2.00 | (III)实验①和④探究_________对反应速率的影响 |
| ④ | 25 | 细颗粒 | 2.00 |
(II)把2.5 mol A和2.5 mol B混合放入2 L密闭容器里,发生反应: 3A(g)+B(g)xC(g)+2D(g),经5s后反应达到平衡。在此5s内C的平均反应速率为0.2 mol/(L·s),同时生成1 mol D。试求:
(1)达到平衡时B的转化率为_____。
(2) x的值为______ 。
(3)若温度不变,达到平衡时容器内气体的压强是反应前的______倍。
高一化学实验题中等难度题查看答案及解析