现代无机化学对硫氮化合物的研究是最为活跃的领域之一。如图是已经合成的最著名的硫氮化合物的分子结构。
下列说法正确的是( )
A.该物质的分子式为SN
B.该物质的分子中所有原子的最外层都达到8电子稳定结构
C.含有1 mol的该物质的微粒中含有共价键为8NA
D.该物质与化合物S2N2互为同位素
高三化学选择题中等难度题
现代无机化学对硫氮化合物的研究是最为活跃的领域之一。如图是已经合成的最著名的硫氮化合物的分子结构。
下列说法正确的是( )
A.该物质的分子式为SN
B.该物质的分子中所有原子的最外层都达到8电子稳定结构
C.含有1 mol的该物质的微粒中含有共价键为8NA
D.该物质与化合物S2N2互为同位素
高三化学选择题中等难度题
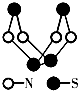
现代无机化学对硫氮化合物的研究是最为活跃的领域之一。如图是已经合成的最著名的硫氮化合物的分子结构。
下列说法正确的是( )
A.该物质的分子式为SN
B.该物质的分子中所有原子的最外层都达到8电子稳定结构
C.含有1 mol的该物质的微粒中含有共价键为8NA
D.该物质与化合物S2N2互为同位素
高三化学选择题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析

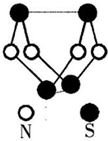
高三化学选择题中等难度题查看答案及解析
高三化学选择题中等难度题查看答案及解析
下图是已经合成的著名的硫-氮化合物的分子结构。下列说法正确的是
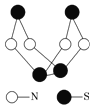
A.该物质的分子式为SN
B.该物质的分子中只有极性键,没有非极性键
C.该物质分子中N-S键键能很大,故其晶体有很大的硬度
D.该物质与化合物S2N2互为同素异形体
高三化学单选题简单题查看答案及解析
[物质结构与性质一选修3]
种类繁多的碳族元素的单质及其化合物,有着重要的研究价值。
(1)锗(Ge)的含量十分稀少,但它被广泛应用于电子、光学、化工、生物医学、能源及其他高新科技领域。
①现代化学中,常利用__________上的特征谱线来鉴定元素。基态锗原子中,核外能级最高的原子轨道上,具有的电子数为___________。
②通常状况下GeCl4是无色液体,易挥发,其熔点为-51.50C,沸点为86.55℃,能溶于乙醚。由此可推知GeCl4应属于共价化合物,其理由是_______,也即氯和锗两元素的电负性相差应该_______1.7(填“小于”或“大于”)。
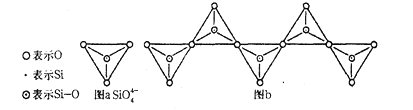
(2)在硅酸盐中,如图a所示为四面体结构,它可以通过公用顶角0原子,形成链状层状、岛状和网状结构的不同硅酸盐。图b表示由n个四面体连接成的硅酸根,其中Si的杂化形式为_____,Si与O的原子个数比为________,化学式可表示为__________。
(3)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图(a)所示。图(b)是一个石墨的六方晶胞示意图。
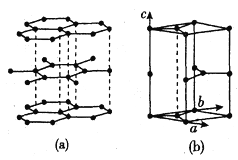
①请在图中画出晶胞沿c轴的投影 (用“·”标出碳原子位置即可)_________。
②假设石墨晶胞高为h cm,C-C键长为r cm,则石墨晶体密度的表达式为__________g.cm-3(阿伏加德罗常数为NA)。
高三化学综合题中等难度题查看答案及解析
2001年诺贝尔化学奖被美国的诺尔斯、夏普雷斯和日本的野依良治获得,他们发现了某些手性分子可用作某些化学反应的催化剂,为合成对人类有用的重要化合物开辟了一个全新的研究领域。在有机物分子中,若某个碳原子连接4个不同的原子或基团,则这种碳原子称为“手性碳原子”,如。若同一个碳原子上连着2个碳碳双键(如C="=C==C" )时,极不稳定,因此这种结构不存在。某链烃C7H10的众多同分异构体中:
(1)处于同一平面上的碳原子数最多有_______。
A.6个 B.5个 C.7个 D.4个
(2)含有“手性碳原子”,且与足量H2发生加成反应后仍具有“手性碳原子”的有5种。它们的结构简式除以下3种外,还有_______、_______。
①
②
③
(3)含有“手性碳原子”,但与足量H2发生加成反应后,不具有“手性碳原子”的结构简式是_________________。
高三化学填空题困难题查看答案及解析
法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得诺贝尔化学奖。轮烷是一种分子机器的“轮子”,芳香化合物a、b、c是合成轮烷的三种原料,其结构如下图所示。下列说法不正确的是
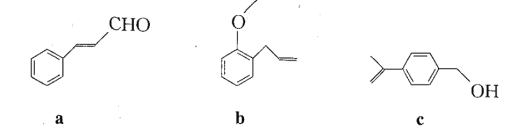
A.b、c互为同分异构体
B.a、c分子中所有碳原子均有可能处于同一平面上
C.a、b、c均能发生氧化反应、加成反应、加聚反应和酯化反应
D.a、b、c均能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色
高三化学单选题中等难度题查看答案及解析
氨的合成与应用一直是众多科学家研究的热门话题,目前该研究领域已经催生了三位诺贝尔化学奖得主,N2不仅可以与H2合成氨气,N2还可以与其他物质反应生成氨气,回答下列相关问题:
(1)德国化学家哈伯研究“N2(g)+3H2(g)2NH3(g)”反应贡献巨大,1918年荣获诺贝尔化学奖,已知该反应在298K时,△H=-92.2 kJ/mol,Kc=4.1×106(mol/L)-2
①若从平衡常数角度分析,反应限度已经较大,但为何化工生产中还需要使用催化剂:____________________________________________
②升高温度,反应物的转化率会降低,而实际化工生产中常常采用700K左右的温度,其原因是____________________________________________。
(2)1931年,科学家卡尔博施因改进合成氨方法而荣获该年度诺贝尔化学奖。研究发现,催化剂Fe3O4·Al2O3)颗粒大小不同、温度不同,平衡混合气体中氨气的含量不同由如图可以得出合成氨的适宜条件是_________________________________
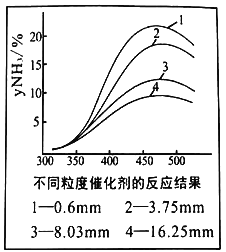
(3)2007年,德国埃特尔发现了合成氨催化机理,开端了表面动力学的研究。研究发现,常温恒压密闭容器中,N2在催化剂表面可以与水发生反应:2N2(g)+6H2O(l)4NH3(g)+3O2(g)
①下列各项能够作为判断该反应一定达到平衡的依据是___________(填标号)。
A.容器中N2(g)、NH3(g)、O2(g)的浓度之比为2:4:3
B.N2与NH3浓度之比恒定不变
C.v(N2)正=2v(NH3)逆
D.混合气体中氨气的质量分数不变
E.压强保持不变
②平衡后若分别改变下列一个条件,可以使N2转化率增大的是___________(填标号。)
A.转移掉部分O2 B.转移掉部分NH3
C.适当增加H2O(l)的量 D.增加N2的量
(4)科学研究发现,天然气CH4(g)与N2(g)在催化剂作用下可以直接用于合成氨气,同时生成副产物焦炭,已知每转移1mol电子,该反应吸收的热量为QkJ。
①写出该反应的热化学反应方程式_________________________________
②700℃时,将3molCH4与3molN2在2L的恒定密闭容器中发生上述反应,达到平衡时生成 amolC,求此时混合气体中氨气的体积分数______________________(用含a的数学表达式即可,下同);该温度下的平衡常数Kc=_________________________________。
高三化学填空题中等难度题查看答案及解析
法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得诺贝尔化学奖。轮烷是一种分子机器的“轮子”,芳香化合物a、b、c是合成轮烷的三种原料,其结构如下图所示。下列说法不正确的是
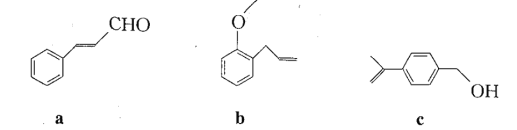
A. b、c互为同分异构体
B. a、c分子中所有碳原子均有可能处于同一平面上
C. a、b、c均能发生氧化反应、加成反应、加聚反应和酯化反应
D. a、b、c均能使酸性高锰酸钾溶液和溴的四氯化碳溶液褪色
高三化学单选题中等难度题查看答案及解析