-
X、Y、Z是位于不同周期的三种短周期元素,且原子序数逐渐增大,X、Z位于同一主族,三种元素可以形成原子个数比为1∶1∶1的化合物W。下列推测正确的是 ( )。
A.元素Z的氧化物一定属于碱性氧化物
B.原子半径:X<Y<Z
C.三种元素中,Y的金属性最强
D.Y、Z都能形成含氧酸,且前者的酸性比后者强
高三化学选择题中等难度题查看答案及解析
-
X、Y、Z是位于不同周期的三种短周期元素,且原子序数逐渐增大,X、Z属于同一主族,三种元素可以形成原子个数比为1:1:1的化合物W。下列推测正确的是
A.元素Z的氧化物一定属于碱性氧化物
B.原子半径关系是:X<Y<Z
C.三种元素中,Y的金属性最强
D.Y、Z都能形成含氧酸,且前者的酸性比后者酸性强
高三化学选择题中等难度题查看答案及解析
-
原子序数依次增大的A、B、C、D、E五种位于不同短周期的元素,可以两两形成多种原子个数比为1:1的化合物,其中的甲、乙、丙、丁4种化合物有两种属于离子化合物.A、B的原子序数之和是元素D的一半.B既是蛋白质的重要组成成分,也是某种化肥的组成部分.只有C为金属元素,焰色反应呈黄色.请回答下列问题:
(1)元素E在周期表中的位置是________________;
(2)B和D形成的化合物甲其相对分子质量在170~190之间,且D的质量分数约为70%,则该化合物的化学式为_____;
(3)A和B形成的化合物乙为B4A4,在一定条件下可以1:1完全电离产生两种离子,其中一种为10e﹣的离子,该物质在一定条件下的电离方程式为_______________________;
(4)化合物C2D溶液在空气中长期放置会变质生成丙C2D2,用化学方程式表示该过程________;
(5)D和E以1:1形成的化合物丁中所有原子均满足8电子稳定结构,该化合物的电子式为________;该物质遇水剧烈反应,产生有刺激性气味的混合气体X和Y,同时还有固体单质产生,是已知X能使品红溶液褪色的气体,Y在标准状态下的密度为1.63g/L,该混合气体相对于H2的密度为21,上述过程对应的化学方程式为___________________________________;某研究小组同学为确定干燥的X和Y混合气体中Y的存在,设计方案如下:把干燥的X和Y与干燥的NH3混合,出现白烟,则证明有Y气体,你认为此方案_______(填“正确”或“不正确”),理由是__________________________________________________.
高三化学综合题中等难度题查看答案及解析
-
A、B、R、D、E、F是六种原子序数依次增大的短周期元素, 其中有两种非金属元素位于同一主族。已知A、B、D均能与R形成原子(或离子)个数不同的几种常见化合物。请回答下列有关问题。
(1)仅由上述信息就可以确定的元素(写出代号与元素符号)是________________,若X、Y是D、F形成的最高价氧化物对应的水化物,浓度均为0.1mol/L的X、Y溶液的pH之和为14,则X、Y的晶体熔点相对高低为(写化学式)____________________
(2) A与B、E均可形成正四面体构型的气态分子Q、P,又知P的燃烧热为1430kJ/mol,则其燃烧的热化学方程式____________________________
(3) 上述六种元素间能形成多种常见二元化合物,其中存在两类化学键的物质的电子式为_______________(写一种即可)
(4) R能形成多种单质,如R2、R3,研究表明,新近制得的一种组成为R4的分子中,每个R原子均与另外两个R原子各形成一个键,下列有关R4的说法中正确的是_______________
①R4与R3、R2互为同位素 ②R4不能与A、B、D的单质反应
③R4中各原子最外电子层均为8电子结构 ④R4是一种新型化合物
高三化学填空题简单题查看答案及解析
-
短周期元素X、Y的原子序数相差2,下列叙述正确的是
A.X与Y不可能位于同一周期
B.X与Y不可能形成原子个数比为1∶1型离子化合物
C.X离子与Y离子电子层结构可以相同,也可以不同
D.X与Y形成的共价化合物中,各原子最外层一定满足8电子的稳定结构
高三化学选择题中等难度题查看答案及解析
-
A、B、C、D、E 都是短周期元素,原子序数逐渐增大,A、B 处于同一周期,C、D、E 同处另一周期。C、B 可按原子个数比 2∶l 和 1∶1 分别形成两种离子化合物甲和 乙。A 原子的最外层电子数比次外层电子层多 3 个。E 是地壳中含量最高的金属元素。根据以上信息回答下列问题:
(1)D 元素在周期表中的位置是_______乙物质的电子式是________
(2)A、B、C、D、E 五种元素的原子半径由小到大的顺序是_____(用元素符号填写)
(3)E 的单质加入到 C 的最高价氧化物对应的水化物的溶液中,发生反应的离子方程式是___________(4)E 的单质、石墨和二氧化钛(TiO2)按比例混合,高温下反应得到的两种化合物均由两种元素组成,其中有一种产物是 TiC(在火箭和导弹上有重要应用)其反应方程式为____________
高三化学推断题中等难度题查看答案及解析
-
U、V、W、X、Y、Z是常见的短周期元素,它们的原子序数逐渐增大.其中W、X、Y、Z位于同一周期;W与X是金属元素;Y与Z是非金属元素;W与Y可形成常见的离子化合物W2Y.U元素原子最外层电子数是次外层电子数的2倍,V与Y同主族.请回答下列问题:
(1)V、W、X的原子半径由大到小的顺序为______(用元素符号表示).
(2)比较U、Z气态氢化物的稳定性______(用分子式回答).
(3)写出化合物W2Y的电子式:______.
(4)甲、乙、丙分别是U、X、Y三种元素最高价含氧酸的W盐,甲、乙都能与丙发生反应,且丙用量不同时,反应产物不同.
①向丙溶液中缓慢滴加过量的乙溶液,请按照反应过程分步写出反应的离子方程式:______、______.
②向甲溶液中缓慢滴加等物质的量的丙溶液后,所得溶液中离子浓度由大到小的顺序为:______.
(5)列举由Z元素形成单质的一种用途______(用化学方程式表示).高三化学解答题中等难度题查看答案及解析
-
五种短周期元素A、B、C、D、E,原子序数逐渐增大,A、B处于同一周期,C、D、
E同处另一周期。C、B可按原子个数比2∶l和1∶1分别形成两种离子化合物甲和乙。
A原子的最外层电子数比次外层电子层多3个。D周期序数等于D原子最外层电子数。
E原子半径是同周期中最小的(除稀有气体外)根据以上信息回答下列问题:
(1)A元素在周期表中的位置 ;
(2)乙物质中存在的化学键类型是 ;
(3)写出C与D的最高价氧化物对应的水化物相互间反应的离子方程式 ;
(4)E的单质通入C的最高价氧化物对应的水化物的溶液中反应生成的“84”消毒液的有效成分的化学式为 。
高三化学填空题中等难度题查看答案及解析
-
前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A 元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是 (填元素符号,下同),电负性最大的是 。
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式 ,1 mol AB-中含有π键的数目为 ,黄血盐晶体中各种微粒间的作用力不涉及 (填选项字母)。
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为 ,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③
、④HCHO。其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质) 。
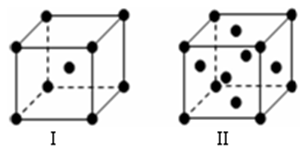
(4)金属C、F晶体的晶胞结构如图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为 。金属C的晶胞中,若设该晶胞的密度为a g/cm3,阿伏加德罗常数的值为NA,C原子的摩尔质量为M,则表示C原子半径的计算式为 cm。
高三化学填空题困难题查看答案及解析
-
前四周期原子序数依次增大的六种元素A、B、C、D、E、F中,A、B属于同一短周期元素且相邻,A 元素所形成的化合物种类最多,C、D、E、F是位于同一周期的金属元素,基态C、F原子的价电子层中未成对电子均为1个,且C、F原子的电子数相差为10,基态D、E原子的价电子层中未成对电子数分别为4、2,且原子序数相差为2。
(1)六种元素中第一电离能最小的是 (填元素符号,下同),电负性最大的是 。
(2)黄血盐是由A、B、C、D四种元素形成的配位化合物C4[D(AB)6],易溶于水,广泛用作食盐添加剂(抗结剂)。请写出黄血盐的化学式 ,1 mol AB-中含有π键的数目为 ,黄血盐晶体中各种微粒间的作用力不涉及 (填选项字母)。
a.离子键 b.共价键 c.配位键 d.金属键 e.氢键 f.分子间的作用力
(3)E2+的价层电子排布图为 ,很多不饱和有机物在E催化下可与H2发生加成反应:如①CH2=CH2、②HC≡CH、③
、④HCHO。其中碳原子采取sp2杂化的分子有 (填物质序号),HCHO分子的立体结构为 形,它加成产物的熔、沸点比CH4的熔、沸点高,其主要原因是(须指明加成产物是何物质) 。
(4)金属C、F晶体的晶胞结构如图(请先判断对应的图),C、F两种晶体晶胞中金属原子的配位数之比为 。金属C的晶胞中,若设该晶胞的密度为a g/cm3,阿伏加德罗常数的值为NA,C原子的摩尔质量为M,则表示C原子半径的计算式为 cm。

高三化学填空题困难题查看答案及解析