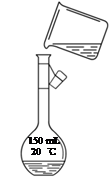-
实验室用氯化钠固体配制1.00mol/L的NaCl溶液100mL,回答下列问题:
(一)主要仪器
托盘天平、量筒、烧杯、玻璃棒、胶头滴管,还需要的玻璃仪器是______.
(二)配制步骤
(1)计算:根据n=c•V,m=n•M,则m(NaCl)=______ g.
(2)称量:用托盘天平准确称取NaCl固体______g.
(3)溶【解析】
将称好的NaCl固体放入烧杯中,用适量蒸馏水溶解;用玻璃棒搅拌,并冷却至室温.
(4)移液:
(5)洗涤:用蒸馏水洗涤烧杯内壁及玻璃棒2-3次,并将洗涤液都注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀.
(6)定容:将蒸馏水注入容量瓶,当液面距容量瓶颈刻度线1cm~2cm时,改用胶头滴管滴加蒸馏水至凹液面最低处与刻度线相切.
(7)摇匀:盖好瓶塞,反复上下颠倒,摇匀.如图是该同学转移溶液的示意图,指出图中的错误:______.
(三)若实验遇到下列情况,对NaCl溶液的物质的量浓度有何影响(填写“偏高”、“偏低”或“不变”)?
①为加速固体溶解,可稍微加热并不断搅拌.在未降至室温时,立即将溶液转移至容量瓶定容.______.
②溶解的NaCl溶液转移到容量瓶中后未洗涤烧杯:______.
③定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度.______.
-
(16分)实验室用氯化钠固体配制1.00 mol /L的NaCl溶液100 mL,回答下列问题:
1.主要仪器
托盘天平、量筒、烧杯、玻璃棒、胶头滴管,还需要的玻璃仪器是_______________。
2.配制步骤
(1)计算:根据n=c·V,m=n·M ,则m(NaCl)=__________ g。
(2)称量:用托盘天平准确称取NaCl固体__________g。
(3)溶【解析】
将称好的NaCl固体放入烧杯中,用适量蒸馏水溶解;用玻璃棒搅拌,并冷却至室温。
(4)移液:
(5)洗涤:用蒸馏水洗涤烧杯内壁及玻璃棒2-3次,并将洗涤液都注入容量瓶中,轻轻摇动容量瓶,使溶液混合均匀。
(6)定容:将蒸馏水注入容量瓶,当液面距容量瓶颈刻度线1 cm~2 cm时,
改用胶头滴管滴加蒸馏水至凹液面最低处与刻度线相切。
(7)摇匀:盖好瓶塞,反复上下颠倒,摇匀。
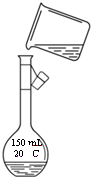
右图是该同学转移溶液的示意图,指出图中的错误:
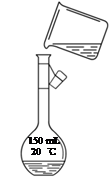
_____________________________________________。
3.若实验遇到下列情况,对NaCl溶液的物质的量浓度有何影响(填写“偏高”、“偏低”或“不变”)?
①为加速固体溶解,可稍微加热并不断搅拌。在未降至室温时,立即将溶液转移至容量瓶定容。________。
②溶解的NaCl溶液转移到容量瓶中后未洗涤烧杯:________。
③定容后,加盖倒转摇匀后,发现液面低于刻度线,又滴加蒸馏水至刻度。________ 。
-
(18分)实验室用氯化钠固体配制1.00mol/L的NaCl溶液0.5 L,回答下列问题
(1)简述该实验的主要实验步骤________
(2)所需仪器为:容量瓶 (规格:________)、托盘天平、还需要那些实验仪器才能完成该实验,请写出:________。
(3)试分析下列操作对所配溶液的浓度有何影响及造成该影响的原因。
①配制前容量瓶洗涤后没烘干,对所配溶液浓度的影响是 (偏大、偏小、无影响。以下同)
②未洗涤烧杯和玻璃棒,对所配溶液浓度的影响:________。
③为加速固体溶解,可稍微加热并不断搅拌。在未降至室温时,立即将溶液转移至溶量瓶定容。对所配溶液浓度的影响:________。
④定容后,加盖倒转摇匀后,发现溶面低于刻度线,又滴加蒸馏水至刻度。对所配溶液浓度的影响________。
-
用氯化钠固体配制1.00mol/L的NaCl溶液95mL,回答下列问题
(1)所需仪器为:托盘天平、量筒、烧杯胶头滴管,若要完成实验,还需要两种玻璃仪器为______、_____。
(2)该实验的实验步骤为:
①计算,②称量_______gNaCl, ③溶解,④移液,⑤洗涤,⑥定容,⑦ 摇匀。
(3)试分析下列操作,对所配溶液的浓度有何影响。(用偏低、偏高、无影响填空)。
①为加速固体溶解,微热烧杯溶液并不断搅拌。在未降至20℃时,就将溶液转移至容量瓶定 容。所配溶液的浓度____________;
②若定容时仰视刻度线。所配溶液的浓度______________;
③定容后,加盖、倒转、摇匀后,发现液面低于刻度线,又补加蒸馏水至刻度。则所配溶液的浓度______。
-
用氯化钠固体配制1.00mol/L的NaCl溶液95mL,回答下列问题
⑴所需仪器为:托盘天平、量筒、烧杯胶头滴管,若要完成实验,还需要两种玻璃仪器为________、。
⑵该实验的实验步骤为:
①计算,②称量________gNaCl, ③溶解,④移液,⑤洗涤,⑥定容,⑦ 摇匀。
⑶试分析下列操作,对所配溶液的浓度有何影响。(用偏低、偏高、无影响填空)。
①用天平称量氯化钠后,发现砝码底部有锈斑。所配溶液的浓度;
②为加速固体溶解,微热烧杯溶液并不断搅拌。在未降至20℃时,就将溶液转移至容量瓶定容。所配溶液的浓度________;
③容量瓶不干燥,含有少量蒸馏水。所配溶液的浓度________;
④若定容时仰视刻度线。所配溶液的浓度________;
⑤定容后,加盖、倒转、摇匀后,发现液面低于刻度线,又补加蒸馏水至刻度。则所配溶液的浓度________。
-
实验室要配制100 mL 2 mol/L NaCl溶液,请回答下列问题:
(1)配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、量筒和________。
(2)用托盘天平称取氯化钠固体,其质量为__________ g。
(3)下列主要操作步骤的正确顺序是___________(填序号)。
①称取一定质量的氯化钠,放入烧杯中,用适量蒸馏水溶解
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切
③将溶液转移到容量瓶中
④盖好瓶塞,反复上下颠倒,摇匀
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中
(4)如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度_______(填“偏高”或“偏低”或“无影响”,下同);若定容时俯视容量瓶刻度线,会造成所配溶液的物质的量浓度_________。
-
实验室要配制100 mL 2 mol/L NaCl溶液,请回答下列问题:
(1)配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、量筒和___________。
(2)用托盘天平称取氯化钠固体,其质量为__________ g。
(3)下列主要操作步骤的正确顺序是___________(填序号)。
①称取一定质量的氯化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
(4)如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度_______(填“偏高”或“偏低”或“无影响”,)
-
(4分)实验室要配制100 mL 2 mol/L NaCl溶液,请回答下列问题
(1)制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、量筒和________。
(2)用托盘天平称取氯化钠固体,其质量为________ g。
(3)若定容时俯视容量瓶刻度线,会造成所配溶液的物质的量浓度_________(偏大、偏小或无影响)。
-
实验室要配制100mL 2mol/L NaCl溶液,请回答下列问题
(1)制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、量筒和________.
(2)用托盘天平称取氯化钠固体,其质量为________ g.
(3)若定容时俯视容量瓶刻度线,会造成所配溶液的物质的量浓度________(偏大、偏小或无影响).
-
(5分)实验室要配制100 mL 2 mol/L NaCl溶液,请回答下列问题:
⑴.配制过程中需要使用的主要玻璃仪器包括烧杯、玻璃棒、胶头滴管、量筒和___________。
⑵.用托盘天平称取氯化钠固体,其质量为__________ g。
⑶.下列主要操作步骤的正确顺序是___________(填序号)。
①称取一定质量的氯化钠,放入烧杯中,用适量蒸馏水溶解;
②加水至液面离容量瓶颈刻度线下1~2厘米时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切;
③将溶液转移到容量瓶中;
④盖好瓶塞,反复上下颠倒,摇匀;
⑤用少量蒸馏水洗涤烧杯内壁和玻璃棒2~3次,洗涤液转移到容量瓶中。
⑷.如果实验过程中缺少步骤⑤,会造成所配溶液的物质的量浓度_______(填“偏高”或“偏低”或“无影响”,下同);若定容时俯视容量瓶刻度线,会造成所配溶液的物质的量浓度_________。