-
黑火药是我国古代四大发明之一,在化学史上占有重要地位。黑火药主要是硝酸钾、硫磺、木炭三者的粉末状混合物,在点燃条件下,发生的主要反应为:
KNO3+S+C―→N2↑ +CO2↑+K2S(未配平)。试填写下列空白:
(1)在黑火药燃烧的反应中,氧化剂为________,被氧化的物质为________。
(2) 硝酸钾与木炭混合点燃,即可见到焰火。试综合上述有关信息,推断硝酸钾与木炭反应的化学方程式__________________________。
高二化学填空题简单题查看答案及解析
-
(10分)(1)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成的,爆炸的反应为:S+2KNO3+3C==K2S+N2↑+3CO2↑。该反应中,KNO3 (填“被氧化”或“被还原”),C是 (填“氧化剂”或“还原剂”);得到1mol的N2需要消耗_________g 的碳单质。
(2)在3种有机物①CH2=CH2、②CH3COOH 、③蔗糖、④苯中,能用作水果催熟剂的是 (填数字序号,下同),能发生水解反应的是 ,能使紫色石蕊溶液变红的是 。
高二化学填空题中等难度题查看答案及解析
-
火药是中国古代四大发明之一,由硫磺、火硝和木炭粉均匀混合而成,点燃后可能发生的反应:S+2KNO3+3C=N2↑+3CO2↑+X(已配平),则物质X是
A. K2S B. SO2 C. H2S D. SO3
高二化学单选题中等难度题查看答案及解析
-
化学与生活密切相关,下列有关说法正确的是
A. 黑火药是我国古代四大发明之一,配方为“一硫二硝三木炭”,其中的硝是指硝酸
B. 包装食品里常有硅胶.生石灰.还原铁粉三类小包,其作用相同
C. 洪灾区民众用明矾净水并用漂白粉消毒,二者化学原理相同
D. 家中做卫生保洁时,不可将“84”消毒液与洁厕精(含浓盐酸)混合使用
高二化学单选题中等难度题查看答案及解析
-
化学与生活密切相关,下列有关说法正确的是
A.黑火药是我国古代四大发明之一,配方为“一硫二硝三木炭”,其中的硝是指硝酸
B.包装食品里常有硅胶.生石灰.还原铁粉三类小包,其作用相同
C.洪灾区民众用明矾净水并用漂白粉消毒,二者化学原理相同
D.家中做卫生保洁时,不可将“84”消毒液与洁厕精(含浓盐酸)混合使用
高二化学选择题中等难度题查看答案及解析
-
一种新型火药用高氯酸钾代替硝酸钾,用糖类代替木炭和硫磺,可避免二氧化硫等有害物质的排放,这种新型火药爆炸的热化学方程式:C6H12O6(s)+3KClO4(s)=3KCl(s)+6H2O(g)+6CO2(g) △H=xkJ/mol,已知:葡萄糖的燃烧热:△H1=akJ/mol,KClO4(s)=KCl(s)+2O2(g) △H2=bkJ/mol,H2O(g)= H2O(l) △H3=ckJ/mol,则 x 为()
A. a+3b-6c B. 6c+3a-b C. a+b-6c D. 6c+a-b
高二化学单选题中等难度题查看答案及解析
-
《天工开物》中记载了古人冶金、制陶瓷、硫磺、火药等的过程,是我国古代闪耀的“科技之光”,下列冶炼铁的过程中发生化学变化的是
A.凡铁场所在有之,其铁浅浮土面,浮者拾之
B.取来淘洗
C.入炉熔化
D.凡铁一炉载土二千余斤,或用硬木柴,或用煤炭,或用木炭,土化成铁




A. A B. B C. C D. D
高二化学单选题中等难度题查看答案及解析
-
硫及其化合物广泛分布于自然界中,硫酸工业在国民经济中占有极其重要的地位,运用相关原理回答下列问题:
(1)硫酸生产中,根据化学平衡原理来确定的条件或措施有_______(填序号)。
A.矿石加入沸腾护之前先粉碎
B.使用V2O5作催化剂
C.接触室中不使用很高的温度
D.净化后炉气中要有过量的空气
E.接触氧化在常压下进行
(2)若实验室在537℃、1.01×105Pa和催化剂存在条件下,向某密闭容器中充入2mol SO2和2mol O2,此时体积为10L,在温度和压强不变条件下20分钟后反应达到平衡,SO3体积分数为0.5。
①该温度下,从反应开始至平衡时氧气的平均反应速率是_______;
②该温度下,反应2SO2(g)+O2(g)
2SO3(g)的平衡常数的值为_______________。
(3)工业上冶炼铜主要以黄铜矿(主要成分CuFeS2)为原料,经过多歩反应将铜元素还原为铜。其中有一步为:2Cu2S+3O2(g) === 2Cu2O+2SO2。试从反应的自发性判断此反应的ΔH________0 (填“>”、“=”或“<”)。
(4)用电解的方法将硫化钠溶液氧化为多硫化物的研究具有重要的实际意义,将硫化物转变为多硫化物是电解法处理硫化氢废气的一个重要内容。如图,是电解产生多硫化物的实验装置:
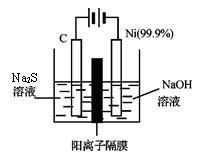
①已知阳极的反应为:(x+1)S2-=== Sx+S2-+2xe-,则阴极的电极反应式是:__________。当反应转移xmol电子时,产生的气体体积为_________(标准状况下)。
②将Na2S·9H2O溶于水中配制硫化物溶液时,通常是在氮气气氛下溶解。其原因是(用离子方程式表示):____________。溶液中离子浓度由大到小的顺序____________。
高二化学简答题困难题查看答案及解析
-
黑火药是我国历史上的四大发明之一,它的成分是硝酸钾、炭粉和硫粉的混合物,点火爆炸后的产物是二氧化碳、硫化钾和氮气。在该反应中被还原的元素为 ( )
A.S B.C C.N D.S和N
高二化学选择题简单题查看答案及解析
-
碘及其化合物在人类活动中占有重要地位。
(1)加碘食盐中含有碘酸钾(KIO3),工业上以电解法制备碘酸钾,电解设备如图所示。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:
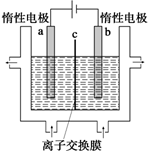
3I2+6KOH=5KI+KIO3+3H2O,再将该溶液加入________(阴极、阳极)区,另将氢氧化钾溶液加入另外一个区。使用________(阴、阳)离子交换膜,在阳极发生的电极反应式:________。
(2)碘化氢不稳定,分解反应的热化学方程式是2HI(g)
I2(g)+H2(g) ΔH=+9.48 kJ·mol-1已知ΔS>0
①该反应属于( )
A.任何温度均自发 B.任何温度均不自发 C.高温自发 D.低温自发
②一定条件下,反应在一个带有活塞的密闭容器中达到平衡,下列说法中不正确的是( )
A.恒温,缩小体积,平衡常数不变
B.恒温,缩小体积,平衡不移动,颜色加深
C.恒容,升温,正向反应速率和逆向反应速率均增大
D.恒容,在容器中若投入2mol HI,达到平衡时吸收9.48 kJ 的热量
③一定温度下,平衡常数K=1/4,在2L的容器中,加入4molHI发生反应达到平衡,HI的转化率________。
高二化学填空题极难题查看答案及解析