-
用9mol/L的浓硫酸稀释成 0.9mol/L的稀硫酸 100mL ,回答下列问题:
(1)需要取浓硫酸__________ mL
(2)如果实验室用98%的浓硫酸(密度为1.8g·cm-3 ) 配制3. 6 mol·L-1的稀硫酸250mL。计算所需浓硫酸的体积为_____________mL。
(3)由于错误操作, 使得浓度数据比理论值偏大的是__________________(填写序号)。
A.使用容量瓶配制溶液时, 俯视液面定容后所得溶液的浓度
B.没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中
C.容量瓶用蒸馏水洗净,没有烘干
D.定容时,滴加蒸馏水时液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
E.溶液稀释后未冷却至室温就转移到容量瓶并定容
高二化学填空题简单题查看答案及解析
-
(6分)用9mol/L的浓硫酸稀释成 0.9mol/L的稀硫酸 100mL ,回答下列问题:
(1)配制操作可分解成如下几步,以下正确的操作顺序是_____________________
A 向容量瓶中注入少量蒸馏水,检查是否漏水
B 用少量蒸馏水洗涤烧杯及玻璃棒,将溶液注入容量瓶,并重复操作两次
C 用已冷却的稀硫酸注入已检查不漏水的容量瓶中
D 根据计算,用量筒量取一定体积的浓硫酸
E.将浓硫酸沿烧杯壁慢慢注入盛有蒸馏水的小烧杯中,并不断用玻璃棒搅拌
F.盖上容量瓶塞子,振荡,摇匀
G.用胶头滴管滴加蒸馏水,使溶液凹面恰好与刻度相切
H.继续往容量瓶中小心地加蒸馏水,使液面接近刻度线1~2 cm
(2)如果实验室用98%的浓硫酸(密度为1.8g·cm-3 ) 配制3. 6 mol·L-1的稀硫酸250mL。计算所需浓硫酸的体积为_____________mL。
(3)由于错误操作, 使得到的浓度数据比正确的偏大的是___________(填写序号)。
A 使用容量瓶配制溶液时, 俯视液面定容后所得溶液的浓度
B 没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中
C 容量瓶用蒸馏水洗净,没有烘干
D 定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
E.把配好的溶液倒入用蒸馏水洗净而未干的试剂瓶中备用
高二化学填空题中等难度题查看答案及解析
-
在100g浓度为18mol/L、密度为ρ (g/cm3)的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加入水的体积为
A、小于100mL B.等于100mL C.大于100mL D.等于100/p mL
高二化学选择题中等难度题查看答案及解析
-
在100克浓度为18mol/L.密度为ρ(g/cm3)的浓硫酸中加入一定量的水稀释成9mol/L的硫酸,则加水的体积为(提示:硫酸溶液越浓,其密度越大)
A. 小于100mL B. 等于100mL
C. 大于100mL D. 无法确定
高二化学选择题困难题查看答案及解析
-
通过稀释浓硫酸配制 100mL 0.l mol• L-1 稀硫酸,不需要用到的仪器是
A.
 B.
B.
C.
 D.
D.
高二化学单选题简单题查看答案及解析
-
根据题意,完成下列问题。
(1)常温下,将1 mL 0.05mol/L的H2SO4溶液加水稀释至100 mL,稀释后溶液的pH= 。若将pH=5的硫酸溶液稀释500倍,稀释后溶液中c(SO42-):c(H+)= 。
(2)某温度时,测得0.01mol•L-1的NaOH溶液的pH为11,该溶液与pH=5的HCl溶液等体积混合(
混合后溶液体积变化忽略不计),混合后溶液pH= 。
(3)常温下,pH=5的H2SO4溶液中由水电离出的H+的浓度为c1;pH=5的Al2(SO4)3溶液中由水电离出的H+的浓度为c2,溶液中
=_____________。
(4)常温下,pH=13的Ba(OH)2溶液aL与pH=3的H2SO4溶液bL混合(混合后溶液体积变化忽略不计),若所得混合溶液呈中性,则a :b=___________,若所得混合溶液pH=12,则a:b=___________。
高二化学填空题困难题查看答案及解析
-
向100mL 18mol/L的硫酸溶液中加入足量的铜片并加热,充分反应后,被还原的硫酸物质的量 ( )
A.小于0.9 mol B.等于0.9 mol C.在0.9 mol到1.8 mol之间 D.大于1.8 mol
高二化学选择题简单题查看答案及解析
-
已知H2C2O4的电离平衡常数Ka1=5×10-2,Ka2=5×10-5,请回答下列问题:
(1)将10mL0.1mol/L的H2C2O4溶液加蒸馏水稀释到100mL后,下列变化中正确的有__。
①稀释前后溶液中c(H+)之比小于10
②溶液中所有离子浓度下降
③
不变
(2)下列溶液一定呈中性的是____
A.pH=7 B.
=10-14 C.c(H+)=
D.H2C2O4和K2C2O4的混合溶液中c(K+)=c(HC2O4-)+2c(C2O42-)
(3)草酸亚铁晶体(FeC2O4.xH2O)为淡黄色粉末,不溶于水,可作照相显影剂和用于制药工业。某化学兴趣小组称取yg样品,加入适量稀硫酸溶解,用0.1mol/L的酸性KMnO4溶液滴定测定x的值,发生的反应为Fe2++C2O42-+MnO4-→Fe3++CO2+Mn2+(未配平),滴定终点的现象为__,若滴定终点消耗20.00mLKMnO4溶液,则x=__(用含y的式子表示)。
(4)已知:亚硝酸(HNO2)性质和硝酸类似,常温下亚硝酸的电离平衡常数Ka=5.1×10-4。在该温度下向含有1mol草酸钠的溶液中加入2mol的亚硝酸,溶液中所发生反应的离子反应方程式为___。
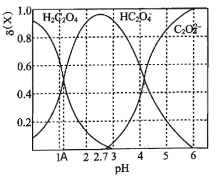
(5)T℃时,向某浓度的草酸溶液中逐滴加入一定浓度的NaOH溶液,所得溶液中三种微粒H2C2O4、HC2O4- 、C2O42-的物质的量分数(δ)与pH的关系如图所示:则A点对应的pH为__。
高二化学综合题中等难度题查看答案及解析
-
(3分)在硫酸铝、硫酸钾和明矾[KAl(SO4)2·12H2O]的混合溶液100ml中,SO42—的浓度为0.9mol/L,当加入2mol/L KOH溶液100ml时,生成的沉淀恰好完全溶解。则原混合物中K+的物质的量浓度是________.
高二化学计算题简单题查看答案及解析
-
在硫酸铝、硫酸钾和明矾[KAl(SO4)2•12H2O]的混合溶液100ml中,SO42-的浓度为0.9mol/L,当加入2mol/L KOH溶液100ml时,生成的沉淀恰好完全溶解.则原混合物中K+的物质的量浓度是________.
高二化学填空题中等难度题查看答案及解析